Rtuť
| Rtuť | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ↓ Periodická tabulka ↓ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Obecné | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Název, značka, číslo | Rtuť, Hg, 80 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cizojazyčné názvy | lat. hydrargyrum | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupina, perioda, blok | 12. skupina, 6. perioda, blok d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemická skupina | Přechodné kovy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vzhled | stříbrný kapalný kov | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikace | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Registrační číslo CAS | 7439-97-6 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomové vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Relativní atomová hmotnost | 200,59 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomový poloměr | 151 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalentní poloměr | 132±5 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waalsův poloměr | 155 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronová konfigurace | [Xe] 4f14 5d10 6s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidační čísla | 4, 2, 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativita (Paulingova stupnice) | 2,00 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionizační energie | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| První | 1007,1 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Druhá | 1810 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Třetí | 3300 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Látkové vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalografická soustava | rhomboedrální | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mechanické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hustota | 13,534 g·cm−3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenství | kapalné | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tlak syté páry | 1 Pa (315 K) 1 kPa (449 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tepelná vodivost | 8,30 W·m−1·K−1 (300 K) W⋅m−1⋅K−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termodynamické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota tání | −38,83 °C (234,32 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota varu | 356,73 °C (629,88 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenské teplo tání | 2,29 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenské teplo varu | 59,11 kJ·mol−1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Měrná tepelná kapacita | 140 J·kg−1·K−1 (20 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektromagnetické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Měrný elektrický odpor | 961 nΩ·m (25 °C) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Magnetické chování | diamagnetické | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bezpečnost | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| [1] Nebezpečí[1] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| R-věty | R61 R26 R48/23 R50/53 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S-věty | S53 S45 S60 S61 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Rtuť (chemická značka Hg, latinsky hydrargyrum), přezdívaná živé stříbro,[2] je těžký, toxický kovový prvek. Slouží jako součást slitin (amalgámů) a jako náplň různých přístrojů (teploměry, barometry). Je jediným z kovových prvků, který je za normálních podmínek kapalný. Rtuť je jedovatá[3], některé sloučeniny rtuti se řadí mezi velice toxické látky.[2][4]
Základní fyzikálně-chemické vlastnosti[editovat | editovat zdroj]

Rtuť je kapalný kovový prvek stříbřitě bílé barvy. Je nápadně těžká a dobře vede elektrický proud. Je supravodičem 1. typu, a to za teplot pod 4,154 K (Hg – α) a 3,949 K (Hg – β). Patří mezi přechodné kovy, které mají valenční elektrony v d-sféře. Ve sloučeninách se vyskytuje v mocenství Hg+ (kovalentní vazba rtuť–rtuť) a Hg2+, přičemž vlastnosti sloučenin rtuťných se podobají sloučeninám stříbrným, zatímco rtuťnaté soli připomínají spíše sloučeniny měďnaté.
Rtuť je méně reaktivní než zinek a kadmium, dobře se rozpouští v kyselině dusičné za vývoje oxidů dusíku.[5] Na vzduchu je rtuť neomezeně stálá, velmi ochotně však reaguje s elementární sírou a halogeny.
S některými kovy tvoří rtuť kapalné i pevné slitiny – amalgámy.[5] Zvláště snadno vzniká amalgám zlata a rtuť proto vzbuzovala již odedávna zájem alchymistů, kteří věřili, že s její pomocí vytvoří zlato i z jiných prvků pomocí tzv. transmutace.[6]
Výskyt a výroba[editovat | editovat zdroj]

V zemské kůře je rtuť velmi vzácná. Průměrný obsah činí kolem 0,1–0,3 mg/kg. I v mořské vodě je její koncentrace téměř na hranici měřitelnosti – 0,03 mikrogramu v jednom litru. Předpokládá se, že ve vesmíru připadá na jeden atom rtuti přibližně 120 miliard atomů vodíku.
V přírodě se rtuť vyskytuje poměrně vzácně i jako elementární prvek. Hlavním minerálem a zdrojem pro výrobu je však sulfid rtuťnatý, HgS, česky rumělka neboli cinabarit. Největší světová ložiska tohoto nerostu se nacházejí ve Španělsku, Slovinsku, Itálii, USA a Rusku.
Výroba rtuti z rumělky spočívá v jejím pražení za přístupu vzduchu podle rovnice:
- HgS + O2 → Hg + SO2
Další možností získání elementární rtuti ze sulfidických rud je její redukce kovovým železem nebo pražení rudy s přídavky oxidu vápenatého, kde probíhá následující reakce:
- 4 HgS + 4 CaO → 4 Hg + 3 CaS + CaSO4
Vzniklé rtuťové páry jsou ochlazovány, dochází k jejich kondenzaci a produktem je poměrně velmi čistá kovová rtuť. Proces destilace rtuti je i spolehlivým způsobem jejího čištění a rafinace.
Průmyslové využití rtuti přináší vážné ekologické, zdravotní a společenské problémy. Evropská unie proto přijala strategii eliminace rtuti (které předcházela roku 2002 zpráva Evropské komise), která má zahrnovat snížení emisí rtuti do prostředí, řešení problému dlouhodobých přebytků rtuti, ochranu lidí a podporu mezinárodních akcí týkajících se rtuti. Připravovaná strategie se měla bezprostředně dotýkat také sektoru nakládání s odpady.[7] Z celosvětového hlediska se roku 2009 začala připravovat a roku 2013 podepsala Minamatská úmluva o rtuti (ČR ji ratifikovalo roku 2017).
Roku 2022 byla Čína hlavní producent rtuti dodávající 91 % (2000 z 2200 tun), následována Tádžikistánem (120 tun), Mexikem (40 tun), Peru (30 tun) a Norskem (20 tun).[8] V 19. století měla Čína podíl 20 %.[9]
Využití[editovat | editovat zdroj]
Nejvýznamnější uplatnění v praxi má rtuť ve formě svých slitin s jinými kovy – amalgámy. Ochotně je vytváří s Au, Ag, Cu, Zn, Cd, Na, naopak s železnými kovy jako jsou Fe, Ni a Co nevznikají vůbec.
Dentální amalgámy[editovat | editovat zdroj]
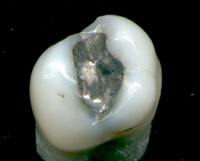
V běžném životě se nejčastěji vyskytují amalgámy dentální, používané v zubním lékařství jako velmi odolná výplň zubu po odstranění zubního kazu. Již přes 100 let se používají amalgámy, které vzniknou smísením rtuti se slitinou stříbra, mědi a cínu.[10] Poměr posledních tří prvků se liší podle jednotlivých výrobců a obchodních značek, ale obvykle je výsledný amalgám tvořen přibližně stejným váhovým množstvím rtuti jako sumy zbývajících kovových prvků.
Dentální amalgám musí splňovat řadu přísných kritérií:
- Rychlost tuhnutí musí být taková, aby lékař měl dostatek času plombu do zubu správně zasadit a mechanicky upravit, současně by však již po hodině až dvou měla být natolik tvrdá, že ji pacient může používat (kousat na ošetřený zub). Celkově amalgám tvrdne po dobu přibližně 24 hodin.
- Během tvrdnutí nesmí docházet k velkým rozměrovým změnám amalgámu – při expanzi by hrozilo roztržení zubu, při zmenšení objemu by plomba vypadávala.
- Amalgám musí být co nejvíce chemicky odolný vůči prostředí v lidských ústech, aby nedocházelo k uvolňování rtuti a zbylých kovů do organismu.
Přestože se používá amalgám v dentální medicíně stále méně a je nahrazován různými plastickými polymery, jsou jeho mechanické vlastnosti stále nejlepší ze všech zubních výplní[zdroj?]. Proto jej většina zubních lékařů používá především k výplním stoliček, kde nevadí jeho estetická nevzhlednost (tmavá barva), ale plně se uplatní jeho tvrdost a dlouhodobá mechanická odolnost.
Další amalgámy[editovat | editovat zdroj]
Další amalgám se prakticky sporadicky využívá při amalgamaci zlata při jeho těžbě z rud o vysoké kovnatosti. Jemně rozdrcená hornina se kontaktuje s kovovou rtutí a zlato prakticky kompletně přejde do kapalného amalgámu. Po oddělení od horniny se rtuť oddestiluje a vrací zpět do procesu, získané zlato se pak dále rafinuje. Velkým problémem tohoto způsobu těžby je fakt, že kompletní oddělení rtuti od zbytkové hlušiny je prakticky nemožné a dochází tak ke kontaminaci životního prostředí vysoce toxickou rtutí.
Sodíkový amalgám vznikající při elektrolýze chloridu sodného s použitím rtuťové katody se dále používá k výrobě hydroxidu sodného reakcí s vodou. Podstatná část ekologické havárie pří záplavách v roce 2002 ve Spolaně Neratovice byla způsobená zatopením provozu elektrolýzy a následnou kontaminací labské vody rtutí.
Fyzikální přístroje[editovat | editovat zdroj]


Elementární rtuť se používá jako náplň různých jednoduchých fyzikálních přístrojů – teploměrů a tlakoměrů na měření atmosférického tlaku. Ještě v nedávné době bylo zvykem udávat atmosférický tlak v mm rtuťového sloupce, přičemž normální tlak měl hodnotu 760 mm Hg. Dobré elektrické vodivosti a tekutosti rtuti i za pokojových teplot se občas využívá ke konstrukci polohových spínačů elektrického proudu (v žargonu prasátek).
Evropská unie výrobu rtuťových teploměrů zakázala.[11] Ve Spojených státech amerických se od roku 2011 přestávají kalibrovat.[12]
Výbojky a zářivky[editovat | editovat zdroj]
Elektrický výboj v prostředí rtuťových par s nízkým tlakem spolu s různými inertními plyny vyvolává silné světelné vyzařování v ultrafialové oblasti spektra. To se v luminoforu naneseném na vnitřním povrchu mění ve viditelné záření. Slouží tak při výrobě osvětlovacích těles s vyšší světelnou účinností, než klasické žárovky s wolframovým vláknem. Zářivkové trubice tak obsahují malé množství rtuti a je třeba dbát zvýšené opatrnosti při jejich likvidaci.
Polarografie[editovat | editovat zdroj]
Elektrochemická analytická technika – polarografie je založena na měření intenzity elektrického proudu mezi rtuťovou kapkovou a referenční elektrodou v závislosti na elektrickém potenciálu, vloženém na tyto elektrody. Při měření se obě elektrody ponoří do analyzovaného roztoku a zaznamenává se intenzita proudu procházejícího mezi elektrodami při plynulé změně potenciálu. Analyzované ionty obsažené v roztoku se postupně redukují podle svého redoxního potenciálu a intenzita dosaženého proudu (limitní difuzní proud) je mírou koncentrace měřené látky.
Za objev a rozvoj využití polarografické metody v analytické chemii získal akademik Jaroslav Heyrovský v roce 1959 Nobelovu cenu za chemii.
V současné době existuje v analytické elektrochemii celá řada technik, které využívají polarografického principu, nahrazují však rtuťovou kapkovou elektrodu jinými typy elektrod (rotující disková elektroda) nebo modifikují různým způsobem elektrický potenciál vložený na měrné elektrody (diferenční pulsní voltametrie).
Vakcíny[editovat | editovat zdroj]
Historicky vakcíny obsahovaly stopové množství rtuti ve sloučenině zvané thiomersal. Její přítomnost zabraňovala jednak množení bakterií, ale hlavně likvidovala případné aktivní zbytky virů (účinně likvidovala hepatitidu typu B, meningitidu, tetanus, viry dětské obrny a mnoho dalších). Jelikož některé studie ukazovaly na možnou toxicitu této látky, bylo na začátku 90. let její použití zakázáno ve Spojených státech amerických, zemích Evropské unie a v dalších zemích.[13]
Historie používání této látky vedlo v posledních letech ke vzniku velké paniky okolo očkování. Vzniklo mnoho knih na toto téma, autoři často citují některé studie, které tvrdí, že podávání těchto látek vede k vývoji autismu.[14] Autoři však mnohdy vůbec neuvádějí fakt, že přidávání této látky do vakcín je v současné době již zakázáno.
Výroba chlóru[editovat | editovat zdroj]
Velkého množství kovové rtuti se dříve používalo v chemickém průmyslu v zařízeních pro elektrolytickou výrobu chloru. Tato zařízení jsou energeticky náročná a jsou také významným zdrojem znečištění životního prostředí rtutí, a proto jsou postupně nahrazována modernější membránovou technologií. Poslední zařízení tohoto typu v Česku provozované ve Spolaně Neratovice bylo odstaveno koncem roku 2017.[15]
Sloučeniny[editovat | editovat zdroj]
Prakticky se lze setkat s dvěma řadami sloučenin rtuti: Hg+ a Hg2+. Oba typy jsou prakticky stejně stálé, vyznačují se však podstatně odlišnými chemickými a fyzikálními vlastnostmi.
Sloučeniny Hg+[editovat | editovat zdroj]
Svým chemickým chováním připomínají stříbrné soli. V těchto sloučeninách rtuť dvojvazná (–Hg–Hg–).[5]
Typický je příklad nejdůležitější rtuťné sloučeniny – chloridu rtuťného, kalomelu Hg2Cl2. Je to bílá krystalická látka velmi málo rozpustná ve vodě stejně jako AgCl. Je sice toxický jako všechny soli rtuti, ale vzhledem k nízké rozpustnosti se jen velmi obtížně může dostat z trávicího traktu do krevního řečiště. V dřívějších dobách byl dokonce medicínsky využíván jako projímadlo.
Značný význam má však kalomel v analytické chemii. V elektrochemii je prakticky nejvíce používanou referenční elektrodou kalomelová elektroda, jejíž potenciál je prakticky neměnný a je dán pouze velmi nízkou, ale stálou, koncentrací iontů Hg 2+
2 uvolněných z kalomelu v roztoku chloridu draselného (KCl).
Na přípravu roztoku rtuťné soli se používá dusičnan rtuťný (Hg2(NO3)2), přičemž na dno roztoku se dává kapka kovové rtuti, aby nedocházelo k nežádoucím redoxním dějům.
Další uplatnění nalézá kalomel v gravimetrické analýze platinových kovů, kde působí jako selektivní redukční činidlo. Podle podmínek reakce (teplota roztoku, kyselost) redukuje přídavek kalomelu různé skupiny drahých kovů jako platina, rhodium a iridium.
Sloučeniny Hg2+[editovat | editovat zdroj]

Svým chemickým chováním připomínají měďnaté soli.
Poměrně významný je chlorid rtuťnatý (HgCl2, sublimát). Tato sloučenina je ve vodě velmi dobře rozpustná a současně mimořádně toxická. Spíše pro zajímavost lze uvést, že HgCl2 v roztoku prakticky vůbec nedisociuje jako běžné iontové soli, ale v roztoku se nacházejí pouze solvatované molekuly HgCl2.
Sublimát byl dříve používán jako součást jedů na hlodavce a k moření obilí, kdy byla ta část obilí, která byla určena pro setí na příští rok, napuštěna roztokem sublimátu a tak chráněna před hlodavci. Občas však docházelo k tragickým omylům, kdy se takto ošetřené obilí dostalo do mlýna a pak sloužilo ke konzumaci v pečivu.
Sulfid rtuťnatý (HgS) je jako rumělka nejen nejvýznamnějším přírodním zdrojem rtuti, ale i od pradávna používaným barvířským pigmentem. Kromě využití v malířství byl například ve starověkém Egyptě přidávám i do líčidel a jiných kosmetických přípravků.
Fulminát rtuťnatý (Hg(ONC)2) je znám jako třaskavá rtuť. Tato sloučenina slouží k výrobě velmi často používaných pyrotechnických rozbušek. Je velmi citlivý na zvýšení teploty (například třením nebo úderem), ale za normálních podmínek je zcela stabilní.
Dimethylrtuť (Hg(CH3)2) je kapalná látka, která vzniká ze sloučenin rtuti za anaerobních podmínek působením mikroorganizmů. Má podobný bod varu jako voda, je ve vodě rozpustná, ale také je lipofilní. Asi nejznámější otrava dimethylrtutí se stala v japonské zátoce Minamata, kde byly tisíce postižených.[16][17]
Zdravotní rizika[editovat | editovat zdroj]
Rtuť patří mezi prvky, jejichž vliv na zdravotní stav lidského organismu je jednoznačně negativní. Je kumulativním jedem, stejně jako podobně se chovající kadmium. Z organismu se vylučuje jen velmi pozvolna a obtížně, jeho většina se přitom koncentruje především v ledvinách a v menší míře i v játrech a slezině. Bylo prokázáno, že rtuť může v ledvinách setrvat až desítky let. Právě ty jsou při chronické otravě rtutí nejvíce ohroženy.
Projevy chronické otravy bývají často nespecifické – od studených končetin, vypadávání vlasů, přes zažívací poruchy, různé neurologické a psychické potíže až po závažné stavy jako např. chudokrevnost, léčbě odporující chronická candidóza, revmatické choroby či onemocnění ledvin. Při jednorázové vysoké dávce rtuti se dostavují bolesti břicha, průjmy a zvracení.
Do organismu se rtuť dostává především dvěma cestami – v potravě a dýcháním. Z potravin jsou rizikovým faktorem především vnitřnosti (játra, ledviny) nebo ryby, které byly kontaminovány rtutí při svém růstu. Rizikové mohou být i zemědělské plodiny, pěstované na půdě zamořené rtuťnatými sloučeninami ať již z průmyslových zdrojů nebo nevhodně použitými přípravky k hubení zemědělských škůdců.
Elementární rtuť je zdraví člověka nebezpečná zejména v případě vdechování jejích par. I proto se doporučuje přechovávat v laboratoři rtuť, kterou nelze uzavřít do utěsněné nádoby (např. polarografické rezervoáry), překrytou vrstvou destilované vody. Kritickým orgánem při akutním vystavení parám rtuti jsou plíce. Vzniká erozivní bronchitida a postižený člověk může dokonce zemřít na respirační selhání. Poškození dýchacího ústrojí mohou být provázeny také příznaky poškození centrálního nervového systému.[18] Páry elementární rtuti totiž snadno pronikají do nervové soustavy za hematoencefalickou bariéru díky své rozpustnosti v tucích.[19] Proto také vyškolení odborníci větší množství rozlité rtuti odstraňují v protichemických oblecích vybavených dýchacími přístroji.[20]
Zvláště nebezpečné jsou organokovové sloučeniny rtuti, které se mohou snadno dostat do živých tkání a to například i pouhým stykem s pokožkou. Tyto sloučeniny se mohou dostávat do životního prostředí např. rozkladem různých organických sloučenin s obsahem rtuti nebo i metabolickými pochody mikroorganizmů při styku s rtutí. Nejčastěji uváděným příkladem je dimethylrtuť, (CH3)-Hg-(CH3), kde je jako smrtelná dávka pro dospělého člověka uváděno již 0,1 ml této kapalné substance.
Sporná je otázka dlouhodobého působení amalgámových zubních plomb, které někteří lékaři považují za zcela neškodné, jiní upozorňují na glomerulopatie a autoimunitní onemocnění, které byly ve vztahu k expozici rtuti popsány.[21] Popisované hypersenzitivní reakce na rtuť se vyznačují celkovými příznaky, vyrážkou na tváři, na krku a v místech ohybu končetin (flexní rýhy) končetin několik hodin po kontaktu. Zaznamenáno bylo i nespecifické poškození v ústech zvané lichen ruber planus.[21] Problematický je však především osud rtuti, která se uvolňuje do atmosféry při zpopelňování těchto osob v krematoriích, což je stále častější způsob pohřbu. Evropané mají v ústech více než 1 100 tun rtuti a každý rok končí jen v zemích EU asi 30 tun rtuti ze zubních amalgámů v půdě, 24 tun ve vodě a 23 tun v ovzduší.[22]
Toxicita jednotlivých sloučenin je závislá především na jejich rozpustnosti ve vodě.[18] Z tohoto pohledu jsou nejvíce rizikové sloučeniny dvojmocné rtuti Hg2+, které jsou, nebo spíše bývaly, užívány jako jedy na hubení hlodavců a jiných zemědělských škůdců.
Nebezpečnost elementární rtuti při požití je nízká. Vstřebává se cca 0,01 % požité rtuti a pokud rtuť nesetrvá v trávicím traktu delší dobu nebo není požívána dlouhodobě, nemá zřejmě žádné toxické účinky.[23]
Minimální škodlivost elementární rtuti dokazuje kuriózní příklad nepovedené sebevraždy, kdy si potenciální sebevrah vstříkl injekčně několik mililitrů rtuti do žíly. Protože pH lidské krve nedovoluje rozpouštění kovové rtuti, nestalo se naprosto nic. Rtuť nakonec skončila v srdci „sebevraha“ a on s ní žil ještě řadu let.[18]
Nejtoxičtější je rtuť ve formě organosloučenin (methylrtuť). V této podobě se nachází v rybách a organismus je schopen ji přijmout téměř ze sta procent.[zdroj?] Způsobuje neurologické poruchy, poruchy vidění, svalovou slabost, únavu, snižuje reprodukční schopnosti, prochází placentou a způsobuje psychomotorické poškození plodu.
Ekologická rizika[editovat | editovat zdroj]
Rtuť vypuštěná do životního prostředí představuje vážné riziko. Je schopna putovat na velké vzdálenosti a kontaminovat vodu a půdu i tisíce kilometrů daleko od zdroje znečištění. V Evropě se daří snižovat znečištění rtutí, ale její vypouštěné množství stále zůstává příliš velké.[24] Vážná ohrožení životního prostředí v současnosti představuje zejména používání kovové rtuti pro těžbu zlata, např. v Mongolsku,[25] Indonésii,[26] v jižní Americe[27] nebo v Africe.[28] Převážně řekami se pak dostává do oceánů.[29] Tam se dostává do masa ryb, ale minimálně od roku 1971 se koncentrace rtuti v rybách nemění.[30]
RoHS[editovat | editovat zdroj]
Vzhledem k její nebezpečnosti je omezeno používání rtuti v některých elektronických a elektrických zařízeních směrnicí RoHS spolu s olovem, kadmiem a dalšími látkami.[31]
Odkazy[editovat | editovat zdroj]
Reference[editovat | editovat zdroj]
- ↑ a b Mercury. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ a b VELEBIL, Dalibor. Dobývání rtuti v Čechách [online]. 08. 11. 2013 [cit. 2021-04-12]. Dostupné online.
- ↑ Mercury, element summary [online]. National Center for Biotechnology Information [cit. 2021-04-12]. Kapitola Uses. Dostupné online.
- ↑ Dimethylmercury, compound summary [online]. National Center for Biotechnology Information [cit. 2021-04-12]. Kapitola Toxicity. Dostupné online.
- ↑ a b c HOUSECROFT, Catherine; SHARPE, Alan. Anorganická chemie. 1. vyd. Praha: VŠCHT, 2014. 1119 s. ISBN 978-0273-74275-3. S. 820–823.
- ↑ Nová alchymie. vesmir.cz [online]. [cit. 2023-04-04]. Dostupné online.
- ↑ Miroslav Šuta: Evropská strategie eliminace rtuti Archivováno 10. 9. 2009 na Wayback Machine., Odpady, 14.7.2005
- ↑ Sheaffer, Kristin N. (2023) Mercury. USGS
- ↑ Researchers estimate anthropogenic mercury emissions from 1500 to 1900. phys.org [online]. [cit. 2023-08-18]. Dostupné online.
- ↑ Je ošetření zubu amalgámem bezpečné? | MT | Beneš & Michl. www.tribune.cz [online]. [cit. 2023-04-04]. Dostupné online.
- ↑ Evropská směrnice 2007/51/ES zakazující mimo jiné použití rtuti v lékařských přístrojích
- ↑ (anglicky) End of an era: NIST to cease calibrating mercury thermometers
- ↑ Bigham M, Copes R. Thiomersal in vaccines: balancing the risk of adverse effects with the risk of vaccine-preventable disease. Drug Saf. 2005, s. 89–101. DOI 10.2165/00002018-200528020-00001. PMID 15691220.
- ↑ Vakcinace a autismus[nedostupný zdroj], Zdravotnické noviny, 32/2005
- ↑ SPOLANA s.r.o. [cit. 2021-11-20]. Dostupné online.
- ↑ Látka: Rtuť a sloučeniny (jako Hg) Archivováno 31. 5. 2008 na Wayback Machine., Integrovaný registr znečišťování
- ↑ TED Case Studies – Minamata Disaster
- ↑ a b c Vladimír Bencko, Miroslav Cikrt, Jaroslav Lener: Toxické kovy v životním a pracovním prostředí člověka, Grada 1995, ISBN 80-7169-150-X
- ↑ Pavel Urban: AKTUÁLNÍ PROBLÉMY NEUROTOXICITY RTUTI Neurol. pro praxi, 2006; 5: 251–253
- ↑ Vylitá rtuť na ulici Masarykova Archivováno 18. 2. 2005 na Wayback Machine., 23.1.2002
- ↑ a b Milan Tuček, Vladimír Bencko, Svatopluk Krýsl: ZDRAVOTNÍ RIZIKA RTUTI ZE ZUBNÍCH AMALGÁMŮ Chem. Listy 101, 1038–1044 (2007)
- ↑ Miroslav Šuta: Dám či nedám (si) amalgám? Archivováno 9. 9. 2009 na Wayback Machine., respekt.cz, 24. leden 2008
- ↑ MERCURY – MONOGRAPH FOR UKPID
- ↑ Miroslav Šuta: Znečištění rtutí a olovem zůstává vážným problémem Evropy Archivováno 5. 3. 2009 na Wayback Machine., respekt.cz, 5. května 2008
- ↑ Mongolská zlatá horečka ničí řeky i život nomádů. Aktuálně.cz [online]. Economia, 2008-11-08 [cit. 2019-03-19]. Dostupné online.
- ↑ ISMAWATI, Yuyun; PETRLIK, Jindrich; DIGANGI, Joseph. Mercury Hotspots in Indonesia: ASGM sites: Poboya and Sekotong in Indonesia. IPEN Mercury-Free Campaign Report. 1. vyd. Denpasar: BaliFokus Foundation; IPEN; Arnika, 2013. 18 s. Dostupné online. DOI 10.13140/RG.2.2.26150.73282.
- ↑ GONZALEZ, Susana; PAREDES, Mario; PETRLIK, Jindrich. ASGM and LSGM Site: Paso Yobái in Paraguay ASGM and LSGM site: Paso Yobái in Paraguay. 1. vyd. Asinción: Alter Vida; Arnika; IPEN, 2013. 7 s. Dostupné online. DOI 10.13140/RG.2.2.12943.69282.
- ↑ Miroslav Šuta: Jak se (taky) rodí zlato Archivováno 7. 6. 2008 na Wayback Machine., respekt.cz, 29. ledna 2008
- ↑ https://phys.org/news/2021-08-rivers-largest-global-source-mercury.html - Rivers are largest global source of mercury in oceans
- ↑ Mercury levels in tuna remain nearly unchanged since 1971, study says. phys.org [online]. [cit. 2024-02-21]. Dostupné online.
- ↑ Miroslav Šuta: Zákaz některých chemikálií v nových spotřebičích Archivováno 24. 5. 2011 na Wayback Machine., Odpady, 9/2006
Literatura[editovat | editovat zdroj]
- Jursík F.: Anorganická chemie kovů. 1. vyd. 2002. ISBN 80-7080-504-8 (elektronická verze)
- Greenwood N.N., Earnshaw A.: Chemie prvků II. 1. vyd. 1993. ISBN 80-85427-38-9
- Vladimír Bencko, Miroslav Cikrt, Jaroslav Lener: Toxické kovy v životním a pracovním prostředí člověka, Grada 1995, ISBN 80-7169-150-X
- Handbook on the Toxicology of Metals, vol. II., 1986
- Beneš, J. a kol.: Životní prostředí České republiky. Ročenka 1992, MŽP ČR a ČEú, Praha 1993
- J. Píša: Narušení reprodukčních procesů působením kadmia, olova a rtuti. in: J. Cibulka a kol. Pohyb olova, kadmia a rtuti v biosféře. Akademia Praha , 1991
- H. Pohunková, H. Reisnerová: Vliv olova, kadmia a rtuti na změny ve tkáních a orgánech suchozemských živočichů.in: Pohyb olova, kadmia a rtuti v biosféře. Academia Praha, 1991.
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu rtuť na Wikimedia Commons
Obrázky, zvuky či videa k tématu rtuť na Wikimedia Commons  Slovníkové heslo rtuť ve Wikislovníku
Slovníkové heslo rtuť ve Wikislovníku- (česky) Pavel Urban: Aktuální problémy neurotoxicity rtuti, Neurológia pre prax, 5/2006 (PDF)
- (česky) Český rozhlas – Leonardo: Kauza amalgám – amalgámová výplň zubů, 6.9.2005
- (česky) Zbyněk Mlčoch: Otrava (intoxikace) rtutí – příznaky, projevy, léčba, prevence, amalgám
- (česky) Rtuť v databázi toxických látek na webu Arniky
- (anglicky) Environmental Protection Agency: Mercury – Spills, Disposal and Site Cleanup
- (anglicky) Environmental Protection Agency: Initial Risk-Based Prioritization of Mercury in Certain Products (PDF)
- (anglicky) UNEP: UNEP Global Mercury Partnership



