Atom
| Atom | |
|---|---|
 Znázornění struktury atomu helia. Elektronový obal, sestávající z orbitalu 1s, je zobrazen černě, přičemž odstín vyjadřuje hustotu pravděpodobnosti (integrovanou podél přímky pohledu). Oblast atomového jádra je vyznačena růžově; jeho zvětšenina, na které jsou červeně zobrazeny protony a fialově neutrony, je však jen schematická. Ve skutečnosti je i jádro helia (a vlnové funkce jednotlivých nukleonů) kulově symetrické. | |
| Obecné vlastnosti | |
| Klasifikace | Nejmenší částice chemického prvku |
| Fyzikální vlastnosti | |
| Klidová hmotnost | ≈ 1,67×10−27 až 4,52×10−25 kg |
| Elektrický náboj | 0 (atom má vždy stejný počet protonů a elektronů, v jiném případě se nejedná o atom, nýbrž o ion) C |
Atom (z řeckého ἄτομος, átomos – nedělitelný) je nejmenší částice běžné hmoty, částice, kterou už chemickými prostředky dále nelze dělit (ovšem fyzikálními ano – viz např. jaderná reakce) a která definuje vlastnosti daného chemického prvku. Atom se skládá z atomového jádra obsahujícího protony a neutrony a obalu obsahujícího elektrony.
Historický vývoj atomové teorie[editovat | editovat zdroj]
První představy o atomu pocházejí z antického Řecka, ve kterém v 5. století př. n. l. Démokritos představil filozofickou teorii – atomismus, podle které nelze hmotu dělit do nekonečna, neboť na nejnižší úrovni existují dále nedělitelné částice, které označil slovem atomos (ἄτομος). Podle této teorie je veškerá hmota složena z různě uspořádaných atomů různého druhu, které jsou nedělitelné, přičemž je nelze vytvářet ani ničit. Navíc se objevuje i myšlenka existence prázdného prostoru, kterým se mohou atomy pohybovat.[1]
Vědeckou formu atomové teorii poskytl na začátku 19. století John Dalton, podle kterého se každý chemický prvek skládá ze stejných atomů zvláštního typu, které nelze měnit ani ničit, ale lze je skládat do složitějších struktur (sloučenin). Na základě této teorie byl schopen vysvětlit některé otevřené otázky tehdejší chemie, např. proč při chemických reakcích reagují vždy jednoduché poměry množství příslušných látek (viz zákon násobných poměrů slučovacích).
Thomsonův (pudinkový) model atomu[editovat | editovat zdroj]
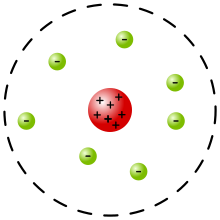
Teorii o nedělitelných atomech (přesněji částicích, které atomy nazval Dalton) však v roce 1897 vyvrátil J. J. Thomson, který při studiu katodového záření objevil elektron — tedy první subatomární částici. Na základě tohoto objevu vytvořil tzv. Thomsonův model atomu (též pudinkový model), který předpokládal, že atom je tvořen rovnoměrně rozloženou kladně nabitou hmotou, ve které jsou (jako rozinky v pudinku) rozptýleny záporně nabité elektrony.
Rutherfordův (planetární) model atomu[editovat | editovat zdroj]
Thomsonův model překonal na začátku 20. století Ernest Rutherford, který analýzou experimentů Geigera a Marsdena dokázal, že většina hmoty s kladným nábojem je umístěna ve velmi malém prostoru ve středu atomu.[2] To ho vedlo k Rutherfordově modelu, podle kterého se atom skládá z kladně nabitého hutného jádra, kolem kterého obíhají záporně nabité elektrony obdobně jako planety obíhají Slunce (proto se tento model nazývá též planetární model atomu). Později také zjistil, že jádro atomu vodíku je nejjednodušším jádrem, které je tvořeno jedinou částicí, přičemž tato částice je obsažena také v jádrech ostatních atomů. Tato částice se nazývá proton. V roce 1932 pak James Chadwick objevil neutron, který se v jádře nachází spolu s protony.
Planetární model však trpěl mnoha zásadními nedostatky: například podle všech známých zákonů by elektricky nabité těleso (elektron) obíhající po kruhové či eliptické dráze muselo vysílat elektromagnetické záření, čímž by ztrácelo energii a ve velmi krátkém čase by se všechny elektrony spirálovitě zřítily do atomových jader.
Bohrův-Sommerfeldův model atomu[editovat | editovat zdroj]
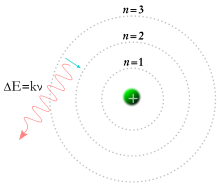
Zásadní problémy Rutherfordova modelu překonala až nová kvantová teorie, podle které je elektromagnetické záření vysíláno i pohlcováno po nedělitelných množstvích, kvantech. V roce 1913 vytvořil Niels Bohr podle této teorie Bohrův model atomu. Podle tohoto modelu obíhají elektrony atomové jádro jen na některých dovolených kruhových drahách, přičemž nemohou vyzařovat a spirálovitě padat do jádra, protože mezilehlé dráhy nejsou možné a vyzařování energie není spojité, mohou pouze za určitých podmínek jednorázovými změnami „přeskočit“ z jedné energetické hladiny do jiné.
Bohrův model byl navržen ad hoc, byl poměrně komplikovaný, ale dokázal předpovědět několik důležitých faktů o atomových spektrech. V některých ohledech však stále selhával (např. vysvětlení štěpení spektrálních čar). Bohrův model je stále založen na klasické fyzice, na rozdíl od planetárního modelu však doplnil některé postuláty, kterými se pokusil odstranit rozpory planetárního modelu. Jedná se tedy o soubor uměle definovaných fenomenologických tvrzení, o kterém byl samotný Bohr přesvědčen, že nemůže být konečným vysvětlením. Bohrovy postuláty však byly jedním z podstatných podnětů, které iniciovaly vznik kvantové teorie — nového teoretického základu, ze kterého postuláty přirozeně vyplývají.
Arnold Sommerfeld doplnil Bohrův model o vybrané eliptické dráhy oběhu elektronů a přidal příslušné postuláty. Umožnil tak dílčí vysvětlení pro rozštěpení některých spektrálních linií a některé změny spekter v magnetickém poli.
Kvantověmechanický model atomu[editovat | editovat zdroj]
Moderní kvantověmechanický model atomu vznikl na základě de Broglieho teorie částicových vln a následné Schrödingerovy práce, v níž představil tzv. Schrödingerovu rovnici, podle které elektron (stejně jako všechny ostatní částice) není popisován jako hmotný bod, ale jako vlnová funkce definující pravděpodobnosti výskytu elektronu v různých místech prostoru. Spolu s Heisenbergovými relacemi neurčitosti to znamená, že mechanistické eliptické dráhy Bohrova-Sommerfeldova modelu byly opuštěny a nahrazeny neostře definovanými oblastmi, ve kterých se elektron s určitou pravděpodobností nalézá, tzv. orbitaly.
Model založený na Schrödingerově kvantové mechanice dokázal vysvětlit mnoho atomových vlastností, které byly dřívějšími teoriemi nepředpověditelné (např. pravděpodobnosti přechodů a tedy intenzity spektrálních čar). Některé jevy v jemné struktuře spekter se však pomocí něho vysvětlit nepodařilo.
K přesnějšímu vystižení vlastností atomového obalu je potřeba relativistická kvantová mechanika. Chování elektronů tak lépe popisuje relativistická Diracova rovnice, ze které přirozeně vyplývají i korekce k Schrödingerovu modelu, mající původ v relativistické změně hmotnosti a v interakci spinů elektronů (přesněji jejich magnetických polí) ve víceelektronových atomových obalech. Podobně Kleinova–Gordonova rovnice popisuje vlastnosti exotických mezoatomů, jejichž atomový obal je tvořený mezony (zpravidla záporné piony).
Složení atomu[editovat | editovat zdroj]
Přestože podle jména je atom „nedělitelný“, ve skutečnosti jej lze rozložit na menší složky, někdy označované jako subatomární částice:
- elektrony jsou záporně nabité částice, které se nacházejí v atomovém obalu, ze kterého je lze relativně snadno vyjmout a vytvořit tím nabitý iont (viz ionizace);
- ve středu atomu je atomové jádro obsahující tzv. nukleony (jádro zabírá jen nepatrnou část atomu, ale tvoří naprostou většinu jeho hmotnosti):
Elektrony jsou k atomovému jádru vázány elektromagnetickou silou zprostředkovávanou fotony. Protony a neutrony v jádře jsou navzájem vázány jadernou silou zprostředkovanou gluony.
Samotné protony a neutrony se ještě skládají z kvarků.
Druhy atomů[editovat | editovat zdroj]
Různé atomy se liší svým složením: počtem jednotlivých částic. Atomy různých prvků se liší svým atomovým číslem, které vyjadřuje počet protonů v jádře (např. atom se šesti protony je atomem uhlíku; počet elektronů v obalu je u běžného elektricky neutrálního atomu shodný s počtem protonů v jádře). Atomy jednoho prvku se mohou lišit počtem neutronů v jádře (tzv. nukleonovým číslem), čímž tvoří různé izotopy (např. atom s šesti protony a osmi neutrony je izotop uhlík 14, 14C). Pokud se z elektricky neutrálního atomu vyjme elektron (nebo se naopak do něj vloží), vznikne nabitý iont.
Je známo asi 256 druhů atomů (nuklidů), které jsou stabilní, a mnoho dalších, jejichž jádra jsou nestabilní a samovolně se radioaktivně rozpadají.
Exotické druhy[editovat | editovat zdroj]
V atomovém jádře může být nukleon nahrazen hyperonem, zpravidla hyperonem Λ. Jedná se pak o atom s hyperjádrem.
Elektron v atomovém obalu může být nahrazen mionem (nebo lehčím záporně nabitým mezonem, např. pionem[3]). Takový atom se pak nazývá mioatomem (resp. mezoatomem). Vzhledem k větší hmotnosti je klasický Bohrův poloměr mioatomu mnohem menší, mion je vázán těsněji a je vysoká pravděpodobnost záchytu mionu jádrem (obdoba záchytu elektronu u radioaktivní přeměny beta). Atomové orbitaly mezoatomů se liší nejen kvůli odlišné hmotnosti, ale také tím, že k popisu kvantověmechanického chování mezonu v obalu je nutno použít Kleinovu–Gordonovu rovnici (na rozdíl od Diracovy rovnice pro elektron). Také jádro (proton u atomu lehkého vodíku) může být také nahrazeno antimionem nebo kladně nabitým mezonem – v r. 2016 tak např. byla prokázána existence exotických atomů složených z pionu a kaonu (jak K+π− tak π+K−).[4]
Někdy bývá za exotický atom považováno i tzv. pozitronium, vázaná soustava pozitronu a elektronu, a mionium, název nesystematicky používaný jak pro soustavu antimionu a elektronu, tak antimionu a mionu. Ve všech těchto případech kladně nabitý antilepton nahrazuje klasické atomové jádro.
Mohou existovat i vázané soustavy atomového jádra a antiprotonu, nahrazujícího elektron v obalu. Takové soustavy se nazývají baryonové atomy. V r. 1991 bylo objeveno antiprotonové hélium (atomové jádro hélia s „obalem“ tvořeným antiprotonem a elektronem), v r. 2006 pak byla prokázána produkce protonia čili antiprotonového vodíku, vázané soustavy protonu a antiprotonu.[5] V případě antiprotonového hélia, jakéhosi hybridu mezi atomem a molekulou, se používá též název atomkule. Za relativní stabilitu dvou jeho konfigurací může koordinace kvantového chování antiprotonu a elektronu v jeho obalu.[6]
Všechny exotické atomy jsou nestabilní.
Atomy a molekuly[editovat | editovat zdroj]
V plynech, kapalinách a některých pevných látkách jsou atomy chemickými vazbami vázány do molekul. V jiných pevných látkách jsou atomy vázány přímo bez tvorby molekul. Tak vznikají krystalické látky; zvláštním případem jsou molekulární krystaly.
Silové působení v atomu[editovat | editovat zdroj]
Protože je atom složen z částic, je pro jeho stabilitu důležitá vyváženost sil, které v něm působí:[7]
- Gravitační síla působící mezi všemi formami hmoty je v atomech zanedbatelná. Je to nejen z důvodu, že subatomární částice mají velkou hybnost, ale především proto, že gravitace je ze všech interakcí nejslabší. Například mezi protonem a elektronem vzdáleným 10−10m (poloměr atomu) působí gravitační síla 10−47N, zatímco síla mezi dvěma protony (či neutrony) vzdálenými 10−15m (poloměr jádra atomu) působí gravitační síla 10−34N.
- Elektromagnetická síla je síla nekonečného dosahu, která působí pouze na částice s elektrickým nábojem. V běžném atomu to jsou elektron a proton, zatímco neutron je elektricky neutrální. Přitažlivá elektromagnetická síla mezi záporně nabitým elektronem a kladně nabitým protonem je tedy síla, která drží elektrony v elektronovém obalu a brání jim, aby atom opustily a to silou řádu 10−8N. Na druhou stranu mezi samotnými protony působí odpudivá elektromagnetická síla, a to v řádu 100 N.
- Silná jaderná síla je přitažlivá síla, která působí mezi všemi kvarky a gluony až do vzdálenosti 10−15m. V atomu jsou z kvarků složeny proton a neutron. Silná síla je tedy zodpovědná za to, že protony a neutrony drží pohromadě a vytváří atomové jádro a především, že drží pohromadě protony, které se vzájemně elektricky odpuzují.
- Slabá jaderná síla je síla působící mezi všemi fermiony až do vzdálenosti 10−18m. V běžném atomu jsou všechny částice fermiony, protože mají spin 1/2.
Z toho vyplývá, že za interakce v atomovém obalu (elektrony v poli jádra, elektrony navzájem, přechody mezi energetickými stavy) je zodpovědná elektromagnetická interakce.
V atomovém jádře se významně projevuje silná interakce (drží jádro pohromadě, je zodpovědná za radioaktivní přeměnu alfa), ale i slabá interakce (zodpovědná za radioaktivní přeměnu beta) a elektromagnetická interakce (snižuje vazbovou energii jádra, zodpovědná za přechody mezi energetickými stavy jádra – radioaktivitu gama).
Výzkum atomů[editovat | editovat zdroj]
Nemožnost vizualizace atomů viditelným světlem[editovat | editovat zdroj]
Vizualizaci makroskopických objektů lze bezproblémově provést opticky, tedy pomocí viditelného světla. Tehdy lze proces vizualizace popsat následovně: Světlo putuje ze zdroje záření na objekt od nějž se odrazí (nebo je světlo pohlceno a následně vyzářeno) a pokračuje do měřícího přístroje, např. mikroskopu. Makroskopické objekty jsou díky své hmotnosti ovlivněny světelným tokem pouze nepatrně a vliv měření se zpravidla zanedbává.
Problém nastává u mikroskopických objektů, jako jsou atomy, kde vliv měření zanedbat nelze. Maximální přesnost měření je dána principem neurčitosti, . Vyplývá z něj, že polohu atomu nemůžeme změřit naprosto přesně, takže obraz bude vždy rozostřen a toto omezení nelze nijak obejít. Dále z něj vyplývá, že čím menší rozostření chceme, tím větší hybnost světlo musí mít. Protože ale hovoříme o rozostření menším než velikost atomu, tedy v řádu , tak hybnost fotonů musí být v řádu , neboli minimální frekvence použitelného světla je . Nejvyšší frekvence viditelného světla je ale řádu a tedy viditelným světlem není možné atomy pozorovat. Zpětný výpočet ukazuje, že viditelným světlem je možné pozorovat pouze objekty, které jsou alespoň 10000krát větší než je atom. Toto omezení je platné pro všechny optické mikroskopy bez ohledu na jejich konstrukci.
Zařízení pro vizualizaci atomů[editovat | editovat zdroj]
Aby se daly atomy vizualizovat, je nutné místo viditelného světla použít něco jiného nebo použít úplně jiný způsob vizualizace. Mezi základní zařízení pro vizualizaci atomů patří:
- Elektronový mikroskop – Namísto viditelného světla (fotonů) používá elektrony a namísto optických čoček používá elektromagnetické čočky. Použití elektronů umožňuje kvantová mechanika, podle níž mají všechny částice, a tedy i elektron, vlnovou povahu (korpuskulárně-vlnový dualismus). Výhoda elektronového mikroskopu je jeho mnohostrannost.
- Řádkovací tunelový mikroskop – Pro zobrazení povrchu využívá tunelový jev. Ostrý hrot se pohybuje těsně nad povrchem zkoumaného vzorku. Tunelový jev umožňuje přechod proudu (elektronů) z povrchu na hrot i když se hrot povrchu „nedotýká“. Mikroskop v dané poloze hrotu z velikosti procházejícího proudu určí vzdálenost mezi hrotem a povrchem a tedy výšku povrchu (z-ovou souřadnici). Na základě zmapování vzdáleností hrotu a povrchu v mnoha bodech roviny v níž se hrot pohybuje, vytvoří mikroskop obraz reliéfu zkoumaného povrchu. Nevýhodou tunelovacího mikroskopu je, že se dá použít pouze pro vizualizaci vodivých povrchů.
- AFM mikroskop – Pro zobrazení povrchu využívá atomárních sil atomů povrchu zkoumaného vzorku. Ostrý hrot připevněný na ohebném nosníku se pohybuje po povrchu vzorku. Atomární síly povrchových atomů působí na hrot a ohýbají nosník. Mikroskop sledováním ohybu nosníku v dané poloze určí polohu hrotu a tedy i výšku povrchu. K vizualizaci reliéfu celého povrchu je potřeba hrotem zmapovat celý povrch. Výhoda AFM je, že se dá použít i pro vizualizaci nevodivých povrchů.
Manipulace s atomy[editovat | editovat zdroj]
S jednotlivými atomy se poprvé podařilo manipulovat v roce 1989 Donaldu Eiglerovi z IBM, který ze 35 atomů xenonu vytvořil nápis „IBM“. Pro manipulaci s atomy použil řádkovací tunelový mikroskop při velmi nízkých teplotách a v ultravysokém vakuu.
Manipulace s jednotlivými atomy je velmi důležitá pro budoucí rozvoj nanotechnologie, oboru, který na úrovni atomů a molekul pomáhá vytvářet materiály speciálních vlastností, např. materiály s vysokou pevností.
Reference[editovat | editovat zdroj]
- ↑ http://www.osel.cz/10700-demokritos-jen-atomy-a-prazdno.html - Démokritos: Jen atomy a prázdno
- ↑ E. Rutherford, The Scattering of and Particles by Matter and the Structure of the Atom, Philos. Mag, 6 (1911) 21, PDF
- ↑ HOUSER, Pavel. Na okamžik připravili heliový atom s pionem namísto elektronu. SCIENCEmag.cz [online]. 2020-05-08. Dostupné online.
- ↑ ADEVA, B., et al. (DIRAC Collaboration). Observation of π−K+ and π+K− Atoms. Physical Review Letters [online]. 8. září 2016. Svazek 117, čís. 11: 112001. Dostupné online. ISSN 1079-7114. DOI 10.1103/PhysRevLett.117.112001. (anglicky)
- ↑ Spojení světa a antisvěta
- ↑ HOUSER, Pavel. Kouzla s antihmotou: Atomy helia, ale s antiprotonem. SCIENCEmag.cz [online]. Nitemedia s.r.o., 19. březen 2020. Dostupné online.
- ↑ D. McMahon, Quantum Field Theory Demystified, McGraw-Hill (2008) 12-32
Literatura[editovat | editovat zdroj]
- Dr. Heinrich Remy, Anorganická chemie 1. díl, 1. vydání 1961
- N. N. Greenwood – A. Earnshaw, Chemie prvků 1. díl, 1. vydání 1993 ISBN 80-85427-38-9
Související články[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu atom na Wikimedia Commons
Obrázky, zvuky či videa k tématu atom na Wikimedia Commons  Galerie atom na Wikimedia Commons
Galerie atom na Wikimedia Commons Slovníkové heslo atom ve Wikislovníku
Slovníkové heslo atom ve Wikislovníku Encyklopedické heslo Atom v Ottově slovníku naučném ve Wikizdrojích
Encyklopedické heslo Atom v Ottově slovníku naučném ve Wikizdrojích







![{\displaystyle [x,y,0]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/aac9f203121210a544e830db040947b07934df2a)
![{\displaystyle [x,y]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/1b7bd6292c6023626c6358bfd3943a031b27d663)

