Rutherfordův model atomu
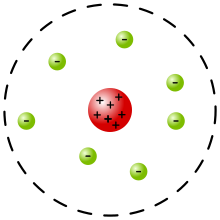
Rutherfordův model atomu (též planetární model atomu) je model atomu, který navrhl Ernest Rutherford v roce 1911 na základě analýzy experimentů Geigera a Marsdena.[1] V tomto modelu je atom složen z velmi malého hmotného jádra, kolem nějž obíhají elektrony ve vzdálenosti cca 10000krát větší než je poloměr jádra atomu.
Experiment[editovat | editovat zdroj]
V letech 1909–1910 prováděli Hans Geiger a Ernest Marsden rozptylové experimenty částic alfa a beta.[2] Mimo jiné ozařovali alfa částicemi zlatou a platinovou fólii, jejichž tloušťka byla v řádu 10−6 metrů (cca 10000 atomových vrstev). V těchto experimentech zjistili, že většina alfa částic není atomy fólie příliš ovlivněna a že střední odchylka od původního směru pohybu alfa částic způsobená fólií je přibližně 1°. Nicméně si Geiger a Marsden všimli, že určité množství alfa částic (cca 1 z 20000 pro zlatou fólii) neprošlo fólií a byly rozptýleny o úhel větší než 90°. Tento poznatek byl rozhodující pro pozdější Rutherfordovu interpretaci experimentu a vytvoření planetárního modelu atomu.
Analýza experimentu[editovat | editovat zdroj]
Rutherfordův rozptyl[editovat | editovat zdroj]
Rutherford předpokládal, že alfa částice mající náboj +2e interagují s atomy fólie pouze elektricky, tedy v souladu s Coulombovým zákonem. Na základě tohoto předpokladu odvodil vzorec, který z celkového počtu nalétávajících alfa částic určí počet alfa částic, které atom fólie odchýlí o úhel . Dnes se používá spíše diferenciální tvar tohoto vzorce[3] a určuje veličinu, která se nazývá diferenciální srážkový průřez Rutherfordova rozptylu
kde je coulombovský potenciál, je hmotnost nalétávající částice alfa, je hybnost částice alfa, je úhel rozptylu a je prostorový úhel.
Koincidence úspěchu[editovat | editovat zdroj]
K objevení malého hmotného atomového jádra a správné interpretaci rozptylových experimentů, přispěly mimo jiné následující skutečnosti:[4]
- Rutherford předpokládal, že Coulombův zákon, který byl ověřen pro vzdálenosti větší než 10−3 m, je platný i v případě atomárních vzdáleností.
- Účinný průřez elektricky nabitých částic odvozený v rámci kvantové mechaniky dává stejný vzorec jako Rutherfordův vzorec odvozený v rámci klasické fyziky.
Kdyby některá z těchto skutečností neplatila, pak by interpretace Geigerových a Marsdenových experimentů byla významně obtížnější.
Nevýhody modelu[editovat | editovat zdroj]
Hlavním problémem Rutherfordova modelu je stabilita atomu. Pokud by se elektrony pohybovaly kolem hmotného jádra, podobně jako planety kolem centra soustavy, pak by byly dostředivě urychlovány a podle klasické elektromagnetické teorie by měly vyzařovat energii ve formě elektromagnetických vln. Vyzařování by mělo snižovat energii elektronu a tedy by se elektron měl postupně přibližovat k jádru atomu až by měl na jádro spadnout. V případě atomu vodíku by stačilo pouhých 10−16 sekundy,[5] aby elektron na jádro spadl. Z experimentu ale vyplývá, že atomy vodíku jsou stabilní. Tento problém vyřešil až Bohrův model atomu.
Reference[editovat | editovat zdroj]
- ↑ E. Rutherford, The Scattering of and Particles by Matter and the Structure of the Atom, Philos. Mag, 6 (1911) 21, http://mrmackenzie.co.uk/podpress_trac/feed/3110/0/Rutherford-paper.pdf
- ↑ H. Geiger, E. Marsden, Proc. Roy. Soc., 82 (1909) 495; http://plato.if.usp.br/~fnc0404d/Geiger-1909.pdf[nedostupný zdroj]; H. Geiger, Proc. Roy. Soc. 83 (1910) 492.
- ↑ I. Štoll, Mechanika, skriptum FJFI, Vydavatelství ČVUT, Praha (1998) 148-152; I. Štoll, Teoretická fyzika, skriptum FJFI, Vydavatelství ČVUT, Praha (1999) 64-72; J. Žáček, Úvod do fyziky elementárních částic, Nakladatelství Karolinum, Praha (2005) 16
- ↑ J. Kvasnica, A. Havránek, P. Lukáč, B. Sprušil, Mechanika, Academia, Praha (2004) 175-177
- ↑ A. Beiser, Úvod do moderní fyziky, Academia, Praha (1978) 131-132
Související články[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Rutherfordův model atomu na Wikimedia Commons
Obrázky, zvuky či videa k tématu Rutherfordův model atomu na Wikimedia Commons








