Lanthan
| Lanthan | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ↓ Periodická tabulka ↓ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Obecné | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
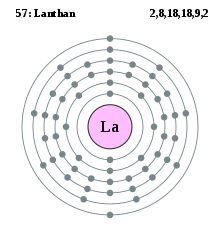
| Název, značka, číslo | Lanthan, La, 57 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cizojazyčné názvy | lat. Lanthanum | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupina, perioda, blok | 3. skupina, 6. perioda, blok d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chemická skupina | Lanthanoidy | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vzhled | stříbřitě lesklý | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identifikace | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Registrační číslo CAS | 7439-91-0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomové vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Relativní atomová hmotnost | 138,905 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomový poloměr | empiricky: 187 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalentní poloměr | 207±8 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronová konfigurace | [Xe] 5d1 6s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxidační čísla | 0[1], +1, +2, +3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronegativita (Paulingova stupnice) | 1,1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionizační energie | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| První | 538,1 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Druhá | 1067 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Třetí | 1850,3 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Látkové vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Krystalická struktura | dvojitě hexagonální těsně uspořádaná | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mechanické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hustota | 6,17 g/cm³ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenství | Pevné | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tvrdost | 2,5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rychlost zvuku | 2475 m/s | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tepelná vodivost | 13,4 W/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Součinitel délkové roztažnosti | 12,1 µm/(m·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termodynamické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota tání | 920 °C (1 193,15 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplota varu | 3 470 °C (3 743,15 K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenské teplo tání | 6,20 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Skupenské teplo varu | 400 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molární tepelná kapacita | 27,11 J/(mol·K) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektromagnetické vlastnosti | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Teplotní součinitel elektrického odporu | 615 nΩ·m | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Měrná magnetická susceptibilita | +118,0·10−6 cm3/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Bezpečnost | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| [2] Nebezpečí[2] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Izotopy | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Není-li uvedeno jinak, jsou použity jednotky SI a STP (25 °C, 100 kPa). | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Lanthan (chemická značka La, latinsky Lanthanum) je stříbřitě lesklý, přechodný kovový prvek, 1. člen skupiny lanthanoidů a 3. člen skupiny kovů vzácných zemin. Hlavní uplatnění nalézá v metalurgickém průmyslu při výrobě speciálních slitin anebo jejich deoxidaci a jako složka některých speciálních skel.
Základní fyzikálně-chemické vlastnosti[editovat | editovat zdroj]
Lanthan je stříbřitě bílý, měkký, velmi elektropozitivní přechodný kov. Je supravodičem 1. typu, a to za teplot pod 6,00 K.
Chemicky je lanthan značně reaktivním prvkem, ve skupině lanthanoidů patří mezi nejreaktivnější. Již za normální teploty reaguje se vzdušným kyslíkem za vzniku velmi stabilního oxidu lanthanitého. S vodou reaguje lanthan zvolna za vzniku plynného vodíku, snadno se rozpouští v běžných minerálních kyselinách. Za zvýšené teploty také přímo reaguje s běžnými nekovovými prvky jako jsou dusík, bor, fosfor, síra a halogeny.
Ve sloučeninách se vyskytuje pouze v mocenství La3+. Svými chemickými vlastnostmi se značně podobá hliníku. Oba prvky tvoří například vysoce stabilní oxidy, které nereagují s vodou a jen velmi obtížně se redukují. Ze solí anorganických kyselin jsou důležité především fluoridy a fosforečnany, jejich nerozpustnost ve vodě se používá k separaci lanthanoidů od jiných kovových iontů. Další nerozpustnou sloučeninou je šťavelan, který se dokonce používá ke gravimetrickému stanovení lanthanu.
Lanthan byl objeven v roce 1839 Carlem Mosanderem, v čisté podobě byl izolován až roku 1923.
Výskyt a výroba[editovat | editovat zdroj]
Lanthan je v zemské kůře obsažen v koncentraci asi 18–30 mg/kg. V mořské vodě je jeho koncentrace kolem 1,2×10−8 g/l. Ve vesmíru připadá jeden atom lanthanu na 100 miliard atomů vodíku.
V přírodě se lanthan vyskytuje pouze ve formě sloučenin. Neexistují však ani minerály, v nichž by se některé lanthanoidy (prvky vzácných zemin) vyskytovaly samostatně, ale vždy se jedná o minerály směsné, které obsahují prakticky všechny prvky této skupiny. Mezi nejznámější patří monazitové písky a xenotim, chemicky fosforečnany lanthanoidů, a dále bastnäsity – směsné flourouhličitany prvků vzácných zemin.
Velká ložiska těchto rud se nalézají ve Skandinávii, Spojených státech amerických, Číně a Vietnamu. Významným zdrojem jsou i fosfátové suroviny - apatity z poloostrova Kola v Rusku
Při průmyslové výrobě prvků vzácných zemin se jejich rudy nejprve louží směsí kyseliny sírové a chlorovodíkové a ze vzniklého roztoku solí se přídavkem hydroxidu sodného vysráží hydroxidy.
Separace jednotlivých prvků se provádí řadou různých postupů – kapalinovou extrakcí, za použití ionexových kolon nebo selektivním srážením nerozpustných komplexních solí.
Příprava čistého kovu se obvykle provádí redukcí solí kovovým vápníkem. Redukci fluoridu lanthanitého popisuje rovnice:
- 2 LaF3 + 3 Ca → 2 La + 3 CaF2
Použití a sloučeniny[editovat | editovat zdroj]
Vzhledem k vysokému zastoupení lanthanu v rudách vzácných zemin je tohoto prvku na trhu relativně nadbytek, protože vzniká částečně jako přebytek při výrobě vysoce žádaných lanthanoidů, především europia nebo samaria.
Základním průmyslové využití nalézá lanthan v metalurgii. Jeho vysoká afinita ke kyslíku se uplatní při odkysličování roztavených kovů a malé přídavky lanthanu do různých slitin mají vliv na výsledné mechanické vlastnosti produktu. Například oceli nebo litina s obsahem malých množství lanthanu vykazují vyšší tvárnost a kujnost a mají vyšší mechanickou odolnost proti nárazu. Ve slitinách molybdenu snižuje přídavek lanthanu tvrdost a zvyšuje odolnost proti náhlým teplotním změnám.
Významné uplatnění nalézají sloučeniny lanthanu, především oxid lanthanitý La2O3, ve sklářském průmyslu. Sklo s obsahem malých množství této sloučeniny získává vysoký index lomu a vykazuje nízký světelný rozptyl – používá se proto často pro výrobu optických čoček v objektivech fotoaparátů nebo dalekohledech. Sklo s obsahem lanthanu pohlcuje infračervené záření a vyrábí se z něj optické filtry, propouštějící pouze viditelné světlo.
Katalyzátory s obsahem lanthanu se používají i v petrochemii při krakování ropy.
Brusné a lešticí práškové materiály, používané při výrobě optických součástek (přesné čočky, zrcadla do dalekohledů, …) obsahují často významný podíl sloučenin lanthanu.
Přídavek lanthanitých iontů do analyzovaných roztoků působí jako spektrální iontový pufr a především v atomové absorpční spektrometrii slouží k potlačení nežádoucích interferencí, vznikajících přítomností vysokých množství solí.
Odkazy[editovat | editovat zdroj]
Reference[editovat | editovat zdroj]
- ↑ CLOKE, F; GEOFFREY, N. Zero oxidation state compounds of scandium, yttrium, and the lanthanides. Chemical Society Reviews. 1993, roč. 22, čís. 1, s. 17. Dostupné online. ISSN 1460-4744. DOI 10.1039/CS9932200017.
- ↑ a b Lanthanum. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
Literatura[editovat | editovat zdroj]
- Cotton F.A., Wilkinson J.:Anorganická chemie, souborné zpracování pro pokročilé, ACADEMIA, Praha 1973
- Holzbecher Z.:Analytická chemie, SNTL, Praha 1974
- Dr. Heinrich Remy, Anorganická chemie 1. díl, 1. vydání 1961
- N. N. Greenwood – A. Earnshaw, Chemie prvků 1. díl, 1. vydání 1993 ISBN 80-85427-38-9
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu lanthan na Wikimedia Commons
Obrázky, zvuky či videa k tématu lanthan na Wikimedia Commons  Slovníkové heslo lanthan ve Wikislovníku
Slovníkové heslo lanthan ve Wikislovníku

