DNA

Deoxyribonukleová kyselina, běžně označovaná DNA (z anglického deoxyribonucleic acid, česky zřídka i DNK), je nukleová kyselina, nositelka genetické informace všech organismů s výjimkou některých nebuněčných, u nichž hraje tuto úlohu RNA (např. RNA viry). DNA je tedy pro život velmi důležitou látkou, která ve své struktuře kóduje a buňkám zadává jejich program, a tím předurčuje vývoj a vlastnosti celého organismu. U eukaryotických organismů (jako jsou např. rostliny a živočichové) je DNA hlavní složkou chromatinu, směsi nukleových kyselin a proteinů, a je uložena zejména uvnitř buněčného jádra, zatímco u prokaryot (jako jsou např. bakterie a archea) se DNA nachází volně v cytoplazmě.
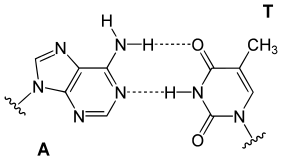
DNA je biologická makromolekula – polymer v podobě řetězce nukleotidů. Nukleotidy jsou vždy složeny z cukru deoxyribózy, fosfátové skupiny a jedné ze čtyř nukleových bází. Informační funkci mají právě báze, jimiž může být adenin A, guanin G, cytosin C nebo thymin T. První dvě patří mezi puriny, zbylé mezi tzv. pyrimidiny. Dvě vlákna DNA se často spojují a vytvářejí dvoušroubovici, jejíž tvar je tak slavný, že se stal kulturní ikonou moderní doby.[1] Dvoušroubovici DNA tvoří dvě navzájem spletené šroubovice, každá mířící opačným směrem (jsou antiparalelní). Mezi protilehlými bázemi obou vláken se vytvářejí vodíkové můstky, a to tři mezi guaninem a cytosinem nebo dva mezi adeninem a thyminem. Existují i jiné způsoby uspořádání řetězců, vymykající se tradiční představě dvoušroubovice.
Deoxyribonukleová kyselina je středem zájmu vědců nejen z biologických oborů a byly vyvinuty promyšlené techniky její izolace, separace, barvení, sekvenování, umělé syntézy a manipulace s ní pomocí metod genového inženýrství. Všechny tyto postupy jsou důležité i pro lékaře, kriminalisty či evoluční biology – DNA je zásadním materiálem v diagnostice nemocí, testech otcovství, při vyšetřování zločinů, přípravě plodin s novými vlastnostmi či třeba hledání příbuzenských vztahů mezi organismy.
Historie výzkumu[editovat | editovat zdroj]

Deoxyribonukleová kyselina byla popsána roku 1869, kdy švýcarský lékař Friedrich Miescher zkoumal složení hnisu z nemocničních obvazů. Z jader bílých krvinek přítomných v tomto hnisu získal jisté množství nukleových kyselin, které souhrnně nazýval nuklein.[2] Na počátku 20. století Phoebus Levene rozpoznal, že DNA se skládá z cukrů, fosfátů a bází.[3]
O funkci DNA toho dlouho nebylo moc známo. První důkaz o roli DNA v přenosu genetické informace přinesl v roce 1944 Averyho-MacLeodův-McCartyho experiment, který provedli Oswald Avery společně s Colinem MacLeodem a Maclynem McCartym. Sérií pokusů s transformací pneumokoků zjistili, že DNA je genetickým materiálem buněk.[4] Další důkaz přinesl v roce 1952 Hersheyho–Chaseové experiment.
Patrně nejslavnějším milníkem ve výzkumu DNA bylo odhalení její trojrozměrné struktury. Správný dvoušroubovicový model poprvé představili v roce 1953 v časopise Nature James D. Watson a Francis Crick, pozdější laureáti Nobelovy ceny.[5] Vycházeli přitom z rentgenové difrakční analýzy, kterou o rok dříve provedli Rosalind Franklinová a Raymond Gosling a publikovali ve stejném čísle Nature. Další článek v tomto vydání předložil i Maurice Wilkins.[6] V roce 1957 předložil v té době již slavný Crick sérii pravidel, které se označují jako centrální dogma molekulární biologie a popisují vztahy mezi DNA, RNA a proteiny.[7] O rok později slavný Meselsonův–Stahlův experiment umožnil poznat způsob replikace DNA v buňkách.[8] Genetický kód rozluštili na počátku 60. let Har Gobind Khorana, Robert W. Holley a Marshall Warren Nirenberg.[9]
Původ[editovat | editovat zdroj]
Přítomnost nukleových kyselin, tedy DNA a RNA, je společnou vlastností všech známých pozemských organismů. Veškerý život je založen na koexistenci těchto nukleových kyselin s bílkovinami, nicméně není zcela jasné, jak se vztah mezi DNA a bílkovinami vyvinul. Podle některých hypotéz nejprve existovaly bílkoviny a až následně vznikly nukleové kyseliny, nicméně nejvíce příznivců má zřejmě v současnosti představa, že prapůvodní látkou byla nukleová kyselina, která byla schopna biologické evoluce. Podle teorie RNA světa však hlavní roli hrála nejprve spíše RNA a teprve posléze přejala hlavní roli DNA.[10] Doklady ve prospěch takových hypotéz jsou však vždy nepřímé, protože nejsou k dispozici dostatečně staré vzorky DNA. Život vznikl již před několika miliardami let, jenže už po několika desítkách tisíců let klesá množství DNA na setinu původního stavu. Studie v časopise Nature z let 2000 a 2002 nicméně popisují nález až 450 milionů let starých vzorků bakteriální DNA uchovaných v solných krystalech,[11][12] dále existuje i řada dalších, více nebo méně spolehlivých studií.
Stavba[editovat | editovat zdroj]
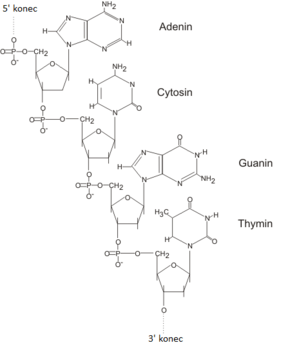
Stavbu DNA je možno zkoumat na několika úrovních. Pořadí nukleotidů v lineárním dvouvlákně je záležitostí tzv. primární struktury. Stáčení vlákna do dvoušroubovice se označuje jako sekundární struktura DNA. Konečně pod tzv. terciární strukturou se rozumí obvykle nadšroubovicové vinutí, které usnadňuje kondenzaci DNA.
Chemická struktura[editovat | editovat zdroj]
DNA vlastně není nic jiného než velmi dlouhý lineární řetězec nukleotidů. Například uvnitř každého virionu planých neštovic se nachází DNA o délce 193 mikrometrů, kruhová DNA u Escherichia coli má délku 1 600 µm (1,6 mm), lidský genom je rozložen do 23 lineárních molekul DNA (v haploidním stavu) o celkové délce 1 metru.[13] Nukleotid je základní stavební jednotkou všech molekul DNA; existují přitom čtyři základní typy nukleotidů, jež se v DNA přirozeně vyskytují. Tyto čtyři nukleotidy (dATP, dGTP, dCTP, dTTP) se navzájem liší typem přivěšené nukleové báze, jíž může být především adenin, guanin, cytosin či thymin.[pozn. 1] Důležité je, že každý nukleotid má tři důležité stavební součásti:
- deoxyribóza – pětiuhlíkový cukr (pentóza), který se v DNA vyskytuje v cyklické furanózové formě. Jeho uhlíky se po směru pohybu hodinových ručiček označují 1', 2', 3', 4' a 5', přičemž na 1' uhlíku je navěšena nukleová báze, na 3' a 5' uhlíku jsou přes OH skupinu připevněny fosfátové skupiny;
- fosfát – vazebný zbytek kyseliny ortofosforečné, který je navázán na 5' uhlíku každého nukleotidu. Záporný náboj na fosforečnanu je důvodem celkového negativního náboje DNA. Fosfátová skupina je můstek propojující 5' uhlík každé deoxyribózy s 3' uhlíkem předchozí deoxyribózy. Výsledkem je tzv. cukr-fosfátová kostra DNA.
- nukleová báze – dusíkatá heterocyklická sloučenina. V DNA se v různých kombinacích vyskytují především čtyři základní nukleové báze, dvě purinové (adenin
Aa guaninG) a dvě pyrimidinové (thyminTa cytosinC). Jedna z těchto čtyř nukleových bází je připojena na 1' uhlíku deoxyribózy pomocí N-glykosidové vazby. Právě existence čtyř nukleových bází je zásadní pro informační vlastnosti DNA. Důležitá je také schopnost nukleových bází vytvářet celou řadu vodíkových můstků.
Primární struktura DNA se dá znázornit jako lineární řada nukleotidů nebo třeba jako řada písmen, které odpovídají dusíkatým bázím v těchto nukleotidech. Dále je důležité, že DNA je směrovaná (direkcionalizovaná), tzn. dají se jednoznačně odlišit oba konce. Směr vláken se označuje právě podle orientace deoxyribózy v něm, tedy: směr 3'→5' a opačný směr 5'→3'. Podle konvence se pořadí nukleotidů zapisuje směrem 5'→3' (např. TACGGACGGG AGAAGCGCGC GGGCGGGCCG je prvních 30 z 3 675 nukleotidů tvořících přepisovanou část genu pro lidský alfa-tubulin[15]).
V roce 2011 se objevila zpráva o existenci bakterií GFAJ-1, která údajně ve své DNA obsahuje místo fosfátových skupin arseničnany.[16] Hypotéza byla definitivně vyvrácena v r. 2012.[17][18][19]
Uspořádání řetězců[editovat | editovat zdroj]
Deoxyribonukleová kyselina (DNA) může existovat jako samostatná jednovláknová molekula (tzv. ssDNA), nicméně velmi často vytváří vícevláknové struktury, které jsou složené z několika řetězců spojených vodíkovými můstky. Vodíkové můstky jsou jedním z typů poměrně slabých vazebných interakcí, mezi dvěma či více vlákny DNA jich však může vzniknout obrovské množství; výsledná vícevláknová struktura tak je poměrně stabilní. Typickou formou takového vícevláknového uspořádání DNA je dvoušroubovice, notoricky známá molekula DNA (připomínající „stočený žebřík“) tvořená dvěma lineárními řetězci. Aby vznikla pravidelná struktura s velkým množstvím vodíkových můstků, je žádoucí, aby se vedle sebe „v příčli žebříku“ vyskytovaly vždy určité nukleové báze, které spolu ve správném prostorovém uspořádání vytváří několik vodíkových můstků. V typickém případě (ne však vždy) se nukleové báze spojují navzájem s odpovídající bází podle jednoduchého klíče:
Ase páruje sT(vzájemně jsou spojeny dvěma vodíkovými vazbami)Gse páruje sC(vzájemně jsou spojeny třemi vodíkovými vazbami)
Jedná se o tzv. komplementaritu bází, z ní vychází vzájemná komplementarita obou vláken DNA. Vždy je na určité pozici v molekule jeden nukleotid z dvojice a v protějším vlákně druhý z nich. Takto se uchovává v každém z vláken tatáž informace, i když jedno z vláken je „negativem“ vlákna druhého – podle jednoho vlákna je možné přiřazením komplementárních bází vytvořit vlákno druhé. Poměr AT a GC párů v molekule DNA je velmi různý: tzv. obsah GC se pohybuje u bakterií od 25 do 75 %, u savců v rozmezí 39–46 %.[20]
Existuje celá řada dalších možností, jak pomocí vodíkových můstků spárovat báze, neboť atomů schopných podílet se na vzniku vodíkových vazeb je na molekulách purinů i pyrimidinů celá řada. Samostatnou kapitolou je tzv. hoogsteenovské párování pojmenované podle Karsta Hoogsteena, který je v 60. letech 20. století jako první popsal.[21] Jinou možností je tzv. wobble párování, které umožňuje úsporné rozeznávání kodonů pomocí tRNA molekul. Při wobble párování může například guanin vytvářet vazbu s uracilem; někdy je rekrutován inosin, jenž má velmi obecné vazebné schopnosti a je schopen vázat se na C, A a U.[22]
Kromě vodíkových můstků se uplatňuje hydrofobie.[23]
Dvoušroubovice[editovat | editovat zdroj]

V drtivém procentu případů se DNA za běžných podmínek uchovává ve formě pravotočivé dvoušroubovice. Dvoušroubovice DNA je tvořena dvěma vlákny DNA, které se obtáčí kolem společné osy a interagují spolu. Vlákna jsou tzv. antiparalelní, tzn. směřují opačnými směry[24] – zatímco jedno vlákno můžeme jedním směrem popsat jako 5'-3', druhé je ve stejném směru 3'-5'. Čísla 3' a 5' označují čísla uhlíku na deoxyribóze, na které se upínají fosfátové skupiny v cukr-fosfátové kostře DNA. Mezi bázemi v rámci jednoho „patra“ dvoušroubovice platí pravidla Watson-Crickovské komplementarity.
Existuje několik tzv. helikálních forem (konformací) DNA, které se liší celou řadou parametrů. Typická Watson-Crickovská pravotočivá dvoušroubovice (tzv. B-DNA) je nicméně zcela převažující a ostatní formy (zejména pravotočivá A-DNA a levotočivá Z-DNA) se sice mohou vyskytovat i v podmínkách živé buňky, nicméně spíše vzácně a jen za specifických okolností.[25][26][27]
Jiná uspořádání řetězců[editovat | editovat zdroj]

V obecném povědomí DNA tvoří dvoušroubovici, nicméně existují i jiné způsoby uspořádání. Některé se vyskytují i v buňkách (in vivo), jiné jsou spíše laboratorní záležitost. Mnohdy se využívá neobvyklých párovacích míst na molekulách bází. To je případ tzv. G-kvartetů, čtyřvláknových úseků DNA v telomerických oblastech chromozomů, v nichž do kruhu párují čtyři guaninové báze.[28] Co se týče trojšroubovice DNA,[29][30] možná dočasně vzniká při tzv. crossing-overu;[31] laboratorně může být trojvláknová struktura připravena např. z vláken poly(A) a polydeoxy(U).[32]
DNA se také může větvit a vznikají např. třívláknová či čtyřvláknová spojení. V některých případech dvoušroubovicová DNA na jednom svém konci lokálně denaturuje a na uvolněné konce se připojí třetí řetězec – v prostředí buňky by tato struktura mohla vznikat při crossing-overu, pokud nedošlo k replikaci v jednom z genomů.[33] Jindy takto vlastně denaturují dvě dvoušroubovice a vzájemně se komplementárně přiloží, čímž vzniká čtyřvláknové spojení. V případě crossing-overu se jedná o známý Hollidayův spoj, který umožňuje vlastní výměnu homologních vláken.[34] Při replikaci DNA či při opravě DNA mohou větvení vznikat také. V laboratoři nicméně vznikají ještě mnohem fantastičtější prostorové struktury DNA – byly vyrobeny např. krychle či osmistěn složené celé pouze z DNA molekul. Tyto a další syntetické struktury DNA jsou v centru zájmu DNA nanotechnologů.[1]
Vyšší úrovně struktury[editovat | editovat zdroj]
Genom, tedy souhrn DNA v buňce, není pouhou změtí dvoušroubovicové DNA – na vyšších úrovních je možné pozorovat komplikované vinutí a četné interakce s buněčnými bílkovinami. Tyto struktury také nesou genetickou informaci.[35] Zcela typické je tzv. nadšroubovicové vinutí (supercoiling), tedy dodatečné šroubovicové vinutí již existující dvoušroubovice.[36] Nadšroubovicové vinutí se dá zjednodušeně představit tak, že držíme v každé ruce jeden z obou konců provázku a postupně na jednom konci provázek kroutíme. Vzniklé napětí se opět uvolní (relaxuje) jen tehdy, pokud uvolníme jednu ruku. Dvoušroubovice je však stočená již ve svém relaxovaném stavu (jedna otáčka každých cca 10 párů bází), a tak můžeme rozlišit, zda se nadšroubovice vine stejným směrem, jako dvoušroubovice (tzv. pozitivní supercoiling), nebo směrem opačným (negativní supercoiling, uvolňuje DNA). Nadšroubovicové vinutí má celou řadu důležitých funkcí a regulačních rolí;[37] v žádném případě se nejedná pouze o anomálii ve struktuře.
DNA se v buňce dále organizuje do mikroskopicky pozorovatelných útvarů známých jako chromozomy. U bakterií je zřejmě systém kondenzace DNA do (obvykle jediného) chromozomu poněkud méně propracovaný a např. u Escherichia coli zahrnuje několik proteinů, které jsou schopné udržovat nadšroubovicové vinutí a vytvářet ostré ohyby vlákna DNA.[38] Eukaryotické organismy, jako je třeba člověk, mají velmi komplikovaně sbalenou DNA. Souvisí to s délkou jejich DNA – např. lidský genom má na délku dva metry, přitom buněčné jádro má na délku několik mikrometrů. Dvouvlákno DNA se nejprve nabaluje na bazické proteiny známé jako histony; DNA nabalená na osm histonů vytváří tzv. „nukleozom“, a tak na této úrovni DNA vypadá jako řada korálků (nukleozomů) na provázku (DNA). Tyto korálky se však obvykle ještě stáčí do 30 nanometrů tlusté šroubovice.[39] Na vzniku chromozomů se podílí ještě vyšší úrovně sbalení DNA, které jsou však méně prostudované a vznikají jen v určitých fázích buněčného cyklu.

Vlastnosti[editovat | editovat zdroj]

DNA je polymerní sloučeninou s vysokou molární hmotností. Molární hmotnost závisí na délce DNA a zhruba platí, že s každým nukleotidem stoupá molární hmotnost o 330 g/mol, v případě dvouvláknové DNA na jeden pár bází připadá asi 650 g/mol.[40] Deoxyribonukleová kyselina je záporně nabitá (díky fosforečnanovým skupinám), a je tedy polárního charakteru. Díky tomu je rozpustná ve vodě, naopak v ethanolu se sráží (neboť dochází k vyvázání záporných nábojů).[41] Po vysrážení má DNA bílou barvu.[42][nedostupný zdroj] Izolovaná DNA zaujímá dvoušroubovicové uspořádání, to je však možné rozrušit v procesu denaturace. Typicky se denaturace provádí zvýšením teploty, ale denaturaci způsobuje i nízká iontová síla roztoku nebo silně zásadité prostředí. Naopak kyselé prostředí není vhodné, protože dochází k hydrolýze glykosidových vazeb mezi cukrem a bází.[43] DNA absorbuje v UV oblasti s absorpčním maximem při vlnové délce 260 nm. Při denaturaci DNA se absorbance v této oblasti zvyšuje – tomuto jevu se říká hyperchromní efekt.[44] Je to dáno tím, že na absorpci se v největší míře podílejí báze DNA, které jsou v dsDNA „schované“ uvnitř dvoušroubovice. Po denaturaci dochází k „obnažení“ bází, které tak mohou lépe absorbovat UV záření.
Poločas rozpadu DNA činí dle studia kosterních nálezů asi 521 let.[45] DNA je považována za stabilní molekulu, což vynikne zejména při srovnání s RNA jakožto druhou významnou nukleovou kyselinou. V molekule DNA není na 2' uhlíku OH skupina – u RNA tam tato reaktivní skupina je a způsobuje nižší stabilitu RNA.[46] DNA se v laboratoři dlouhodobě skladuje při −20° nebo −70 °C, kde vydrží i několik let. Při teplotě 4 °C v TE pufru vydrží několik týdnů.[47] Existuje mnoho různých metod k uchování DNA na delší čas (zmrazení vzorků tekutým dusíkem, FTA karty, plastové mikrozkumavky, uchování pomocí chitosanu[48]). Uvnitř těl živých organismů však DNA musí snášet i poměrně vysoké teploty, a přesto vydrží. Krajním případem jsou hypertermofilní organismy, které žijí i při teplotách kolem 100 °C. Jejich DNA čelí jak riziku denaturace, tak i termodegradaci (rozpadu pevných chemických vazeb). Přesto žijí a mimo opravných mechanismů k tomu zřejmě přispívá i nadšroubovicové vinutí a také optimální iontové složení cytoplazmy.[49]
Pro DNA jsou však dále typické i některé vlastnosti, které ji do jisté míry odlišují od běžných chemických látek. V buňce je například možné replikovat DNA, tedy vytvářet její kopie. Víceméně každé buněčné dělení vyžaduje zmnožení genetické informace, aby jí v každé buňce bylo stále konstantní množství. V průběhu procesu se oddělí řetězce mateřské DNA a oba slouží jako návod (tzv. „templát“) pro tvorbu druhých vláken v rámci obou nově vznikajících dvoušroubovic. Ty jsou následně napůl tvořeny původní DNA a napůl nově dosyntetizované – celý proces je semikonzervativní. K dalším zajímavým vlastnostem DNA v buňkách patří možnost opravovat DNA, což ještě dále vylepšuje (už tak poměrně precizní) přenos genetické informace.[50] Bylo by možno najít množství dalších pozoruhodných vlastností DNA, vesměs probíhajících v buňce za pomoci speciálních enzymů.
Funkce[editovat | editovat zdroj]
DNA je nositelkou genetické informace všech živých organismů v pravém slova smyslu, ale i mnoha virů. V DNA je zapsána sekvence všech bílkovin a přeneseně je genetickou informací podmíněna existence všech biomolekul a buněčných struktur (k jejichž tvorbě jsou potřeba bílkoviny).[51] Schopnost ukládat a přenášet genetickou informaci je jednou z fundamentálních vlastností života.[51] Bez DNA buňky vydrží žít jen omezenou dobu; například lidské červené krvinky při svém zrání vyvrhují jádro, a protože pak nejsou schopné vyrábět nové bílkoviny a udržovat buňku, jsou po několika měsících poškozeny a musí se z oběhu odstraňovat.[52] Některé viry jsou sice schopné uchovávat svůj genetický materiál v podobě RNA (tzv. RNA viry), jenže RNA genomy nepodléhají opravným mechanismům a rychle mutují, a proto mají limitovanou velikost.[53] Život, tak jak ho známe, je proto závislý na DNA.
Konkrétní uložení DNA v buňce závisí na příslušnosti organismu k jedné z dvou základních skupin organismů. Bakterie a archea (souhrnně „prokaryota“) mají DNA obvykle uloženu volně v cytoplazmě. Obvykle vzniká pouze jistá jaderná oblast, tzv. nukleoid. Mimo to řada bakterií vlastní i malé kruhové molekuly DNA, tzv. plazmidy, které umožňují mimo jiné horizontální výměnu genetické informace. Zbylé organismy, tedy např. člověk, ale i rostliny, živočichové či prvoci, mají DNA uloženu především v buněčném jádře. Dále však se DNA nachází v některých eukaryotických organelách, jmenovitě v mitochondriích a v plastidech, pokud je buňka vlastní (jev zvaný mimojaderná dědičnost).
Informace nesená sekvencí nukleotidů v DNA se označuje jako genetická informace. Na každé nukleotidové pozici se nachází jedna ze čtyř bází (A, C, G či T), což znamená, že sekvence o délce n může nabývat 4n stavů.[54] Pro DNA dlouhou pouhých 10 nukleotidů existuje tedy teoreticky 410 = 1 048 576 kombinací. Lidský genom (souhrn lidské jaderné DNA) přitom obsahuje 3,1 miliardy (párů) bází.[55] Nejvyšší informační hodnota se přitom v genomu objevuje v místech, kde sídlí tzv. geny, která zaznamenávají informaci pro tvorbu RNA a potažmo i všech bílkovin. Informace pro tvorbu bílkovin je zašifrována pomocí třípísmenného kódu známého jako genetický kód. Každé trojici bází v DNA totiž u protein-kódujících genů odpovídá určitá aminokyselina. Aminokyseliny jsou základní stavební kameny bílkovin, takže je vlastně genetická informace jakýmsi návodem na výrobu bílkovin. Genetická informace je uplatňována podle tzv. centrálního dogmatu molekulární biologie. DNA je nejprve přepisována v RNA (obvykle tzv. messenger RNA), načež je tato RNA použita jako vzor pro tvorbu bílkovin. První zmíněný krok se jmenuje transkripce, druhý translace.
Velká část genomu mnoha organismů však není součástí žádného genu a dokonce se ani nepřepisuje v RNA. Role této tzv. nekódující DNA je v mnoha případech neznámá; někdy však pomáhá regulovat spouštění a vypínání okolních genů.[56] Velká část nekódující DNA dle současné úrovně znalostí nemá žádnou konkrétní funkci a označuje se prostě jako junk (odpadní) DNA.[57] Část této odpadní DNA však podle výsledků projektu ENCODE ve skutečnosti kóduje různé krátké regulační RNA; celkem se odhaduje, že 10–20 % genomu má díky těmto RNA významnou regulační funkci. V těsném okolí těchto regulačních sekvencí se tak podle ENCODE celkem nachází až 95 % lidského genomu.[58][59]
Práce s DNA[editovat | editovat zdroj]
Izolace a separace[editovat | editovat zdroj]

V celé řadě případů je žádoucí izolovat z buněk či z virových partikulí jejich DNA. Existuje samozřejmě celá řada metod extrakce DNA, nicméně u všech je nutné získat dostatečné množství biologického materiálu, uvolnit DNA a oddělit ji z nadmolekulárních struktur, načež je nutné vzorek přečistit a případně zahustit.[60] Důležitým krokem je uvolnění DNA z buněk, které se u živočišných buněk provádí pomocí detergentů (povrchově aktivních čisticích látek), jež rozrušují membrány. U buněk s buněčnou stěnou je to komplikovanější a je nutné nasadit třeba lysozymy (na bakteriální buněčnou stěnu) či mechanickou degradaci. Co se týče přečišťování buněčných extraktů, obvykle je nutné se zbavit bílkovin, které představují hlavní kontaminaci vzorků. Je možné použít proteázy, ale mnohdy se proteiny sráží fenolem a chloroformem, zatímco nukleové kyseliny zůstanou v roztoku a je možné je pak vysrážet třeba ethanolem.[61]
Po izolaci DNA následuje často separace (oddělení) požadovaných druhů molekul. Může být žádoucí oddělení třeba plazmidů od genomové DNA bakterií, což se dělá poměrně jednoduše centrifugací při vhodně nastavených parametrech, obvykle pomocí denaturace a následné renaturace.[61] Pro jemnější rozdělování podle velikosti i podle topologie DNA se často používá elektroforéza na agarózovém (či v případě velmi malých molekul na polyakrylamidovém) gelu. V případě extrémně velkých fragmentů DNA se užívá tzv. pulzní gelová elektroforéza. Z gelu je možné následně DNA převést na nitrocelulózovou membránu pomocí tzv. Southernova přenosu. Další metodou dělení DNA je centrifugace v hustotním gradientu, obvykle v gradientu chloridu cesného – tato metoda odděluje zejména fragmenty, jež se liší zastoupením bází (obsahem GC).[62]
Barvení[editovat | editovat zdroj]

Byl vyvinut nespočet způsobů, jak obarvit DNA – a to jak přímo v buňce, tak i DNA izolovanou v laboratorním skle. Používají se často v laboratořích ve chvíli, kdy je nutné např. v elektroforetickém gelu či přímo ve fixované buňce zvýraznit DNA. Ke známým takovým barvivům patří (bez logické následnosti): SYBR Green, YOYO-1, TOTO-1, TO-PRO, SYTOX Green, ale i klasický ethidiumbromid a propidiumjodid, akridinová oranž, různá Hoechst barviva či třeba DAPI.[63] K velmi specifickým barvícím metodám patří fluorescenční in situ hybridizace (FISH), která umožňuje navázání fluorescenčních sond na konkrétní sekvenci DNA.[64]
Sekvenování a umělá syntéza[editovat | editovat zdroj]

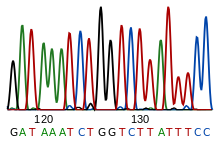
Sekvenování DNA je souhrnný termín pro biochemické metody, jimiž se zjišťuje pořadí nukleových bází v sekvencích DNA.[65] Právě pořadí bází je princip zakódování genetické informace, a proto je v centru zájmu biologů. Původní a po dlouhá léta převažující metodou bylo tzv. Sangerovo sekvenování, které využívá speciálně chemicky upravených nukleotidů, jež jsou pomocí DNA polymerázy zařazovány s určitou pravděpodobností do prodlužující se DNA – tím blokují další polymeraci a výsledný produkt je možné detekovat pomocí elektroforézy. V souvislosti se snahou zrychlit a zlevnit sekvenovací proces byla vyvinuta celá řada sekvenačních metod nové generace. K těm patří např. pyrosekvenování a příbuzné metody. Studie Zhang et al. 2011 uvádí pět moderních metod, jež jsou komerčně dostupné: Roche GS-FLX 454 („454 sekvenování“), Illumina („Solexa“), ABI SOLiD, Polonator G.007 a Helicos HeliScope.[66]
Existuje i celá řada postupů, jak si připravit či namnožit konkrétní molekulu DNA. Jednou z možností je chemická syntéza DNA, při níž dochází k sestavování krátkých oligonukleotidů, a to postupným řazením nukleotidů za sebou. V typickém případě však již je určité množství DNA k dispozici a je žádoucí ho pouze zmnožit tak, aby všechny kopie měly pokud možno totožnou sekvenci. To se často dělá buď pomocí klonování DNA nebo metodou polymerázové řetězové reakce.[67]
Význam ve společnosti[editovat | editovat zdroj]
Lékařská diagnostika[editovat | editovat zdroj]
Vědecký pokrok v oblasti genetiky způsobil boom v mnoha oblastech lékařské diagnostiky. Například v bakteriologii, virologii a parazitologii se uplatnily metody, jež umožňují v napadené tkáni detekovat DNA pocházející z mikroorganismů, jež tuto tkáň napadly. To se dělá buď pomocí různých DNA prób schopných se specificky vázat na určitou sekvenci typickou pro daného parazita, nebo např. cestou namnožení DNA pomocí polymerázové řetězové reakce a následným sekvenováním – tím je možné získat sekvenci DNA patogenních organismů, jíž mikrobiologové srovnají s databázemi patogenních kmenů. Tyto pokročilé molekulární metody se uplatňují např. při identifikaci těžko kultivovatelných bakterií či při určování celé řady virových či parazitárních onemocnění.[68]
Součástí diagnostické práce je však i studium lidské DNA – uplatňuje se například v rakovinné terapii[69] či při diagnostice některých genetických onemocnění. Své místo již molekulární metody našly v prenatální diagnostice chorob, např. ze vzorku plodové vody.[70] Další testy se rutinně provádí z kapky krve novorozenců. Testy DNA v rámci genetického poradenství však dnes mohou pomoci i párům, jež teprve dítě plánují. Je to vhodné tehdy, vyskytuje-li se v rodinné historii nějaké genetické onemocnění. Dnes jsou genetické testy dostupné všem zájemcům a je možné o sobě zjistit celou řadu informací od těch zřejmých (barva očí) přes různé zajímavosti (atletické vlohy) až po vážné údaje (náchylnost k rakovině atp.).[71]
Genetická daktyloskopie[editovat | editovat zdroj]

Některé oblasti např. lidské jaderné DNA jsou velmi proměnlivé a člověk od člověka se v nich téměř vždy liší. Z tohoto důvodu je DNA v kriminalistice a v forenzních vědách neocenitelným zdrojem informací. Repetitivní sekvence známé jako VNTR či STR patří mezi ty nejčastěji studované. Studium VNTR repetic vyžaduje relativně velké množství DNA, a proto se využívá zejména tehdy, máme-li k dispozici vzorek krve (např. u testů otcovství). Obvykle se testují metodou RFLP (jenž zkoumá polymorfismus délky restrikčních fragmentů). V kriminalistice našly větší využití tzv. STR (čili ~mikrosatelity). Pravděpodobnost, že dvě osoby budou mít jednu STR oblast shodnou, je pro danou variantu např. 1 : 83, což by nebylo příliš přesvědčivé, a proto se používá obvykle 13 markerů, které se vyhodnocují zvlášť a vzájemný pozitivní výsledek důvěryhodnost testu mnohonásobně zvyšuje. První použití DNA v kriminalistice se datuje do roku 1986 a došlo k němu v rámci soudního řízení v Anglii. Testování STR oblastí se však dnes prosazuje i v určování otcovství.[72]
Genetická manipulace[editovat | editovat zdroj]
V současnosti je lidstvo schopné provádět cílené změny v genetické informaci (v pořadí nukleotidů v DNA) a ovlivňovat tím některé vlastnosti organismů. Tyto tzv. genetické modifikace způsobily revoluci v celé řadě biotechnologických odvětví a umožňují např. průmyslovou produkci hormonů, srážecích faktorů pro hemofiliky, enzymů užívaných v potravinářství a některých vakcín. Výsledkem genetického inženýrství jsou i různé transgenní plodiny, např. ty odolné k herbicidům.[73] V Evropské unii je z geneticky modifikovaných plodin povolena pouze Bt kukuřice,[74] která nese gen cry pocházející z půdní bakterie Bacillus thuringiensis. Tento gen způsobuje, že je rostlina pro své hmyzí škůdce jedovatá.[75]
Biologická systematika[editovat | editovat zdroj]
V neposlední řadě se studium sekvencí DNA uplatňuje v třídění organismů podle jejich příbuznosti, tedy v oboru biologie známém jako fylogenetika. Jedním z prvních krůčků v tomto oboru byla v 60. letech studie, která srovnávala sekvenci genu pro cytochrom c u různých organismů: výsledky jsou v podstatě intuitivní, zatímco šimpanz má sekvenci tohoto genu s člověkem zcela shodnou a makak rhesus se liší pouze jedinou nukleotidovou záměnou, psí gen pro cytochrom už se od lidského genu liší na 13 místech a kvasinkový gen dokonce na 56 pozicích. Na základě těchto informací si lze udělat obrázek o příbuzenských vztazích mezi organismy. V souvislosti s rozmachem sekvenování je dnes k dispozici obrovské množství sekvencí DNA celé řady organismů a k jejich analýze se používají různé sofistikované nástroje, jako například metoda parsimonie nebo metoda maximální pravděpodobnosti. Dnes je možno i odhadnout čas, který dělí v evoluční historii libovolné dva druhy – metoda k tomu užívaná opět pracuje se sekvencemi DNA a označuje se jako molekulární hodiny. Pomocí fylogenetických přístupů je možno odpovídat na celou řadu dalších otázek, namátkou „jaký vztah mají neandertálci k dnešním lidem“, „jak se mezi jednotlivými nemocnými šíří virus HIV“ a podobně.[76]
Pravěká DNA[editovat | editovat zdroj]
Od 50. a 60. let 20. století se objevují studie o údajném izolování sekvencí DNA pravěkých organismů.[77] V 80. a 90. letech přinesl tomuto oboru („paleogenetika“) slávu Crichtonův román a jeho Spielbergova filmová adaptace Jurský park (1993), ve kterém byli naklonováni druhohorní (nejen ti z jury) dinosauři. Dinosauří proteiny a měkké tkáně byly skutečně získány např. Mary H. Schweitzerovou a jejím týmem[78], pravěká DNA dinosaurů ale nejspíš nikdy získána nebude.[79][80][81] Nepotvrdily se ani domněnky o získání DNA ze 120–135 milionů let starého libanonského jantaru entomologem Georgem Poinarem v roce 1993.[81][82][83] Lze ovšem získat DNA starou více než 1 milión let.[84]
Některé paleontologické objevy nicméně naznačují, že alespoň stopy po původní DNA mohou být v dinosauřích fosiliích z období druhohor skutečně objeveny.[78][85][86]
U malého opeřeného dinosaura rodu Caudipteryx, žijícího na území Číny před 125 miliony let (období rané křídy), byla v roce 2021 identifikována fosilie původní buněčné struktury, která by mohla být chromatinem (obsahovat jakési pozůstatky komplexu DNA a bílkovin).[87]
Odkazy[editovat | editovat zdroj]
Poznámky[editovat | editovat zdroj]
- ↑ Ve skutečnosti se jich v DNA přirozeně vyskytuje 8, neboť kvůli zamezení genové exprese jsou některé cytosinové báze methylovány a cytosin je nahrazen 5-methylcytosinem či 5-hydroxymethylcytosinem, naopak při demethylaci vznikají ještě 5-formylcytosin a 5-karboxylcytosin.[14] Methylace bází je jedním z klíčových epigenetických mechanismů.
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku DNA na anglické Wikipedii.
- ↑ a b SEEMAN, N. C. DNA nanotechnology: novel DNA constructions. Annu Rev Biophys Biomol Struct. 1998, roč. 27, s. 225–48. Dostupné online [PDF]. ISSN 1056-8700. (anglicky) Archivováno 10. 1. 2011 na Wayback Machine.
- ↑ Dahm R. Discovering DNA: Friedrich Miescher and the early years of nucleic acid research. Hum. Genet. January 2008, roč. 122, čís. 6, s. 565–81. DOI 10.1007/s00439-007-0433-0. PMID 17901982. (anglicky)
- ↑ Levene, P. The structure of yeast nucleic acid. J Biol Chem. 1. prosinec 1919, roč. 40, čís. 2, s. 415–24. Dostupné v archivu pořízeném dne 2009-06-29. (anglicky) Archivováno 29. 6. 2009 na Wayback Machine.
- ↑ Avery O., MacLeod C., McCarty M. Studies on the chemical nature of the substance inducing transformation of pneumococcal types. Inductions of transformation by a desoxyribonucleic acid fraction isolated from pneumococcus type III. J Exp Med. 1944, roč. 79, čís. 2, s. 137–158. Dostupné online. DOI 10.1084/jem.79.2.137. PMID 19871359. (anglicky)
- ↑ Watson J.D. and Crick F.H.C. A Structure for Deoxyribose Nucleic Acid. Nature. 1953, roč. 171, čís. 4356, s. 737–738. Dostupné online [PDF]. DOI 10.1038/171737a0. PMID 13054692. (anglicky)
- ↑ Wilkins, M.H.F; A.R. Stokes; Wilson, H.R. Molecular Structure of Deoxypentose Nucleic Acids. Nature. 1953, roč. 171, čís. 4356, s. 738–740. Dostupné online [PDF]. DOI 10.1038/171738a0. PMID 13054693. (anglicky)
- ↑ Crick, F.H.C. On degenerate templates and the adaptor hypothesis (PDF). Archivováno 1. 10. 2008 na Wayback Machine. genome.wellcome.ac.uk (Lecture, 1955). Accessed 22 December 2006
- ↑ CAMMACK, R., et al. Oxford dictionary of biochemistry and molecular biology; revised edition. New York: Oxford University Press, 2006. ISBN 0-19-852917-1. S. 415. (anglicky)
- ↑ The Nobel Prize in Physiology or Medicine 1968 Nobelprize.org Accessed 22 December 06
- ↑ FLEGR, Jaroslav. Evoluční biologie. 2., rozšířené vyd. Praha: Academia, 2009. ISBN 978-80-200-1767-3. Kapitola Kulturní evoluce, s. 320–329.
- ↑ VREELAND, R. H; ROSENZWEIG, W. D; POWERS, D. W. Isolation of a 250 million-year-old halotolerant bacterium from a primary salt crystal. Nature. 19. říjen 2000, roč. 407, čís. 6806, s. 897–900. Dostupné online. ISSN 0028-0836. (anglicky)
- ↑ FISH, S. A; SHEPHERD, T. J; MCGENITY, T. J, et al. Recovery of 16S ribosomal RNA gene fragments from ancient halite. Nature. 2002, roč. 417, čís. 6887, s. 432–6. Dostupné online. ISSN 0028-0836. (anglicky)
- ↑ VOET, Donald; VOET, Judith. Biochemistry. 4. vyd. [s.l.]: Wiley, 2010. Dostupné online. ISBN 978-0470-57095-1. S. 94. (anglicky)
- ↑ Scientists identify seventh and eighth bases of DNA[nedostupný zdroj], PhysOrg podle Science, 21. 7. 2011 (anglicky)
- ↑ 2007 7.013 Problem Set 3 [PDF]. Massachusetts Institute of Technology. Dostupné online. (anglicky)[nedostupný zdroj]
- ↑ WOLFE-SIMON, F; SWITZER BLUM, J; KULP, T. R, et al. A bacterium that can grow by using arsenic instead of phosphorus. Science. 2011, roč. 332, čís. 6034, s. 1163–6. Dostupné online. ISSN 1095-9203. (anglicky)
- ↑ REAVES, Marshall Louis; SINHA, Sunita; RABINOWITZ, Joshua D, KRUGLYAK Leonid, REDFIELD Rosemary J. Absence of Detectable Arsenate in DNA from Arsenate-Grown GFAJ-1 Cells. Science [online]. 8. červenec 2012. Online před tiskem. Dostupné online. ISSN 1095-9203. DOI 10.1126/science.1219861. (anglicky)
- ↑ ERB, Tobias J; KIEFER, Patrick; HATTENDORF, Bodo, GÜNTHER Detlef, VORHOLT Julia A. GFAJ-1 Is an Arsenate-Resistant, Phosphate-Dependent Organism. Science [online]. 8. červenec 2012. Online před tiskem. Dostupné online. ISSN 1095-9203. DOI 10.1126/science.1218455. (anglicky)
- ↑ SHERIDAN, Kerry: Scientists say NASA's 'new arsenic form of life' was untrue (popularizační článek k předchozím 2 referencím). PhysOrg, 9. červenec 2012 (anglicky)
- ↑ Voet & Voet, s. 84–85
- ↑ NELSON, David L; COX, Michael M. Lehninger Principles of Biochemistry. 5. vyd. New York: W. H. Freeman and Company, 2008. Dostupné online. ISBN 978-0-7167-7108-1. S. 282. (anglicky)
- ↑ LODISH, Harvey, et al. Molecular Cell Biology. New York: W.H. Freedman and Company, 2004. Dostupné online. ISBN 0-7167-4366-3. S. 123. (anglicky)
- ↑ HOUSER, Pavel. DNA drží při sobě spíše hydrofobní interakce než vodíkové můstky. sciencemag.cz [online]. 2020-01-02 [cit. 2021-05-08]. Dostupné online.
- ↑ Cammack, s. 47
- ↑ DUKE, Tom, et al. Multiple aspects of DNA and RNA: from Biophysics to Bioinformatics. Příprava vydání Didier Chatenay, et al. [s.l.]: Elsevier, 2005. ISBN 0-444-52081-3. (anglicky)
- ↑ VARGASON, J. M; HENDERSON, K; HO, P. S. A crystallographic map of the transition from B-DNA to A-DNA. Proc Natl Acad Sci U S A. 2001, roč. 98, čís. 13, s. 7265–70. Dostupné online. ISSN 0027-8424. (anglicky)
- ↑ HA, S. C; LOWENHAUPT, K; RICH, A, et al. Crystal structure of a junction between B-DNA and Z-DNA reveals two extruded bases. Nature. 2005, roč. 437, čís. 7062, s. 1183–6. Dostupné online. ISSN 1476-4687. (anglicky)
- ↑ Voet & Voet, s. 1212
- ↑ ARCELLA, Annalisa; PORTELLA, Guillem; LUZ RUIZ, Maria, et al. Structure of Triplex DNA in the Gas Phase. Journal of the American Chemical Society. 2012, roč. 134, čís. 15, s. 6596–6606. Dostupné online. DOI 10.1021/ja209786t. (anglicky)
- ↑ First description of a triple DNA helix in a vacuum (popularizační článek k předchozí referenci). PhysOrg, 18. dubna 2012 (anglicky)
- ↑ Cammack, s. 679
- ↑ Lodish, s. 105
- ↑ GUO, Q; LU, M; CHURCHILL, M. E, et al. Asymmetric structure of a three-arm DNA junction. Biochemistry. 1990, roč. 29, čís. 49, s. 10927–34. ISSN 0006-2960. (anglicky)
- ↑ COOPER, J. P; HAGERMAN, P. J. Geometry of a branched DNA structure in solution. Proceedings of the National Academy of Sciences of the United States of America. 1989-10, roč. 86, čís. 19, s. 7336–7340. ISSN 0027-8424. (anglicky)
- ↑ ARENDS, Erik. Second layer of information in DNA confirmed. phys.org [online]. 2016-06-08 [cit. 2021-05-08]. Dostupné online. (anglicky)
- ↑ ALBERTS, B., et al. The Molecular Biology of the Cell. 5. vyd. [s.l.]: Garland Science, 2007. Dostupné online. ISBN 978-0-8153-4105-5. S. 344. (anglicky)
- ↑ WITZ, G; STASIAK, A. DNA supercoiling and its role in DNA decatenation and unknotting. Nucleic Acids Res. 2010, roč. 38, čís. 7, s. 2119–33. Dostupné online. ISSN 1362-4962. (anglicky)
- ↑ GRISWOLD, Ann. Genome Packaging in Prokaryotes: the Circular Chromosome of E. coli [online]. Nature Education, 2008. Dostupné online. (anglicky)
- ↑ Alberts, s. 211
- ↑ Technical Appendix [online]. Epibio - Epicentre® (an Illumina® company), 2011 [cit. 2011-07-15]. Dostupné v archivu pořízeném z originálu dne 2012-01-19. (anglicky)
- ↑ OSWALD, Nick. The Basics: How Ethanol Precipitation of DNA and RNA Works [online]. Bitesize Bio, 4. prosinec 2007. Dostupné online. (anglicky)
- ↑ Onion Genomic DNA Isolation [PDF]. G-Biosciences. Dostupné online. (anglicky)[nedostupný zdroj]
- ↑ MULLIGAN, Martin E. The physical and chemical properties of nucleic acids [online]. 1996–2003 [cit. 2011-07-15]. Dostupné v archivu pořízeném dne 2010-05-02. (anglicky)
- ↑ VONDREJS, Vladimír; STORCHOVÁ, Zuzana. Genové inženýrství, I. Praha: Karolinum, 1997. S. 22.
- ↑ MIHULKA, Stanislav. Jaký je poločas rozkladu DNA? [online]. OSEL. Dostupné online.
- ↑ RNA vs DNA [online]. NEWTON - Ask a scientist, 2007 [cit. 2011-08-06]. Dostupné v archivu. (anglicky)
- ↑ Current Protocols in Molecular Biology. [s.l.]: John Wiley & Sons, Inc., 2002. Dostupné online. (anglicky)
- ↑ ŠRUBAŘOVÁ, P; DVOŘÁK, J. VYUŽITÍ CHITOSANU PRO UCHOVÁNÍ DNA A BIOLOGICKÝCH VZORKŮ. mendelu.cz [PDF]. [cit. 2018-08-15]. Dostupné online. (anglicky, česky)
- ↑ MARGUET, E; FORTERRE, P. DNA stability at temperatures typical for hyperthermophiles. Nucleic Acids Research. 1994-05-11, roč. 22, čís. 9, s. 1681–1686. ISSN 0305-1048. (anglicky)
- ↑ Alberts, s. 260
- ↑ a b Nelson & Cox, s. 271
- ↑ SHERWOOD, Lauralee. Human physiology: from cells to systems. 7. vyd. [s.l.]: Cengage Learning, 2008. 928 s. Dostupné online. S. 395. (anglicky)
- ↑ HUNT, Margaret. Virology [online]. 2010. Kapitola „RNA virus replication strategies“. Dostupné v archivu pořízeném z originálu. (anglicky)
- ↑ MARATHE, A; CONDON, A. E; CORN, R. M. On combinatorial DNA word design. J Comput Biol. 2001, roč. 8, čís. 3, s. 201–19. Dostupné online. ISSN 1066-5277. (anglicky)
- ↑ LITTLE, Peter F. R. Structure and function of the human genome. Genome Research. 2005-12, roč. 15, čís. 12, s. 1759–1766. Dostupné online. DOI 10.1101/gr.4560905. (anglicky)
- ↑ Alberts, s. 253
- ↑ Alberts, s. 204
- ↑ JHA, Alok. Breakthrough study overturns theory of 'junk DNA' in genome. The Guardian. 5. září 2012. Dostupné online. (anglicky)
- ↑ HAMZELOU, Jessica. Global project reveals just how active our 'junk' DNA is [online]. New Scientist, 6. září 2012 [cit. 2012-09-11]. Dostupné v archivu pořízeném dne 2012-09-11. (anglicky)
- ↑ Vondrejs & Storchová, s. 17
- ↑ a b Vondrejs & Storchová, s. 18
- ↑ Voet & Voet, s. 159
- ↑ Nucleic Acid Stains—Section 8.1 [online]. InVitrogen life technologies. Dostupné online. (anglicky)
- ↑ Cammack, s. 248
- ↑ RACLAVSKÝ, Vladislav. Úvod do základních metod molekulární genetiky [PDF]. Ústav biologie Lékařské fakulty Univerzity Palackého v Olomouci, červen 1999 [cit. 2018-08-27]. Kapitola 8. Sekvenování DNA, s. 21–24. Dostupné online. ISBN 80-7067-892-5.
- ↑ ZHANG, J; CHIODINI, R; BADR, A, et al. The impact of next-generation sequencing on genomics. J Genet Genomics. 2011, roč. 38, čís. 3, s. 95–109. Dostupné online. ISSN 1673-8527. (anglicky)
- ↑ VONDREJS, Vladimír. Genové inženýrství, II. Praha: Karolinum, 2001. S. 22.
- ↑ KAYSER, F. H, et al. Medical Microbiology. [s.l.]: Thieme, 2005. Dostupné online. S. 216. (anglicky)
- ↑ BRONCHUD, Miguel H, et al. Totowa, New Jersey: Humana Press, 2000. S. 45. (anglicky)
- ↑ SADLER, Thomas W. Langman’s Medical Embryology. [s.l.]: Lippincott Williams & Wilkins, 2009. Dostupné online. S. 163. (anglicky)
- ↑ LEWIS, Ricki. Human Genetics: Concepts and Applications. 9. vyd. [s.l.]: McGraw−Hill, 2009. Dostupné online. S. 400. (anglicky)
- ↑ William S. Klug, Michael R. Cummings, Charlotte A. Spencer. Concepts of Genetics. 8. vyd. [s.l.]: [s.n.], 2006. S. 567–568. (anglicky)
- ↑ Klug & Cunnings, s. 550
- ↑ DROBNÍK, Jaroslav. Přehledy o dopadech transgenních plodin [online]. 2010. Dostupné online.
- ↑ MIHULKA, Stanislav. Geneticky modifikovaná kukuřice a chrostíci [online]. 2007. Dostupné online.
- ↑ Klug & Cunnings, s. 656–658
- ↑ JONES, Elizabeth D. Ancient DNA: s history of the science before Jurassic Park. Studies in History and Philosophy of Science, Part C: Studies in History and Philosophy of Biological and Biomedical Sciences [online]. Elsevier B.V, 9. březen 2018. Online před tiskem. Dostupné online. ISSN 1369-8486. DOI 10.1016/j.shpsc.2018.02.001. (anglicky)
- ↑ a b Paul V. Ullmann, Kyle Macauley, Richard D. Ash, Ben Shoup and John B. Scannella (2021). Taphonomic and Diagenetic Pathways to Protein Preservation, Part I: The Case of Tyrannosaurus rex Specimen MOR 1125. Biology. 10 (11): 1193. doi: https://doi.org/10.3390/biology10111193
- ↑ GUTIÉRREZ, Gabriel; MARÍN, Antonio. The most ancient DNA recovered from an amber-preserved specimen may not be as ancient as it seems. Molecular Biology and Evolution. 7. červenec 1998, svazek 15, čís. s. 926–929. [http://mbe.oxfordjournals.org/content/15/7/926.full.pdf Dostupné online [PDF, cit. 2016-11-22]. ISSN 737-4038. (anglicky)
- ↑ PALMER, Roxanne. 'Jurassic Park' Method Of Cloning Dinosaurs From Amber-Preserved Insects Not Feasible, Scientists Say. Internation Business Times [online]. IBT Media Inc., 13. listopad 2009 [cit. 2016-11-22]. Dostupné online. (anglicky)
- ↑ a b SOCHA, Vladimír. Byla skutečně objevena dinosauří DNA?. Osel.cz [online]. 25. duben 2016. Dostupné online.
- ↑ AUSTIN, Jeremy J; ROSS, Andrew J; SMITH, Andrew B; FORTEY, Richard A; THOMAS, Richard H. Problems of reproducibility – does geologically ancient DNA survive in amber–preserved insects?. S. 467–474. Proceedings of the Royal Society B [online]. 22. duben 1997 [cit. 2016-11-22]. Svazek 264, čís. 1381, s. 467–474. Dostupné online. Dostupné také na: [1]. Dále dostupné na: [2]. ISSN 1471-2954. DOI 10.1098/rspb.1997.0067. PMID 9149422. (anglicky)
- ↑ PENNEY, David; WADSWORTH, Caroline; FOX, Graeme; KENNEDY, Sandra L; PREZIOSI, Richard F; BROWN, Terence A. Absence of Ancient DNA in Sub-Fossil Insect Inclusions Preserved in ‘Anthropocene’ Colombian Copal. PLoS ONE [online]. 11. září 2013 [cit. 2016-11-22]. Svazek 8, čís. 9: e73150. Dostupné online. ISSN 1932-6203. DOI 10.1371/journal.pone.0073150. (anglicky)
- ↑ 'Game-changing' research could solve evolution mysteries. phys.org [online]. 2019-09-11 [cit. 2021-05-08]. Dostupné online. (anglicky)
- ↑ BAILLEUL, Alida M; ZHENG, Wenxia; HORNER, John R; HALL, Brian K; HOLLIDAY, Casey M; SCHWEITZER, Mary H. Evidence of proteins, chromosomes and chemical markers of DNA in exceptionally preserved dinosaur cartilage. S. 815–822. National Science Review [online]. 2020-04-01 [cit. 2021-05-08]. Roč. 7, čís. 4, s. 815–822. Dostupné online. DOI 10.1093/nsr/nwz206. (anglicky)
- ↑ SOCHA, Vladimír. Příběh gravidní tyranosauřice pokračuje. OSEL.cz [online]. 23. prosince 2021. Dostupné online. (česky)
- ↑ SOCHA, Vladimír. O krůček blíž k Jurskému parku. OSEL.cz [online]. 28. října 2021. Dostupné online. (česky)
Literatura[editovat | editovat zdroj]
- Česky
- ROSYPAL, Stanislav. Úvod do molekulární biologie. První díl, Vstup do molekulární biologie. Molekulární biologie prokaryotické buňky. 4. inov. vyd. Brno: Rosypal, 2006. 289 s. ISBN 80-902562-5-2.
- VOET, Donald; VOET, Judith. Biochemie (původním názvem: Biochemistry). Překlad Arnošt Kotyk a kolektiv. 1. vyd. Praha: Victoria Publishing, 1995. xiv, 1325, xxiii s. ISBN 80-85605-44-9.
- ŠTÍPEK, Stanislav. Stručná biochemie : uchování a exprese genetické informace : učební texty. Praha: Medprint, 1997. 92 s. Dostupné online. ISBN 80-902036-2-0.
- ŠMARDA, Jan, et al. Metody molekulární biologie. Brno: MU Brno, 2005. 188 s. ISBN 80-210-3841-1.
- Anglicky
- ALBERTS, Bruce, a kol. The Molecular Biology of the Cell. 5. vyd. New York: Garland Science, 2007. 1600 s. ISBN 978-0-8153-4105-5.
- LODISH, Harvey, et al. Molecular Cell Biology. New York: W. H. Freedman and Company, 2004. Dostupné online. ISBN 0-7167-4366-3.
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu DNA na Wikimedia Commons
Obrázky, zvuky či videa k tématu DNA na Wikimedia Commons  Slovníkové heslo DNA ve Wikislovníku
Slovníkové heslo DNA ve Wikislovníku- (česky) DNA nahrazuje pevné disky i procesory – současné technické možnosti využití DNA pozn. Celý článek je k dispozici za poplatek
- (anglicky) Fidelitysystems.com – fotografie DNA pod elektronovým mikroskopem
- (anglicky) DNA Learning Center – internetová stránka zaměřená na popularizaci a výuku informací o DNA a souvisejících tématech
- (anglicky) DNA & RNA na portálu amerického NCBI – seznam vědeckých databází a informačních zdrojů
- (anglicky) DNA from the Beginning – přehledný popis 75 objevů, které změnily pohled na genetiku a na DNA
- (anglicky) National DNA Day – výukové materiály, různé učebnice a články na téma DNA
- (anglicky) DNA – Molecule of the Month – přehledný článek o struktuře DNA Archivováno 4. 9. 2012 na Wayback Machine.