Chlorid berylnatý
| Chlorid berylnatý | |
|---|---|
 Kuličkovo–tyčinkový model části krystalické struktury | |
| Obecné | |
| Systematický název | Chlorid berylnatý |
| Anglický název | Beryllium chloride Beryllium(I) chloride |
| Německý název | Berylliumchlorid |
| Sumární vzorec | BeCl2 |
| Vzhled | Bezbarvá, bílá nebo žlutá krystalická látka |
| Identifikace | |
| Registrační číslo CAS | 7787-47-5 |
| PubChem | 24588 |
| SMILES | [Be+2].[Cl-].[Cl-] |
| InChI | 1S/Be.2ClH/h;2*1H/q+2;;/p-2 |
| Číslo RTECS | DS2625000 |
| Vlastnosti | |
| Molární hmotnost | 79,918 2 g/mol |
| Teplota tání | 399 °C, 672 K, 750 °F |
| Teplota varu | 482 °C, 755 K, 900 °F |
| Hustota | 1,899 g/cm3 1,835 g/cm3 (dihydrát) 1,712 g/cm3 (pevná látka) |
| Rozpustnost ve vodě | 15,1 g/100 ml (20 °C) |
| Rozpustnost v polárních rozpouštědlech | Rozpustný v alkoholu a etheru |
| Rozpustnost v nepolárních rozpouštědlech | Rozpustný v pyridinu |
| Struktura | |
| Tvar molekuly | polymerní |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | −490,4 kJ/mol |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
Některá data mohou pocházet z datové položky. | |
Chlorid berylnatý je anorganická sloučenina se vzorcem BeCl2. Jedná se o bezbarvou až bílou či žlutou krystalickou a hygroskopickou látku dobře rozpustnou v mnoha polárních rozpouštědlech.
Jeho vlastnosti jsou téměř stejné jako u chloridu hlinitého.
Příprava[editovat | editovat zdroj]
BeCl2 se připravuje slučováním kovového beryllia s chlorem při vysoké teplotě[2]
Be + Cl2 → BeCl2.
Také je možné jej připravit redukcí oxidu berylnatého uhlíkem při vysoké teplotě za přítomnosti chloru[3] nebo
Struktura[editovat | editovat zdroj]
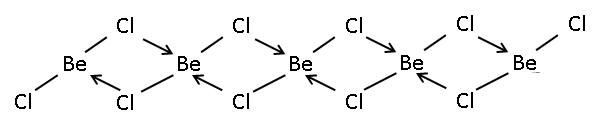 Pevný BeCl2 je jednorozměrný polymer sestávající z tetraedrických struktur.[4]
Pevný BeCl2 je jednorozměrný polymer sestávající z tetraedrických struktur.[4]
Liší se tím od BeF2, který je trojrozměrným polymerem se strukturou podobnou struktuře křemenu.
Podobné sloučeniny[editovat | editovat zdroj]
- Fluorid berylnatý
- Bromid berylnatý
- Jodid berylnatý
- Chlorid hořečnatý
- Chlorid vápenatý
- Chlorid strontnatý
- Chlorid barnatý
- Chlorid radnatý
- Fluorid vápenatý
- Fluorid strontnatý
- Fluorid barnatý
- Bromid barnatý
- Jodid barnatý
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku Beryllium chloride na anglické Wikipedii.
- ↑ a b Beryllium chloride. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ Irving R. Tannenbaum "Beryllium Chloride" Inorganic Syntheses, 1957, vol. 5, p.22. DOI:10.1002/9780470132364.ch7
- ↑ Cotton, F.A.; Wilkinson, G. (1980) Advanced Inorganic Chemistry John Wiley and Sons, Inc: New York, ISBN 0-471-02775-8.
- ↑ Wells, A.F. (1984) Structural Inorganic Chemistry, Oxford: Clarendon Press. ISBN 0-19-855370-6.
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu chlorid berylnatý na Wikimedia Commons
Obrázky, zvuky či videa k tématu chlorid berylnatý na Wikimedia Commons





