Dusičnan amonný
| Dusičnan amonný | |
|---|---|
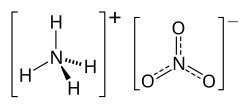 2D model molekuly NH4NO3 | |
 | |
| Obecné | |
| Systematický název | Dusičnan amonný |
| Triviální název | Ledek amonný |
| Ostatní názvy | Amoniumnitrát |
| Anglický název | Ammonium nitrate |
| Německý název | Ammoniumnitrat |
| Sumární vzorec | NH4NO3 |
| Vzhled | bílé krystalky nebo prášek |
| Identifikace | |
| Registrační číslo CAS | 6484-52-2 |
| Číslo RTECS | BR9050000 |
| Vlastnosti | |
| Molární hmotnost | 80,043 g/mol |
| Teplota tání | 169,6 °C |
| Teplota rozkladu | 210 °C |
| Hustota | 1,725 g/cm3 1,66 g/cm3 (170 °C) |
| Index lomu | α - modifikace nDa= 1,45 nDb= 1,59 nDc= 1,63 β - modifikace nD= 1,413 (20 °C) |
| Rozpustnost ve vodě | 117,43 g/100 ml (0 °C) 150 g/100 ml (10 °C) 189,87 g/100 ml (20 °C) 246,25 g/100 ml (32 °C) 421 g/100 ml (60 °C) 600 g/100 ml (80 °C) 871 g/100 ml (100 °C) |
| Rozpustnost v polárních rozpouštědlech | methanol 17,1 g/100 ml (20 °C) ethanol 3,80 g/100 ml (20 °C) aceton diethylether (ne) |
| Měrná magnetická susceptibilita | -5,2×10−6 cm3g-1 |
| Struktura | |
| Krystalová struktura | kosočtverečná (α) krychlová (β) tetragonální (γ) |
| Hrana krystalové mřížky | a= 575 pm b= 545 pm c= 496 pm |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | -365,1 kJ/mol |
| Entalpie tání ΔHt | 80,0 J/g |
| Entalpie rozpouštění ΔHrozp | 321 J/g |
| Standardní molární entropie S° | 151 JK-1mol-1 |
| Standardní slučovací Gibbsova energie ΔGf° | -183,8 kJ/mol |
| Izobarické měrné teplo cp | 1,737 JK-1g-1 |
| Bezpečnost | |
| R-věty | R8,R36,R37,R38 |
| S-věty | S15,S16,S26,S36 |
| NFPA 704 |  0
2
3
OX
|
Některá data mohou pocházet z datové položky. | |
Dusičnan amonný, triviálním názvem ledek amonný či amoniumnitrát, je chemická sloučenina (dusičnan amoniaku) s chemickým vzorcem NH4NO3. Je to bílá krystalická látka používaná jako zemědělské hnojivo, dezinfekční prostředek vody a díky oxidačním vlastnostem také v pyrotechnice. Může vznikat přeměnou močoviny:
Dusičnan amonný je uveden v seznamu látek (tzv. prekurzorů výbušnin), na které se má podle navrhovaného nařízení vztahovat sledování prodeje nepodnikajícím fyzickým osobám.[1] Při prudkém zahřívání se sám o sobě totiž rozkládá explozivně.
Příprava
Dusičnan amonný se připravuje reakcí kyseliny dusičné a čpavku.[2]
- HNO3 + NH3 → NH4NO3.
Dusičnan amonný se také vyrábí amatérskými nadšenci reakcí:
- (NH4)2SO4 + 2 NaNO3 → Na2SO4 + 2 NH4NO3
- Ca(NO3)2 + (NH4)2SO4 → 2 NH4NO3 + CaSO4[zdroj?]
Tato reakce je silně exotermní. Lze ho také připravit reakcí AgNO3(aq) s NH4Cl(aq), přičemž vzniká jako nerozpustná sůl AgCl, která se dá odfiltrovat, takže výtěžek je pak poměrně vysoký.
Využití
- V zemědělství jako hnojivo
- V dezinfekci vod (vodovody, bazény)
- V pyrotechnice
Reference
Literatura
- VOHLÍDAL, JIŘÍ; ŠTULÍK, KAREL; JULÁK, ALOIS. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.

