Kyanid lithný
| Kyanid lithný | |
|---|---|
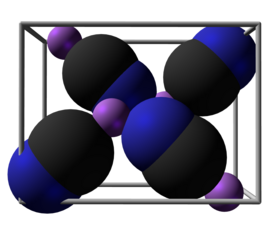 Krystal kyanidu lithného | |
| Obecné | |
| Systematický název | Kyanid lithný |
| Anglický název | Lithium cyanide |
| Německý název | Lithiumcyanid |
| Sumární vzorec | LiCN |
| Vzhled | bílé krystalky nebo prášek |
| Identifikace | |
| Registrační číslo CAS | 2408-36-8 |
| Vlastnosti | |
| Molární hmotnost | 32,959 g/mol |
| Teplota tání | 160 °C |
| Hustota | 1,073 g/cm³ (18 °C) |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| R-věty | 26/27/28-32-50/53 |
| S-věty | 7-28-29-45-60-61 |
| NFPA 704 |  0
0
|
Některá data mohou pocházet z datové položky. | |
Kyanid lithný (chemický vzorec LiCN) je bezbarvá krystalická nebo bílá práškovitá látka patřící mezi anorganické iontové sloučeniny. Je to lithná sůl kyseliny kyanovodíkové. Využívá se především jako reagenční činidlo při syntéze sloučenin.
Vlastnosti
[editovat | editovat zdroj]Stabilita a reaktivita
[editovat | editovat zdroj]Kyanid lithný je v pevném stavu stabilní za laboratorní teploty. Taje při 160 °C a tavenina je silně hygroskopická. Při zahřátí nad 600 °C se rozkládá za vzniku kyanamidu a uhlíku. Reakcí s kyselinami, chlornany a silnými oxidačními činidly dochází ke vzniku silně toxického a vysoce reaktivního plynného kyanovodíku HCN.[2]
Chemické reakce
[editovat | editovat zdroj]Syntéza
[editovat | editovat zdroj]Kyanid lithný lze ve velmi dobrém výtěžku připravit reakcí kapalného kyanovodíku s n-butyllithiem. Jiné metody vycházejí prostě z kontaktu kationtu Li s kyanidovým aniontem. [2]
Reakce poskytující LiCN:
- Li + R-CN → LiCN
- Li + HCN (Benzen) → LiCN
Příprava sloučenin s kyanoskupinou
[editovat | editovat zdroj]- RX + LiCN —THF→ RCN
Kyanid lithný se poměrně často využívá jako reakční činidlo pro přípravu sloučenin s kyanoskupinou v molekule, například kyanohalogenidů.[3]
Vliv na životní prostředí
[editovat | editovat zdroj]Kyanid lithný se bez zásahu člověka sám v přírodě vůbec nevyskytuje. Nejčastějším zdrojem výskytu LiCN v přírodě mohou být lithiové baterie (články). Zvláště baterie typu lithium – oxid siřitý mohou být zdrojem LiCN po vzájemné reakci kovového lithia s acetonitrilem, který se v článku nachází. Po kontaktu s kyselými sloučeninami pak dojde ke vzniku vysoce toxického kyanovodíku. Agentura pro ochranu životního prostředí a Ministerstvo obrany Spojených států amerických proto řadí baterie lithium – oxid siřičitý mezi nebezpečný odpad.[4][5]
Reference
[editovat | editovat zdroj]- ↑ a b Lithium cyanide. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ a b Cyanides. onlinelibrary.wiley.com. E. I. du Pont de Nemours & Co., Inc.. Dostupné online [cit. 2012-11-02].
- ↑ Non-aqueous cyanation of halides using lithium cyanide. www.sciencedirect.com. Elsevier. Dostupné online [cit. 2012-10-17].
- ↑ Evaluation of Lithium Sulfur Dioxide Batteries. www.bariumchemicals.com. U.S. Army Communications - Electronics Command and U.S. Army Electronics Research and Development Command. Dostupné v archivu pořízeném dne 2016-03-06.
- ↑ Regulatory status of spent and/or discarded lithium-sulfur dioxide (Li/S02) batteries. yosemite.epa.gov. United States Environmental Protection Agency, 7 March 1984. Dostupné online [cit. 2012-10-23].
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu Kyanid lithný na Wikimedia Commons
Obrázky, zvuky či videa k tématu Kyanid lithný na Wikimedia Commons



