Kyanamid
| Kyanamid | |
|---|---|
 Rezonanční struktury kyanamidu | |
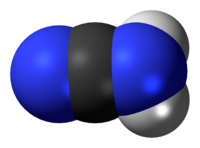 Model molekuly | |
| Obecné | |
| Systematický název | kyanamid |
| Ostatní názvy | karbamonitril |
| Funkční vzorec | NH2CN |
| Sumární vzorec | CN2H2 |
| Vzhled | bezbarvé krystaly[1] |
| Identifikace | |
| Registrační číslo CAS | 420-04-2 |
| EC-no (EINECS/ELINCS/NLP) | 205-861-8 |
| PubChem | 9864 |
| ChEBI | 16698 |
| SMILES | C(#N)N |
| InChI | 1S/CH2N2/c2-1-3/h2H2 |
| Vlastnosti | |
| Molární hmotnost | 42,040 g/mol |
| Teplota tání | 44 °C (317 K)[1] |
| Teplota varu | 83 °C (356 K) (67 Pa) 140 °C (413 K) (2,5 kPa)[1] |
| Teplota rozkladu | 260 °C (533 K)[1] |
| Hustota | 1,282 g/cm3 (20 °C)[1] |
| Index lomu | 1,4418 (48 °C)[1] |
| Disociační konstanta pKa | 10,3[1] |
| Rozpustnost ve vodě | 85 g/100 ml (25 °C) neomezeně rozpustný (43 °C)[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustný v acetonu, butanonu, ethylacetátu, ethanolu, chloroformu[1] |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v sirouhlíku, nerozpustný v benzenu a cyklohexanu[1] |
| Tlak páry | 0,5 Pa (20 °C)[1] |
| Ionizační energie | 10,65 eV |
| Termodynamické vlastnosti | |
| Standardní molární spalná entalpie ΔH°sp | -739 kJ/mol[1] |
| Entalpie varu ΔHv | 1,63 KJ/g[1] |
| Bezpečnost | |
| [1] | |
| H-věty | H261 H302 H315 H317 H318 H335 H412[1] |
| P-věty | P201 P202 P261 P264 P270 P271 P273 P280 P281 P301+310 P302+352 P304+340 P305+351+338 P308+313 P311 P312 P321 P322 P330 P332+313 P337+313 P361 P362 P363 P391 P403+233 P405 P501[1] |
| Teplota vzplanutí | 141 °C (414 K)[1] |
Některá data mohou pocházet z datové položky. | |
Kyanamid je organická sloučenina se vzorcem CN2H2. Používá se na výrobu léčiv a dalších organických látek.
Jako kyanamidy se označují také deriváty této sloučeniny, například kyanamid vápenatý (CaCN2).[2]
Tautomery a autokondenzace[editovat | editovat zdroj]
Protože obsahuje nukleofilní i elektrofilní funkční skupiny, tak kyanamid vstupuje do řady reakcí se sebou samotným. Vytváří dva tautomery, jeden odpovídající vzorci N≡C–NH2 a druhý se vzorcem HN=C=NH (karbodiimid). Převažujícím tautomerem je N≡C–NH2, ale do několika reakcí (například silylace) se zapojuje diimidová forma.[2]
Kyanamid vytváří dimer nazývaný 2-kyanoguanidin (dikyandiamid). K zabránění dimerizaci nebo zpětné přeměně na monomer lze, za nízkých teplot, použít kyseliny. Cyklický trimer se nazývá melamin.[2]
Výroba[editovat | editovat zdroj]
Kyanamid se vyrábí hydrolýzou kyanamidu vápenatého, získávaného Frankovým–Caroovým procesem z acetylidu vápenatého.[3]
Reakce a použití[editovat | editovat zdroj]
Kyanamid je jednouhlíkatá sloučenina, která může působit jako elektrofil i jako nukleofil. Reaguje se sloučeninami obsahujícími kyselé protony, například s vodou vytváří močovinu, se sulfanem thiomočovinu, a se selanem selenomočovinu:
- H2NCN + H2E → H2NC(E)NH2 (E = O, S, Se)
Obdobně z alkoholů vznikají alkylizomočoviny, z thiolů isothimočoviny, a z aminů guanidiny; tímto způsobem se například vyrábí cimetidin, používaný na léčbu žaludečních vředů. Bifunkcionalitu kyanamidu lze také využít k tvorbě heterocyklických sloučenin, což se využívá při výrobě několika léčiv, jako je aminopyrimidin imatinib, a agrochemikálií amitrolu a hexazinonu. 2-aminoimidazolové struktury, vzniklé reakcemi kyanamidu, mají anthelmintika albendazol, flubendazol, a mebendazol[2] K léčivům vyráběným z kyanamidu patří rovněž tirapazamin, etravirin, revaprazan, a dasantafil.
Kyanamidový anion se chová jako pseudochalkogen, kyanamid tak může být považován za analog vody či sulfanu.
Dobrým postupem přípravy sekundárních aminů, ve kterých nejsou obsaženy příměsi primárních nebo terciárních aminů, jsou reakce kyanamidu a alkylhalogenidů za vzniku N,N-dialkylkyanamidů, které lze snadno hydrolyzovat na dialkylaminy a následně dekarboxylovat.[4]
Za přítomnosti N-bromsukcinimidu se kyanamid navazuje na dvojné vazby alkenů. Produkty lze působením zásady přeměnit na N-kyanaziridiny[5] a cyklizovat na imidazoliny, které mohou dále reagovat za tvorby vicinálních diaminů štěpením v zásaditém prostředí.[6]
Kyanamid je vhodný i na přípravu heterocyklických sloučenin: reakcí s 1,2-diaminobenzenem tvoří 2-aminobenzimidazol,[7] spolu s ním vzniká cyklický enamin 4-(cyklohex-1-enyl)morfolin,[8] a také síra a 2-aminothiazol.[9]
Dikyanamid sodný lze získat, s dobrou výtěžností a ve vysoké čistotě, z kyanamidu a chlorkyanu,[10][11] a následně použít na výrobu léčiv.[12]
Při výrobě kreatinu se vytváří guanidinová skupina reakcí kyanamidu se sarkosinem.:[13].

Tímto způsobem se lze vyhnout tvorbě nečistot jako jsou kyselina chloroctová, kyselina iminodioctová, a dihydrotriazin, vznikajících při jiných postupech. Obdobně je možné vytvořit guanidinoacetát reakcí kyanamidu a glycinu.
Zemědělská využití[editovat | editovat zdroj]
Kyanamid se používá ke stimulaci jednotného otevírání pupenů, vedoucí k časnějšímu rašení listů a rychlejšímu kvetení.
50% vodný roztok kyanamidu se také používá jako dezinfekční prostředek při chovu prasat, protože účinně ničí bakterie rodů salmonella a shigella a likviduje mouchy ve všech fázích vývoje.[14]
Vliv na životní prostředí[editovat | editovat zdroj]
Kyanamid se působením vody rozkládá na močovinu. Houby, například Myrothecium verrucaria, tento rozklad urychlují enzymem nazvaným kyanamidhydratáza.[15]
Kyanamidová funkční skupina[editovat | editovat zdroj]
Jako kyanamidy se označují sloučeniny obsahující kyanamidovou funkční skupinu, R1R2N-C≡N, kde R1 a R2 může být řada různých skupin. Příkladem může být naftylkyanamid, C10H7N(CH3)CN, vytvářený von Braunovou reakcí,[16] kdy se přeměňují terciární aminy na kyanamidy působením bromkyanu. Kyanamidy, u kterých jsou skupiny R1 a R2 stejné alkyly, se často připravují přímými alkylacemi solí kyanamidů.[10]
Ve vesmírném prostoru[editovat | editovat zdroj]
Kyanamid byl detekován v mikrovlnném emisním spektru molekulárního mračna Sgr B2 jako první v mězihvězdném prostoru nalezená molekula obsahující vazby NCN.[17]
Bezpečnost[editovat | editovat zdroj]
Kyanamid je mírně toxický.[18] U lidí pracujících s kyanamidem a vystavených této látce byly zaznamenány podráždění dýchací soustavy, kontaktní dermatitida, bolest hlavy, nevolnost, zvracení, nebo průjem.[18]
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku Cyanamide na anglické Wikipedii.
- ↑ a b c d e f g h i j k l m n o p q https://pubchem.ncbi.nlm.nih.gov/compound/9864
- ↑ a b c d Ullmann's Encyclopedia of Industrial Chemistry. Příprava vydání Wiley-VCH. 1. vyd. [s.l.]: Wiley Dostupné online. ISBN 978-3-527-30385-4, ISBN 978-3-527-30673-2. DOI 10.1002/14356007.a08_139.pub2. (anglicky) DOI: 10.1002/14356007.
- ↑ Frederick Kurzer; Alexander Lawson. Methylisourea Hydrochloride. Organic Syntheses. 1954, s. 67. DOI 10.15227/orgsyn.034.0067.
- ↑ A. Jonczyk; Z. Ochal; M. Makosza. Reactions of Organic Anions; LXXXV1. Catalytic Two-Phase Alkylation of Cyanamide. Synthesis. 1978, s. 882–883. DOI 10.1055/s-1978-24922.
- ↑ K. Ponsold; W. Ihn. Die Addition von cyanamid und Halogen an Olefine ein neues Verfahren zur Darstellung von vic.-Halogencyanaminen und Aziridinen. Tetrahedron Letters. 1970, s. 1125–1128. DOI 10.1016/S0040-4039(01)97925-0. PMID 5439242.
- ↑ Harold Kohn; Sang Hun Jung. New stereoselective method for the preparation of vicinal diamines from olefins and cyanamide. Journal of the American Chemical Society. 1983, s. 4106–4108. DOI 10.1021/ja00350a068.
- ↑ Stefan Weiss; Horst Michaud; Horst Prietzel; Helmut Krommer. A New, Simple Synthesis of 2-Aminobenzimidazole. Angewandte Chemie International Edition in English. 1973, s. 841. DOI 10.1002/anie.197308411.
- ↑ S. HÜNIG, E. LÜCKE, W. BRENNINGER. 1-Morpholino-1-Cyclohexene. Org. Synth.. 1961, s. 65. DOI 10.15227/orgsyn.041.0065.
- ↑ K. Gewald; H. Spies; R. Mayer. Zur Reaktion von Enaminen mit Schwefel und Cyanamid. Journal für praktische Chemie. 1970, s. 776–779. DOI 10.1002/prac.19703120507.
- ↑ a b E. B. Vliet. Diallylcyanamide. Organic Syntheses. 1925, s. 45. DOI 10.15227/orgsyn.005.0045.
- ↑ Verfahren zur Herstellung von Natrium-Dicyanamid, veröffentlicht am 10. August 2000, Anmelder: SKW Trostberg AG
- ↑ Sodium dicyanamide (Na-dicyanamide) [online]. [cit. 2019-07-01]. Dostupné v archivu pořízeném z originálu dne 2013-05-23.
- ↑ Deutsche Offenlegungsschrift DE-OS 10 2006 016 227 A1, Offenlegungsdatum: 11. Oktober 2007, Anmelder: Degussa GmbH
- ↑ ALZOGUR [online]. [cit. 2019-07-01]. Dostupné online.
- ↑ H. Stransky; A. Amberger. Isolierung und eigenschaften einer Cyanamid-hydratase (E.C.-Gruppe 4. 2.1.) aus Myrothecium verrucaria Alb. u. Schw.. Zeitschrift für Pflanzenphysiologie. 1973, s. 74-87. DOI 10.1016/S0044-328X(73)80049-2.
- ↑ Homer W. J. Cressman. N-Methyl-1-Naphthylcyanamide. Organic Syntheses. 1947, s. 56. DOI 10.15227/orgsyn.027.0056.
- ↑ B. E. Turner; H. S. Liszt; N. Kaifu; A. G. Kisliakov. Microwave detection of interstellar cyanamide. The Astrophysical Journal. 1975, s. L149. DOI 10.1086/181963. Bibcode 1975ApJ...201L.149T.
- ↑ a b L. Schep; W. Temple; M. Beasley. The adverse effects of hydrogen cyanamide on human health: an evaluation of inquiries to the New Zealand National Poisons Centre. Clinical Toxicology. 2009, s. 58-60. DOI 10.1080/15563650802459254. PMID 18951270.
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu kyanamid na Wikimedia Commons
Obrázky, zvuky či videa k tématu kyanamid na Wikimedia Commons



