Kyselina ftalová: Porovnání verzí
m Úprava parametrů infoboxu |
předělání odkazů |
||
| Řádek 17: | Řádek 17: | ||
|teplota tání=210 °C |
|teplota tání=210 °C |
||
|hustota=1,593 g/cm³ |
|hustota=1,593 g/cm³ |
||
|pKa=pK<sub>a1</sub> |
|pKa=pK<sub>a1</sub>=2,943 pK<sub>a2</sub> = 5,432 |
||
|rozpustnost=málo rozpustná |
|rozpustnost=málo rozpustná |
||
|rozpustnost nepolární=rozpustná |
|rozpustnost nepolární=rozpustná |
||
}} |
}} |
||
'''Kyselina ftalová''' je [[ |
'''Kyselina ftalová''' je [[aromaticita|aromatická]] [[dikarboxylová kyselina|dikarboxylová]] [[kyseliny|kyselina]]. Racionální vzorec je C<sub>6</sub>H<sub>4</sub>(COOH)<sub>2</sub> a jedná se o bílou [[krystal]]ickou látku. Patří do skupiny [[ftalové kyseliny|ftalových kyselin]] a jejími [[izomerie|izomery]] jsou kyseliny [[kyselina isoftalová|isoftalová]] a [[kyselina tereftalová|tereftalová]]. |
||
== Využití == |
== Využití == |
||
| Řádek 28: | Řádek 28: | ||
== Historie == |
== Historie == |
||
''Kyselina ftalová'' byla poprvé vyrobena v |
''Kyselina ftalová'' byla poprvé vyrobena v roce [[1836]] [[Francie|francouzským]] [[chemik]]em [[August Lauren|Augustem Laurenem]] [[oxidace|oxidací]] [[naftalen]]u, který ve víře, že se jedná o kyselinu odvozenou od naftalenu, ji pojmenoval kyselina naftalenová. První, kdo objevil strukturu ''ftalové kyseliny'' byl [[Švýcarsko|Švýcar]] [[Jean Charles Galissard de Marignac]], který ''kyselině ftalové'' dal její správné jméno. |
||
== Chemie == |
== Chemie == |
||
''Kyselina ftalová'' se průmyslově vyrábí oxidací a následnou [[hydrolýza|hydrolýzou]] naftalenu nebo oxidací [[ |
''Kyselina ftalová'' se průmyslově vyrábí oxidací a následnou [[hydrolýza|hydrolýzou]] naftalenu nebo oxidací [[xylen|''o''-xylenu]] vzdušným [[kyslík]]em |
||
[[Soubor:Rce Naftalen na kyselina ftalova.PNG]]<br /><br /> |
[[Soubor:Rce Naftalen na kyselina ftalova.PNG]]<br /><br /> |
||
Zahříváním kyseliny ftalové se uvolňuje [[voda]] a vzniká její [[anhydrid]] - [[ftalanhydrid]]. Kyselina i její anhydrid se používají k |
Zahříváním kyseliny ftalové se uvolňuje [[voda]] a vzniká její [[anhydrid]] - [[ftalanhydrid]]. Kyselina i její anhydrid se používají k výrobě barevných [[indikátor]]ů (fenolftalein). |
||
== Související články == |
== Související články == |
||
Verze z 28. 12. 2015, 12:46
| Kyselina ftalová | |
|---|---|
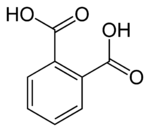 Strukturní vzorec | |
 Prostorový model | |
| Obecné | |
| Systematický název | kyselina benzen-1,2-dikarboxylová |
| Triviální název | kyselina ftalová |
| Anglický název | phthalic acid |
| Funkční vzorec | C6H4(COOH)2 |
| Sumární vzorec | C8H6O4 |
| Vzhled | bezbarvá krystalická látka |
| Identifikace | |
| Registrační číslo CAS | 88-99-3 |
| Vlastnosti | |
| Molární hmotnost | 166,14 g/mol |
| Teplota tání | 210 °C |
| Hustota | 1,593 g/cm³ |
| Disociační konstanta pKa | pKa1=2,943 pKa2 = 5,432 |
| Rozpustnost ve vodě | málo rozpustná |
| Rozpustnost v nepolárních rozpouštědlech | rozpustná |
Některá data mohou pocházet z datové položky. | |
Kyselina ftalová je aromatická dikarboxylová kyselina. Racionální vzorec je C6H4(COOH)2 a jedná se o bílou krystalickou látku. Patří do skupiny ftalových kyselin a jejími izomery jsou kyseliny isoftalová a tereftalová.
Využití
Kyselina ftalová se v chemickém průmyslu používá k výrobě barviv (např. fenolftaleinu), ftalátů, sacharinu a k výrobě syntetických voňavek.
Historie
Kyselina ftalová byla poprvé vyrobena v roce 1836 francouzským chemikem Augustem Laurenem oxidací naftalenu, který ve víře, že se jedná o kyselinu odvozenou od naftalenu, ji pojmenoval kyselina naftalenová. První, kdo objevil strukturu ftalové kyseliny byl Švýcar Jean Charles Galissard de Marignac, který kyselině ftalové dal její správné jméno.
Chemie
Kyselina ftalová se průmyslově vyrábí oxidací a následnou hydrolýzou naftalenu nebo oxidací o-xylenu vzdušným kyslíkem
Zahříváním kyseliny ftalové se uvolňuje voda a vzniká její anhydrid - ftalanhydrid. Kyselina i její anhydrid se používají k výrobě barevných indikátorů (fenolftalein).
