Octan měďnatý
| Octan měďnatý | |
|---|---|
 Vzhled | |
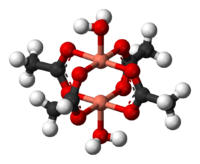 Molekula dihydrátu | |
| Obecné | |
| Systematický název | ethanoát měďnatý |
| Anglický název | copper(II) acetate |
| Sumární vzorec | Cu(CH3COO)2 |
| Identifikace | |
| Registrační číslo CAS | 142-71-2 6046-93-1 (monohydrát) |
| Vlastnosti | |
| Molární hmotnost | 181,63 g/mol (bezvodý) 199,65 g/mol (monohydrát) |
| Teplota tání | 115 °C, 388 K, 239 °F |
| Teplota varu | 240 °C, 513 K, 464 °F |
| Hustota | 1,88 g/cm³ (pevný) |
| Rozpustnost ve vodě | 6,8 g/100 ml (25 °C)[zdroj?] 20 g/100 ml v horké vodě[zdroj?] |
| Rozpustnost v polárních rozpouštědlech | ethanol, mírně rozpustný v glycerolu a etheru. |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| NFPA 704 |  0
2
0
|
Některá data mohou pocházet z datové položky. | |
Octan měďnatý (též ethanoát měďnatý) je měďnatá sůl kyseliny octové. Jedná se o relativně rozpustnou tmavě modrou látku, které se využívá na výrobu organických sloučenin mědi. Je obsažena i v některých nerostech a je i hlavní látkou jednoho z nich.


Výroba[editovat | editovat zdroj]
Měď, na rozdíl od některých jiných kovů, jako je například železo, nereaguje s kyselinami, jelikož měď je podle Beketovovy řady kovů ušlechtilý kov. Proto je výroba poměrně obtížná.
Průmyslově se vyrábí elektrolýzou octanu vápenatého měděnými elektrodami, roztok se nesmí promíchávat, a nakonec se odsaje roztok octanu měďnatého.
Laboratorně lze tuto látku připravit z kyseliny octové a mědi a peroxidu vodíku.
Případně je možno jej připravit z oxidu měďnatého či uhličitanu měďnatého a kyseliny octové
Reakce[editovat | editovat zdroj]
Octan měďnatý reaguje s peroxidem vodíku, dochází k rozpadu na nerozpustný oxid měďnatý, proto se musí při výrobě za pomocí peroxidu velice přesně měřit a počítat, avšak při případné chybě lze oxid měďnatý zase nechat zreagovat, viz výše.
Octan měďnatý reaguje s uhličitanem sodným a kyselinou acetylsalicylovou (aspirinem) za vzniku acetylsalicylátu měďnatého, což je nerozpustné modré barvivo.
Z octanu měďnatého lze vyrábět i například dusičnan měďnatý, přičemž vzniká i octan draselný, tyto 2 látky se od sebe poměrně těžko oddělují. Reakce probíhá podle rovnice:
Octan měďnatý se používá na výrobu organických sloučenin mědi, a také jako katalyzátor, například umožňuje hoření cukru.
Reference[editovat | editovat zdroj]
- ↑ a b Cupric acetate. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Octan měďnatý na Wikimedia Commons
Obrázky, zvuky či videa k tématu Octan měďnatý na Wikimedia Commons








