Fluorid bismutičný
| Fluorid bismutičný | |
|---|---|
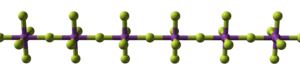
 Krystalová struktura fluoridu bismutičného | |
| Obecné | |
| Systematický název | Fluorid bismutičný |
| Anglický název | Bismuth pentafluoride |
| Německý název | Bismut(V)-fluorid |
| Sumární vzorec | BiF5 |
| Vzhled | bílá krystalická látka |
| Identifikace | |
| Registrační číslo CAS | 7787-62-4 |
| PubChem | 123260 |
| SMILES | [F-].[F-].[F-].[F-].[F-].[Bi+5] |
| InChI | InChI=1S/Bi.5FH/h;5*1H/q+5;;;;;/p-5 |
| Vlastnosti | |
| Molární hmotnost | 303,97 g/mol |
| Teplota tání | 151,4 °C |
| Teplota varu | 230 °C |
| Hustota | 5,40 g/cm3 |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
Některá data mohou pocházet z datové položky. | |
Fluorid bismutičný je anorganická sloučenina s vzorcem BiF5. Je to vysoce reaktivní, bílá pevná látka. Sloučenina je zajímavá pro výzkum, ale zatím nemá praktické využití. Jde o polymerní sloučeninu tvořenou lineárním řetězcem oktaedrů BiF6 spojenými vrcholy.[2][3]
  |
  |
Příprava
[editovat | editovat zdroj]Lze ho připravit reakci fluoridu bismutitého s fluorem za teploty 500 °C.[4]
- BiF3 + F2 → BiF5
Jako fluorační činidlo je možné použít i fluorid chloritý:[5]
- BiF3 + ClF3 → BiF5 + ClF
Reakce
[editovat | editovat zdroj]Fluorid bismutičný je velmi reaktivní a má velmi silné fluorační účinky. S vodou reaguje za vzniku ozonu a difluoridu kyslíku, při teplotě 50 °C dokáže fluorovat parafin a při teplotě 150 °C oxiduje fluorid uraničitý na uranový. Při teplotě 180 °C reaguje s bromem nebo chlorem za vzniku interhalogenů BrF3 a ClF.
Reaguje také s alkalickými fluoridy za vzniku hexafluorobismutičnanů M[BiF6], ty obsahuje oktaedrický anion [BiF6]−.[3]
Odkazy
[editovat | editovat zdroj]Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Bismuth pentafluoride na anglické Wikipedii.
- ↑ a b Bismuth pentafluoride. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ GREENWOOD, NORMAN NEILL. Chemie prvků. Sv. 1.. 1. vyd. vyd. Praha: Informatorium 793 s., 1 příl s. ISBN 8085427389, ISBN 9788085427387. OCLC 320245801 S. 691–697.
- ↑ a b HEBECKER, C. Zur Kristallstruktur von Wismutpentafluorid. Zeitschrift für anorganische und allgemeine Chemie. 1971-8, roč. 384, čís. 2, s. 111–114. Dostupné online [cit. 2019-05-22]. ISSN 0044-2313. DOI 10.1002/zaac.19713840204. (německy)
- ↑ WIBERG, EGON. Inorganic chemistry. 1st English ed.. vyd. San Diego: Academic Press xxxix, 1884 pages s. ISBN 0123526515, ISBN 9780123526519. OCLC 48056955
- ↑ POPOV, A. I.; SCHARABARIN, A. V.; SUKHOVERKHOV, V. F. Synthesis and properties of pentavalent antimony and bismuth fluorides. Zeitschrift für anorganische und allgemeine Chemie. 1989-9, roč. 576, čís. 1, s. 242–254. Dostupné online [cit. 2019-05-22]. ISSN 0044-2313. DOI 10.1002/zaac.19895760128. (německy)
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu Fluorid bismutičný na Wikimedia Commons
Obrázky, zvuky či videa k tématu Fluorid bismutičný na Wikimedia Commons


