Izomerie
Izomerie je vzájemný stav dvou či více sloučenin obsahující stejné atomy ve stejném počtu (mají stejný sumární vzorec), které se od sebe liší pouze strukturním uspořádáním atomů v molekule. Jako izomery jsou označovány sloučeniny vykazující izomerii jakéhokoliv typu.
Základní dělení izomerů je na konstituční (strukturní) izomery a stereoizomery (prostorové nebo též konfigurační izomery). Stereoizomery se dále dělí na enantiomery (zrcadlové obrazy) a diastereoizomery, které se dále dělí na cis-trans diastereoizomery a konformační diastereoizomery (konformery). Izomery mohou a nemusí mít stejné fyzikální a chemické vlastnosti.
Konstituční izomerie (strukturní)[editovat | editovat zdroj]
Konstituční izomery mají stejný sumární vzorec, ale jiné vnitřní uspořádání. Patří sem izomerie
- řetězová – liší se uspořádáním uhlovodíkového řetězce (délka, větvení)
- polohová – liší se umístění násobné vazby (také nazýváno vazebná izomerie) nebo substituentu
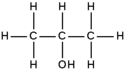
| Buten | Propanol | ||
|---|---|---|---|

|
 |
| |
| but-1-en | but-2-en | propan-1-ol | propan-2-ol |
- funkční nebo skupinová – liší se typem funkční skupiny a mají proto výrazně odlišné chemické i fyzikální vlastnosti

- tautomerie – tautomery jsou dvojice izomerů, které se liší pouze polohou jedné násobné vazby a jednoho atomu vodíku
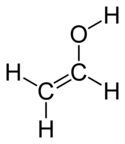
| Ethenol | Ethanal (acetaldehyd) |
|---|---|
 |

|
| enol-forma | keto-forma |
Stereoizomerie[editovat | editovat zdroj]

Stereoizomery mají všechny atomy v molekule vázané stejným způsobem, ale jejich prostorová geometrie je rozdílná. Do této skupiny patří enantiomery, které jsou zrcadlově symetrické a souvisí s optickou aktivitou. Další podskupinou jsou diastereomery, ty se dále dělí na konformační izomery a geometrické izomery. Konformační izomery mohou mezi sebou přecházet pouhou rotací kolem vazby. U geometrických izomerů není umožněna volná otáčivost kvůli násobné vazbě nebo cyklickému uspořádání. Mají rozdílné fyzikální i chemické vlastnosti. Hlavní geometrická izomerie je cis-trans izomerie:
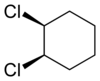
- cis-izomery mají substituenty umístěny ve stejné polorovině vzhledem k násobné vazbě nebo uzavřenému cyklu;
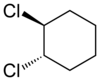
- trans-izomery mají substituenty umístěny v opačných polorovinách vzhledem k násobné vazbě nebo k uzavřenému cyklu, bývají zpravidla stabilnější.
- další používané označení je (Z) =zusammen (ve stejné polorovině) a (E) =entgegen (v opačných polorovinách)
|
|

|

|
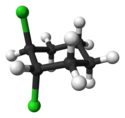
| cis-1,2-dichlorcyklohexan | trans-1,2-dichlorcyklohexan | (Z)-but-2-en | (E)-but-2-en |
|---|
Historie[editovat | editovat zdroj]
První zmínky o izomerii pocházejí z roku 1825, kdy Friedrich Woehler připravil kyselinu kyanatou a zjistil, že ačkoliv má stejné prvkové složení jako kyselina fulminová, její vlastnosti se liší. Tento poznatek zničil tehdejší představu, že chemické látky mohou mít odlišné vlastnosti pouze tehdy, pokud se liší jejich prvkové složení.
V roce 1849 získal Louis Pasteur krystaly obou enantiomerů kyseliny hroznové. Konformaci jednotlivých enantiomerů zjistil pomocí měření otáčení roviny polarizovaného světla (polarimetrie).
Související články[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu izomerie na Wikimedia Commons
Obrázky, zvuky či videa k tématu izomerie na Wikimedia Commons  Encyklopedické heslo Isomerie v Ottově slovníku naučném ve Wikizdrojích
Encyklopedické heslo Isomerie v Ottově slovníku naučném ve Wikizdrojích Slovníkové heslo izomer ve Wikislovníku
Slovníkové heslo izomer ve Wikislovníku
