Hexanol
| Hexanol | |
|---|---|
| Systematický název | hexan-1-ol |
| Ostatní názvy | hexanol |
| Funkční vzorec | CH3(CH2)5OH |
| Sumární vzorec | C6H14O |
| Vzhled | bezbarvá kapalina (všechny izomery) |
| Identifikace | |
| Registrační číslo CAS | 111-27-3 |
| EC-no (EINECS/ELINCS/NLP) | 203-852-3 |
| PubChem | 8103 |
| SMILES | CCCCCCO |
| InChI | 1S/C6H14O/c1-2-3-4-5-6-7/h7H,2-6H2,1H3 |
| Číslo RTECS | MQ4025000 |
| Vlastnosti | |
| Molární hmotnost | 102,104 465 070 g/mol |
| Teplota tání | −53 až −41 °C (1-hexanol) |
| Teplota varu | 119 až 159 °C (podle izomeru), 155 až 159 °C (1-hexanol) |
| Hustota | 0,831 6 g/cm3 (1-hexanol) |
| Rozpustnost ve vodě | 0,59 g/100 ml (20 °C) |
| Rozpustnost v polárních rozpouštědlech | mísitelný s ethanolem a etherem |
| Bezpečnost | |
| [1] Varování[1] | |
| H-věty | H302 |
| R-věty | R22 |
| S-věty | S2, S24/25 |
| NFPA 704 |  2
1
0
|
| Teplota vzplanutí | 59 °C (1-hexanol) |
| Teplota vznícení | 293 °C (1-hexanol) |
Některá data mohou pocházet z datové položky. | |
Hexanol (CH3(CH2)5OH, sumární vzorec C6H14O) je organická sloučenina, alkohol, šestý člen homologické řady alkanolů (alkoholů odvozených od alkanů).
Hexanol má celkem 17 izomerů:
| Struktura | Typ | Systematický název | Teplota varu (°C) |
|---|---|---|---|
| primární | hexan-1-ol | 158 | |
|
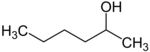
sekundární | hexan-2-ol | 136 |
| sekundární | hexan-3-ol | 135 | |
|
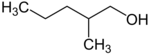
primární | 2-methylpentan-1-ol | 147 |

|
primární | 3-methylpentan-1-ol | 152 |
|
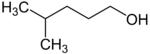
primární | 4-methylpentan-1-ol | 151 |

|
terciární | 2-methylpentan-2-ol | 121 |

|
sekundární | 3-methylpentan-2-ol | 134 |
|
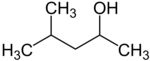
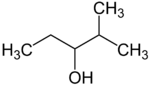
sekundární | 4-methylpentan-2-ol | 131 |
|
sekundární | 2-methylpentan-3-ol | 126 |

|
terciární | 3-methylpentan-3-ol | 122 |

|
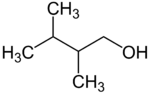
primární | 2,2-dimethylbutan-1-ol | 137 |
|
primární | 2,3-dimethylbutan-1-ol | 145 |

|
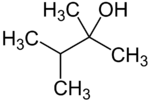
primární | 3,3-dimethylbutan-1-ol | 143 |
|
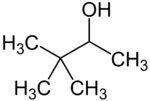
terciární | 2,3-dimethylbutan-2-ol | 119 |
|
sekundární | 3,3-dimethylbutan-2-ol | 120 |

|
primární | 2-ethylbutan-1-ol | 146 |
Příprava[editovat | editovat zdroj]
Průmyslově se hexanol vyrábí oligomerizací ethylenu za použití triethylhliníku[2]:
Al(C2H5)3 + 6 C2H4 → Al(C6H13)3
2 Al(C6H13)3 + 3 O2 + 6 H2O → 6 HOC6H13 + Al(OH)3.
Tento proces vytváří mnoho oligomerů, které se dají oddělit destilací.
Alternativní metody[editovat | editovat zdroj]
Další metodou přípravy hexanolu má za následek hydroformylaci pentenu následovanou hydrogenací aldehydů. Tato metoda je používána v průmyslu k výrobě směsi izomerů, které jsou prekurzory plastifikátorů.
Hexen může být převeden na hexanol (Katalyzátory jsou diboran v tetrahydrofuranu, peroxid vodíku a hydroxid sodný):
Tato metoda se používá v laboratorní syntéze, ovšem nikoliv v praxi.
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku 1-Hexanol na anglické Wikipedii.
- ↑ a b 1-Hexanol. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ FALBE, Jürgen; BAHRMANN, Helmut; LIPPS, Wolfgang; MAYER, Dieter. Alcohols, Aliphatic. [s.l.]: [s.n.] DOI 10.1002/14356007.a01_279.
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Hexanol na Wikimedia Commons
Obrázky, zvuky či videa k tématu Hexanol na Wikimedia Commons



