Karboanion

Karboanion, také karbanion, je anion, ve kterém je třívazný uhlík a má formální záporný náboj alespoň v jedné rezonanční struktuře.[1] Karbanionty nemají π delokalizaci a jejich molekuly zaujímají tvar čtyřstěnu, pokřivenou či lineární strukturu, kde je karbaniontový uhlík navázán na tři (například methylový anion), dva (např. fenylový anion) nebo jeden (např. acetylidový anion) substituent. Karbanion je formálně konjugovanou zásadou karbonové kyseliny:
- R3C-H + B− → R3C− + H-B
kde B označuje zásadu. Karbanionty patří mezi reaktivní meziprodukty v organické chemii. V organické syntéze jsou organolithná a Grignardova činidla často považována za karbanionty, což je vhodné přiblížení, ovšem tyto látky téměř vždy tvoří vícejaderné částice s polárními kovalentními vazbami namísto karbaniontů.
Vlastnosti a příklady výskytu[editovat | editovat zdroj]
Karbanionty jsou obvykle nukleofilní a zásadité. Míra této nukleofility a zásaditosti je ovlivněna substituenty na uhlíku; vliv mají zejména:
- Indukční efekt – elektronegativní atomy v sousedství náboje jej stabilizují.
- Rozsah konjugace aniontu. Rezonanční efekty mohou anion stabilizovat, což se nejčastěji děje, když je anion stabilizován působením aromaticity.
Geometrie molekul také ovlivňuje hybridizaci orbitalů aniontu. Čím silnější je s-charakter nabitého atomu, tím je anion stabilnější.
Organokovová činidla jako je butyllithium (v hexamerním uspořádání, [BuLi]6) nebo methylmagnesiumbromid (etherový komplex, MeMg(Br)(OEt2)2) jsou často označována jako „karbanionty“. Ve skutečnosti však jde o shluky nebo komplexy s kovalentní vazbou, i když je jejich elektronová hustota značně polarizována směrem k uhlíkovému atomu. Methylový anion a jeho vlastnosti byly zkoumány v plynném skupenství. Jeho elektronová aktivita má však hodnotu –2 až –8 kcal/mol, takže se v plynném skupenství rozkládá uvolněním elektronu a čistou „sůl“ iontu CH3– prakticky nelze izolovat.[2] V kondenzované fázi mohou být takto izolovány pouze karbanionty, které jsou dostatečně stabilizovány delokalizací. Roku 1984 byla představena sůl crown-etheru lithia a trifenylmethanidového aniontu složená z trifenylmethanu, n-butyllithia a 12-crown-4 (který tvoří stabilní komplex s lithnými kationty), jež je stabilní při nízkých teplotách.[3]

Přidáním n-butyllithia k roztoku trifenylmethanu (pKaDMSO(CHPh3) = 30,6) v THF za nízké teploty a následným přidáním 12-crown-4 vzniká červený roztok a při -20 °C se vysráží komplex [Li(12-crown-4)]+[CPh3]–. Délka centrálních vazeb C-C je 145 pm s fenylovým kruhem odkloněným průměrně o 31,2°. Je rovněž známa krystalová struktura podobného difenylmethanidového iontu ([Li(12-crown-4)]+[CHPh2]–), připraveného z difenylmethanu (pKaDMSO(CH2Ph2) = 32,3). Pokus o izolaci komplexu s benzylovým aniontem [CH2Ph]– získaným z toluenu (pKaDMSO(CH3Ph) ~ 43) byl kvůli prudké reakci s vytvořeným aniontem neúspěšný.[4]
V letech 1904[5] a 1917[6] Wilhelm Schlenk připravil dvě různé červeně zbarvené soli, jejichž vzorce byly [NMe4]+[CPh3]– a [NMe4]+[CH2Ph]– reakcí odpovídajících organosodných činidel s tetramethylamoniumchloridem. Jelikož tetramethylamoniové kationty nemohou tvořit chemickou vazbu s karbaniontovým centrem, předpokládá se, že tyto látky obsahují volné karbanionty. Když byla struktura první z nich o téměř století později ověřena rentgenovou krystalografií,[7] bylo zjištěno, že druhá je tak nestabilní, že její strukturu nelze určit. Byla popsána reakce předpokládané „[NMe4]+[CH2Ph]–“ s vodou za vzniku toluenu a tetramethylammoniumhydroxidu a zjištěno, že Schlenk skutečně připravil sůl benzylového aniontu.
Detekce[editovat | editovat zdroj]
Karbanionty přítomné v roztoku lze mimo jiné určit pomocí protonové NMR.[8] Ve spektru cyklopentadienu v DMSO jsou patrné čtyři vinylové protony na 6,5 ppm a dva methylenové můstky na 3 ppm, zatímco cyklopentadienylový anion má jedinou rezonanci na 5,50 ppm. Použitím 6Li a 7Li NMR lze získat údaje o struktuře a reaktivitě řady organolithných sloučenin.
Karbonové kyseliny[editovat | editovat zdroj]
V podstatě každá sloučenina obsahující vodík se může deprotonací přeměnit na svou konjugovanou zásadu. Sloučenina je karbonovou kyselinou, pokud se při deprotonaci odštěpí proton z uhlíkového atomu. Ve srovnání s látkami obvykle považovanými za kyseliny (například kyselinou dusičnou nebo karboxylovými kyselinami) jsou takovéto kyseliny až na výjimky mnohem slabší. Příkladem může být benzen, jenž podle Arrheniovy teorie není kyselinou, jelikož jsou jeho vodné roztoky neutrální. Podle Brønstedovy–Lowryho teorie jde však o velmi slabou kyselinu s odhadovanou disociační konstantou ~49, která může projít deprotonací za přítomnosti superzásady jako je například Lochmannova-Schlosserova zásada. Při vzniku dvojice konjugovaná zásada-kyselina faktory, které ovlivňují relativní stabilitu karboaniontů také ovlivňují hodnoty pKa odpovídajících karbonových kyselin; navíc hodnoty pKa umožňují předpovídat, zda přesun protonu bude termodynamicky výhodný: pokud má být deprotonace kyseliny HA zásadou B− termodynamicky výhodná (K > 1), musí platit vztah pKa(BH) > pKa(AH).
Níže uvedené hodnoty pKa byly určeny v DMSO, jenž má širší použitelné rozmezí (~0 až ~35) než voda (~0 až ~15) a lépe zobrazuje zásaditost karbaniontů v obvyklých organických rozpouštědlech. Hodnoty menší než 0 nebo větší než 35 byly získány nepřímým odhadem; jejich přesnost je ovšem omezená. pKa ve vodných roztocích jsou často uváděna v literatuře, hlavně v souvislosti s biochemií a enzymologií. pKa ve vodě a organických rozpouštědlech se často výrazně liší, pokud je anion schopen vodíkové vazby; například pKaaq(H2O) = 15,7, zatímco pKaDMSO(H2O) = 31,4,[9] což odráží rozdílnou schopnost vody a DMSO stabilizovat hydroxidový anion. U cyklopentadienu jsou pKa v obou případech podobné: pKaaq(Cp-H) = 15, zatímco pKaDMSO(Cp-H) = 18.[9]
| název | vzorec | strukturní vzorec | pKaDMSO |
|---|---|---|---|
| Cyklopentan | C5H10 | ~ 59 | |
| Methan | CH4 | 
|
~ 56 |
| Benzen | C6H6 | ~ 49[10] | |
| Propen | C3H6 | ~ 44 | |
| Toluen | C6H5CH3 | ~ 43 | |
| Amoniak (N-H) | NH3 | 
|
~ 41 |
| Dithian | C4H8S2 | 
|
~ 39 |
| Dimethylsulfoxid | (CH3)2SO | 
|
35,1 |
| Difenylmethan | C13H12 | 
|
32,3 |
| Acetonitril | CH3CN | 31.3 | |
| Anilin (N-H) | C6H5NH2 | 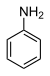
|
30,6 |
| Trifenylmethan | C19H16 | 
|
30,6 |
| Fluoroform | CHF3 | 
|
30,5 |
| Xanthen | C13H10O | 
|
30,0 |
| Ethanol (O-H) | C2H5OH | 29,8 | |
| Fenylacetylen | C8H6 | 
|
28,8 |
| Thioxanthen | C13H10S | 28,6 | |
| Aceton | C3H6O | 
|
26,5 |
| Benzoxazol | C7H5NO | 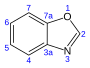
|
24,4 |
| Fluoren | C13H10 | 22,6 | |
| Inden | C9H8 | 20,1 | |
| Cyklopentadien | C5H6 | 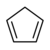
|
18,0 |
| Nitromethan | CH3NO2 | 17,2 | |
| Diethylmalonát | C7H12O4 | 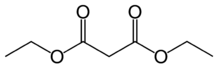
|
16,4 |
| Acetylaceton | C5H8O2 | 13,3 | |
| Kyanovodík | HCN | 12.9 | |
| Kyselina octová (O-H) | CH3COOH | 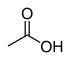
|
12,6 |
| Malononitril | C3H2N2 | 
|
11,1 |
| Dimedon | C8H12O2 | 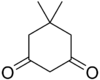
|
10,3 |
| Meldrumova kyselina | C6H8O4 | 
|
7,3 |
| Chlorovodík (Cl-H) | HCl | HCl (g) | –2,0[11] |
| Kyselina triflidová | HC(SO2CF3)3 | ~ –16[12] |
Kyselina octová, amoniak, anilin, ethanol a chlorovodík nejsou karbonové kyseliny, jsou zde uvedeny pouze jako běžné kyseliny pro srovnání.
Chirální karbanionty[editovat | editovat zdroj]
Když je geometrie molekul karbaniontů popisována jako čtyřstěnná, je otázkou, zda mohou vykazovat chiralitu, protože je aktivační bariéra pro změnu této geometrie velmi nízká a tak každý pokus o vytvoření chirality skončí racemizací. Existují však důkazy, že karbanionty mohou být chirální, což se ukázalo například při výzkumu organolithných sloučenin.
První důkazy o existenci chirálních organolithných sloučenin byly získány v roce 1950. Reakcí chirálního 2-jodoktanu se sec-butyllithiem v petroletheru při −70 °C následovanou reakcí se suchým ledem vznikla převážně racemická kyselina 2-methylmáselná ale také menší množství opticky aktivní kyseliny 2-methyloktanové, která se mohla vytvořit jen z rovněž opticky aktivního 2-methylheptyllithia s uhlíkovým atomem navázaným na lithium, který tvoří karbanion.[13]

Při zahřátí směsi na 0 °C optická aktivita zmizela.
Další důkazy byly nalezeny v 60. letech 20. století. Reakcí cis izomeru 2-methylcyklopropylbromidu se sec-butyllithiem a následné karboxylaci suchým ledem vznikla kyselina cis-2-methylcyklopropylkarboxylová. Tvorba trans izomeru by naznačovala, že karbaniontový meziprodukt je nestabilní.[14]

Obdobně reakcí (+)-(S)-l-brom-l-methyl-2,2-difenylcyklopropanu s n-butyllithiem ukončenou methanolem vznikl produkt se zadrženou konfigurací:[15]

Byly též připraveny chirální sloučeniny methyllithia:[16]
![Chirální -oxy-[2H1]methyllithné sloučeniny, Bu zastupuje butyl, i-Pr zastupuje isopropyl](http://upload.wikimedia.org/wikipedia/commons/thumb/1/1d/PhosphatePhosphonateRearrangement.png/500px-PhosphatePhosphonateRearrangement.png)
Organofosfátová sloučenina 1 obsahuje chirální skupinu s vodíkovým a deuteriovým substituentem. Stannylová skupina je nahrazena lithiem za vzniku meziproduktu 2, u něhož proběhne fosfátový-fosforanový přesmyk na fosforanový derivát 3, jenž reakcí s kyselinou octovou vytváří alkohol 4. V rozmezí teplot −78 °C až 0 °C je chiralita zachována v reakční posloupnosti.[17]
Historie[editovat | editovat zdroj]
První reakční mechanimus zahrnující vznik karbaniontu (šlo o mechanismus benzoinové kondenzace) popsali v roce 1907 Clarke a Arthur Lapworth[18] O tři roky dříve připravil Wilhelm Schlenk Ph3C−NMe4+ z tetramethylamoniumchloridu a Ph3CNa.[5] a roku 1914 ukázal, jak mohou být triarylmethylové radikály redukovány na karbanionty alkalickými kovy.[19] Název karbanion použili poprvé roku 1933 Wallis a Adams jako označení záporně nabitého protějšku ke karboniovému iontu.[20][21]
Odkazy[editovat | editovat zdroj]
Související články[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu karboanion na Wikimedia Commons
Obrázky, zvuky či videa k tématu karboanion na Wikimedia Commons
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku Carbanion na anglické Wikipedii.
- ↑ IUPAC Gold Book - carbanion [online]. [cit. 2016-07-30]. Dostupné online.
- ↑ MARYNICK, Dennis S.; DIXON, David A. Electron Affinity of the Methyl Radical: Structures of CH3 and CH3 -. Proceedings of the National Academy of Sciences of the United States of America. 1977, s. 410–413. Dostupné online. DOI 10.1073/pnas.74.2.410.
- ↑ The isolation and X-ray structures of lithium crown ether salts of the free phenyl carbanions [CHPh2]- and [CPh3]- Marilyn M. Olmstead, Philip P. Power; J. Am. Chem. Soc.; 1985; 107(7); 2174-2175. DOI:10.1021/ja00293a059
- ↑ HARDER, S. Schlenk's Early "Free" Carbanions. Chemistry: A European Journal. 2002, s. 3229–3229. DOI 10.1002/1521-3765(20020715)8:14<3229::AID-CHEM3229>3.0.CO;2-3.
- ↑ a b SCHLENK, W.; WEICKEL, T.; HERZENSTEIN, A. Ueber Triphenylmethyl und Analoga des Triphenylmethyls in der Biphenylreihe. [Zweite Mittheilung über „Triarylmethyle”.]. Justus Liebig's Annalen der Chemie. 1910, s. 1. DOI 10.1002/jlac.19103720102.
- ↑ SCHLENK, W.; HOLTZ, Johanna. Über Benzyl-tetramethyl-ammonium. Berichte der deutschen chemischen Gesellschaft. 1917-01-01, s. 274–275. Dostupné online. ISSN 1099-0682. DOI 10.1002/cber.19170500143. (anglicky)
- ↑ HARDER, Sjoerd. Schlenk's Early "Free" Carbanions. Chemistry – A European Journal. 2002-07-15, s. 3229–3232. Dostupné online. ISSN 1521-3765. DOI 10.1002/1521-3765(20020715)8:143.0.CO;2-3. (anglicky)
- ↑ A Simple and Convenient Method for Generation and NMR Observation of Stable Carbanions. Hamid S. Kasmai Journal of Chemical Education • Vol. 76 No. 6 June 1999
- ↑ a b EVANS, D. A.; RIPIN, D. H. Chem 206 pKa Table [online]. 2005 [cit. 2018-03-07]. Dostupné v archivu pořízeném dne 2018-06-19.
- ↑ BORDWELL, G. F.; MATTHEWS, Walter S. Equilibrium acidities of carbon acids. III. Carbon acids in the membrane series. Journal of the American Chemical Society. 2002-05-01, s. 1216–1217. Dostupné online. DOI 10.1021/ja00811a041. (EN)
- ↑ TRUMMAL, Aleksander; LIPPING, Lauri; KALJURAND, Ivari; KOPPEL, Ilmar A.; LEITO, Ivo. Acidity of Strong Acids in Water and Dimethyl Sulfoxide. The Journal of Physical Chemistry A. 2016-05-06, s. 3663–3669. Dostupné online. DOI 10.1021/acs.jpca.6b02253. Bibcode 2016JPCA..120.3663T. (EN)
- ↑ Hodnota pKa v MeCN je –3,7 (J. Org. Chem. 2011, 76, 391). pKa v DMSO se odhaduje na pKaMeCN = 0,98 × pKaDMSO + 11,6 (J. Org. Chem. 2009, 74, 2679).
- ↑ FORMATION OF OPTICALLY ACTIVE 1-METHYLHEPTYLLITHIUM Robert L. Letsinger J. Am. Chem. Soc.; 1950; 72(10) pp 4842 - 4842; DOI:10.1021/ja01166a538
- ↑ The Configurational Stability of cis- and trans-2-Methylcyclopropyllithium and Some Observations on the Stereochemistry of their Reactions with Bromine and Carbon Dioxide Douglas E. Applequist and Alan H. Peterson J. Am. Chem. Soc.; 1961; 83(4) pp 862 - 865; DOI:10.1021/ja01465a030
- ↑ Cyclopropanes. XV. The Optical Stability of 1-Methyl-2,2-diphenylcyclopropyllithium H. M. Walborsky, F. J. Impastato, and A. E. Young J. Am. Chem. Soc.; 1964; 86(16) pp 3283 - 3288; DOI:10.1021/ja01070a017
- ↑ Preparation of Chiral -Oxy-[2H1]methyllithiums of 99% ee and Determination of Their Configurational Stability Dagmar Kapeller, Roland Barth, Kurt Mereiter, and Friedrich Hammerschmidt J. Am. Chem. Soc.; 2007; 129(4) pp 914 - 923; (Article) DOI:10.1021/ja066183s
- ↑ Enantioselektivita byla určena NMR spektroskopií po derivatizaci Mosherovou kyselinou.
- ↑ CLARKE, R. W. L.; LAPWORTH, A. LXV.?An extension of the benzoin synthesis. Journal of the Chemical Society, Transactions. 1907, s. 694. DOI 10.1039/CT9079100694.
- ↑ SCHLENK, W.; MARCUS, E. Über Metalladditinen an freie organische Radikale. (Über Triarylmethyle. XII.). Berichte der deutschen chemischen Gesellschaft. 1914, s. 1664. DOI 10.1002/cber.19140470256.
- ↑ WALLIS, E. S.; ADAMS, F. H. The Spatial Configuration of the Valences in Tricovalent Carbon Compounds1. Journal of the American Chemical Society. 1933, s. 3838. DOI 10.1021/ja01336a068.
- ↑ TIDWELL, T. T. The first century of physical organic chemistry: A prologue. Pure and Applied Chemistry. 1997, s. 211–214. DOI 10.1351/pac199769020211.
