Oxid xenoničelý
| Oxid xenoničelý | |
|---|---|
 Strukturní vzorec | |
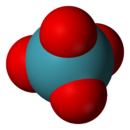 Zobrazení molekuly | |
| Obecné | |
| Systematický název | Oxid xenoničelý |
| Anglický název | Xenon tetroxide |
| Německý název | Xenon(VIII)-oxid |
| Sumární vzorec | XeO4 |
| Vzhled | žlutá pevná látka |
| Identifikace | |
| Registrační číslo CAS | 12340-14-6 |
| Vlastnosti | |
| Molární hmotnost | 195,29 g/mol |
| Teplota tání | −35,9 °C |
| Teplota varu | 0 °C (rozklad) |
| Teplota rozkladu | 0 °C |
| Struktura | |
| Dipólový moment | 0 D |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | 643 kJ/mol |
| Bezpečnost | |
| NFPA 704 |  |
Některá data mohou pocházet z datové položky. | |
Oxid xenoničelý (XeO4) je žlutá, krystalická, silně nestabilní sloučenina vzácného plynu xenonu s kyslíkem. Molekula má tvar tetraedru. Oxid xenoničelý je jedním z pěti známých oxidů s prvkem v nejvyšším oxidačním čísle (ještě jsou známy oxid osmičelý, rutheničelý, iridičelý a hassičelý).
Její explozivní rozklad nastává při teplotě -35,9 °C, který je zároveň její sublimační teplotou a teplotou tání.
Metody přípravy[editovat | editovat zdroj]
Sloučeninu lze připravit například reakcí pevného xenoničelanu barnatého Ba2XeO6 se studenou koncentrovanou kyselinou sírovou za vzniku síranu barnatého, přičemž jako přechodná sloučenina vzniká nejprve kyselina xenoničelá (přesněji tetrahydrogenxenoničelá) H4XeO6, která se okamžitě dále rozpadá podle rovnice:
Další možnou metodou přípravy je disproporcionace xenonanů na xenoničelan a xenon:
- .
Jinou uváděnou reakcí je oxidace xenonanů ozonem:
- .
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Oxid xenoničelý na Wikimedia Commons
Obrázky, zvuky či videa k tématu Oxid xenoničelý na Wikimedia Commons







