Kyselina tetrafluoroboritá
| Kyselina tetrafluoridoboritá | |
|---|---|
 Strukturní vzorec | |
| Obecné | |
| Systematický název | kyselina tetrafluoroboritá |
| Sumární vzorec | HBF4 |
| Vzhled | bezbarvá kapalina[1] |
| Identifikace | |
| Registrační číslo CAS | 16872-11-0 |
| EC-no (EINECS/ELINCS/NLP) | 240-898-3 |
| PubChem | 28118 |
| SMILES | F[B-](F)(F)[FH+] |
| Vlastnosti | |
| Molární hmotnost | 87,81 g/mol |
| Teplota tání | −90 °C (183 K) |
| Teplota varu | 130 °C (403 K)[1] (rozklad) |
| Hustota | 1,8 g/cm3[1] |
| Index lomu | 1,3284 (20% vodný roztok, 20 °C)[1] |
| Disociační konstanta pKa | −4,9[1] |
| Rozpustnost ve vodě | dobře rozpustná[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustná v ethanolu[1] |
| Rozpustnost v nepolárních rozpouštědlech | rozpustná v diethyletheru |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H314[1] |
| P-věty | P260 P264 P280 P301+330+331 P303+361+353 P304+340 P305+351+338 P310 P363 P405 P501[1] |
Některá data mohou pocházet z datové položky. | |
Kyselina tetrafluoridoboritá je anorganická sloučenina, kyselina se vzorcem [H+][BF4−], kde H+ je solvatovaný proton; rozpouštědlem může být téměř jakákoliv Lewisova zásada – například ve vodě se vyskytuje jako tetrafluoridoboritan oxonia, H3OBF4 (i když proton je obvykle solvatován několika molekulami vody a skutečná struktura odpovídá vzorci [H(H2O)n+][BF4−]). Je komerčně dostupná o jako roztok v diethyletheru se strukturou [H(Et2O)n+][BF4−], kde n je nejčastěji 2. Na rozdíl od ostatních silných kyselin, jako jsou H2SO4 a HClO4, není známa ve zcela nesolvatované formě.
Tato kyselina se nejčastěji používá na přípravu tetrafluoridoboritanových solí.[2] Je žíravá a poškozuje kůži. Je dostupná jako roztok ve vodě nebo jiném rozpouštědle, jako je diethylether. Jedná se o silnou kyselinu se slabě koordinující neoxidující konjugovanou zásadou[3], strukturně podobnou kyselině chloristé.
Struktura a výroba
[editovat | editovat zdroj]Čistou HBF4 nelze připravit, protože by u ní došlo k odštěpení fluoridové skupiny protonem za vzniku fluorovodíku a fluoridu boritého
[H+][BF4–] → HF + BF3 (Podobný rozklad se objevuje u superkyselin HPF6 a HSbF6).[4][5]
Roztok BF3 v HF je silně kyselý, při struktuře odpovídající vzorci [H2F+][BF4–] má Hammetovu funkci přibližně –16,6 při 7 molárních procentech BF3, čímž splňuje definici superkyseliny.[6]
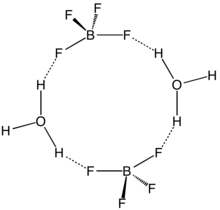
I když nebyla nikdy získána čistá HBF4, tak byly popsány roztoky, ve kterých se nachází v solvatované formě. V těchto roztocích se nacházejí kationty tvořené protonovanými molekulami rozpouštědla, například H3O+ a H5O +
2 , a anionty BF -
4 . Anionty a kationty na sebe působí silnými vodíkovými vazbami.[7]
Vodné roztoky HBF4 se připravují rozpouštěním kyseliny borité ve vodných roztocích kyseliny fluorovodíkové; přitom tři ekvivalenty HF reagují za vzniku fluoridu boritého, který se následně slučuje se čtvrtým ekvivalentem za vzniku tetrafluoroboritanového kationtu.
- B(OH)3 + 4 HF → H3O+ + BF −
4 + 2 H2O
Bezvodé roztoky se připravují z vodných roztoků a acetanhydridu.[8]
Kyselost
[editovat | editovat zdroj]Určení kyselosti kyseliny tetrafluoridoborité je komplikováno skutečností, že kyselina vytváří různé struktury – H(OEt2)+BF −
4 , H3O+BF −
4 a HF.BF3, přičemž kyselost každé z nich je jiná. Hodnota pKa ve vodném roztoku je −0.44.[2] Titrací roztoku NBu +
4 BF −
4 v acetonitrilu vychází pKa 1,6; kyselina tetrafluoridoboritá je tedy podobně silná jako kyselina fluorsírová.[3]
Použití
[editovat | editovat zdroj]Kyselina tetrafluoridoboritá se používá na přípravu tetrafluoridoboritanů, obvykle reakcemi s oxidy kovů. Vzniklé soli slouží jako meziprodukty při výrobě zpomalovačů hoření a při elektrolytické výrobě boru.
Organická chemie
[editovat | editovat zdroj]HBF4 slouží jako katalyzátor alkylačních a polymerizačních reakcí. Roztok kyseliny tetrafluoridoborité v diethyletheru se používá ke katalýze transacetalací a isopropylidenací při navazování chránicích skupin na sacharidy. Acetalové i některé etherové skupiny lze odstranit acetonitrilem.
Z kyseliny borité lze připravit řadu reaktivních kationtů, jako jsou tetrafluoridoboritan tropylia (C7H +
7 BF −
4 ), trifenylmethyltetrafluoridoboritan (Ph3C+BF −
4 ), triethyloxoniumtetrafluoridoborát (Et3O+BF −
4 ) a benzendiazoniumtetrafluoridoborát (PHN +
2 BF −
4 ).
Galvanické pokovování
[editovat | editovat zdroj]Roztoky HBF4 se používají při galvanickém pokovování cínu a jeho slitin, kdy lze také použít kyselinu methansulfonovou.[9]
Odkazy
[editovat | editovat zdroj]Související článek
[editovat | editovat zdroj]Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Fluoroboric acid na anglické Wikipedii.
- ↑ a b c d e f g h i j k Tetrafluoroboric acid. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ a b Gregory K. Friestad, Bruce P. Branchaud "Tetrafluoroboric Acid" E-Eros Encyclopedia of Reagents for Organic Synthesis. DOI:10.1002/047084289X.rt035
- ↑ a b Kütt, A., et al., "Equilibrium Acidities of Superacids", J. Org. Chem. 2010, volume 76, pp. 391-395. DOI:10.1021/jo101409p
- ↑ Mark Juhasz; Stephan Hoffmann; Evgenii Stoyanov; Kee-Chan Kim; Christopher A. Reed. The Strongest Isolable Acid. Angewandte Chemie International Edition. 2004-10-11, s. 5352–5355. ISSN 1433-7851. DOI 10.1126/science.287.5460.2007. PMID 15468064.
- ↑ Christopher A. Reed. Carborane acids. New "strong yet gentle" acids for organic and inorganic chemistry. Chemical Communications. 2005, s. 1669–1677. Dostupné online. ISSN 1359-7345. DOI 10.1039/B415425H. PMID 1579-1275.
- ↑ George Andrew Olah; G. K. Surya Prakash; Jean Sommer; Arpad Molnar. Superacid chemistry. Hoboken: [s.n.], 2009-02-03. ISBN 9780471596684.
- ↑ Mootz, D.; Steffen, M. "Crystal structures of acid hydrates and oxonium salts. XX. Oxonium tetrafluoroborates H3OBF4, [H5O2]BF4, and [H(CH3OH)2]BF4", Zeitschrift für Anorganische und Allgemeine Chemie 1981, vol. 482, pp. 193-200. DOI:10.1002/zaac.19814821124
- ↑ Wudl, F.; Kaplan, M. L., "2,2′-Bi-L,3-Dithiolylidene (Tetrathiafulvalene, TTF) and its Radical Cation Salts" Inorg. Synth. 1979, vol. 19, 27. DOI:10.1002/9780470132500.ch7
- ↑ R. Balaji; Malathy Pushpavanam. Methanesulphonic acid in electroplating related metal finishing industries. Transactions of the Imf. 2003, s. 154–158. DOI 10.1080/00202967.2003.11871526.
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu Kyselina tetrafluorboritá na Wikimedia Commons
Obrázky, zvuky či videa k tématu Kyselina tetrafluorboritá na Wikimedia Commons

