m-kresol
| M-kresol | |
|---|---|
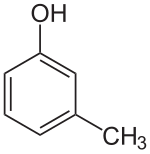 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | 3-methylfenol |
| Ostatní názvy | m-kresol, 3-methylhydroxybenzen |
| Funkční vzorec | C6H4OH-3-CH3 |
| Sumární vzorec | C7H8O |
| Vzhled | bezbarvá kapalina[1] |
| Identifikace | |
| Registrační číslo CAS | 108-39-4 |
| EC-no (EINECS/ELINCS/NLP) | 203-39-4 |
| PubChem | 342 |
| ChEBI | 17231 |
| SMILES | Cc1cc(O)ccc1 |
| InChI | 1/C7H8O/c1-6-3-2-4-7(8)5-6/h2-5,8H,1H3 |
| Číslo RTECS | GGO4Y809LO |
| Vlastnosti | |
| Molární hmotnost | 108,14 g/mol |
| Teplota tání | 11,8 °C (286,0 K)[1] |
| Teplota varu | 202 °C (475 K)[1] |
| Hustota | 1,034 g/cm3 (20 °C)[1] |
| Index lomu | 1,5398 (20 °C)[1] |
| Disociační konstanta pKa | 10,1[1] |
| Rozpustnost ve vodě | 2,27 g/100 ml[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustný v ethanolu, acetonu, glycerolu, zředěných roztocích hydroxidů a v chloroformu[1] |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v tetrachlormethanu, benzenu, diethyletheru a rostlinných olejích[1] |
| Tlak páry | 13 Pa[1] |
| Měrná magnetická susceptibilita | −6,66×105 μm3/g |
| Povrchové napětí | 35,69 mN/m (50 °C)[1] |
| Termodynamické vlastnosti | |
| Standardní molární spalná entalpie ΔH°sp | −3706 kJ/mol[1] |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H301 H311 H314[1] |
| P-věty | P260 P264 P270 P280 P301+310 P301+330+331 P302+352 P303+361+353 P304+340 P305+351+338 P310 P312 P321 P322 P330 P361 P363 P405 P501[1] |
| Teplota vzplanutí | 86 °C (359 K)[1] |
| Teplota vznícení | 558 °C (831 K)[1] |
Některá data mohou pocházet z datové položky. | |
m-Kresol (tj. meta-kresol) (systematický název 3-methylfenol), je organická sloučenina, isomer kresolu (CH3C6H4OH). Tato bezbarvá kapalina se často používá na přípravu dalších sloučenin. Jedná se o methylovaný derivát fenolu a polohový izomer o-kresolu a p-kresolu.
Výroba[editovat | editovat zdroj]
m-Kresol se, spolu s řadou dalších látek, získával z uhelného dehtu, získávaného při výrobě koksu. Vedlejší produkty této výroby obsahují několik procent fenolu a kresolů. Průmyslově se vyrábí také cymenovým-kresolovým procesem, kdy je toluen alkylován propenem za vzniku isomerů cymenu, které jsou poté oxidačně dealkylovány; tento postup je podobný kumenovému procesu. Lze také použít karbonylaci směsi methallylchloridu a ethynu pomocí tetrakarbonylu niklu.[2]
Použití[editovat | editovat zdroj]
m-Kresol je používán na výrobu mnoha látek, ke kterým patří například:
- pesticidy jako fenitrothion a fenthion
- dezinfekční látky, například amylmetakresol
- toliprolol, tolamolol a kresatin
Také je výchozí látkou při totální syntéze thymolu,[3] používaného jako součást vůní a připravovaného uměle kvůli nedostatku přírodních zdrojů:[4]
Výskyt[editovat | editovat zdroj]
m-Kresol je složkou výměšků temporálních žláz sloních samců[5] a také se nachází v cigaretovém kouři.[6]
Odkazy[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu m-kresol na Wikimedia Commons
Obrázky, zvuky či videa k tématu m-kresol na Wikimedia Commons
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku m-Cresol na anglické Wikipedii.
- ↑ a b c d e f g h i j k l m n o p q r m-Cresol. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ Helmut Fiege. Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH, 2007. DOI 10.1002/14356007.a08_025. Kapitola Cresols and Xylenols.
- ↑ R. Stroh; R. Sydel; W. Hahn. Newer Methods of Preparative Organic Chemistry, Volume 2. Příprava vydání Wilhelm Foerst. New York: Academic Press, 1963. ISBN 9780323150422. Kapitola Cresols and Xylenols, s. 344.
- ↑ Asim Kumar Mukhopadhyayn. Industrial Chemical Cresols and Downstream Derivatives. New York: CRC Press, 2004. ISBN 9780203997413. S. 99–100.
- ↑ Some chemical constituents of the secretion from the temporal gland of the African elephant (Loxodonta africana). Jack Adams, Alexander Garcia and Christopher S. Foote, Journal of Chemical Ecology, 1978, Volume 4, Number 1, 17-25, DOI:10.1007/BF00988256
- ↑ R. Talhout; T. Schulz; E. Florek; J. van Benthem; P. Wester; A. Opperhuizen. Hazardous compounds in tobacco smoke. International Journal of Environmental Research and Public Health. 2011, s. 613–628. DOI 10.3390/ijerph8020613. PMID 21556207.


