Cyklohexa-1,3-dien
| Cyklohexa-1,3-dien | |
|---|---|
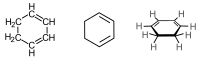 Strukturní vzorec | |
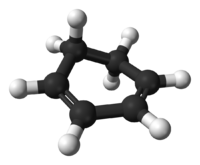 Model molekuly | |
| Obecné | |
| Systematický název | cyklohexa-1,3-dien |
| Ostatní názvy | 1,2-dihydrobenzen |
| Sumární vzorec | C6H8 |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 592-57-4 |
| ChEBI | 37610 |
| SMILES | C1CC=CC=C1 |
| InChI | 1/C6H8/c1-2-4-6-5-3-1/h1-4H,5-6H2 |
| Číslo RTECS | GU4702350 |
| Vlastnosti | |
| Molární hmotnost | 80,128 g/mol |
| Teplota tání | −98 °C (175 K) |
| Teplota varu | 80 °C (353 K) |
| Hustota | 0,841 g/cm3 |
| Index lomu | 1,475 (20 C) |
| Rozpustnost ve vodě | nerozpustný |
| Měrná magnetická susceptibilita | −6,07.105 μm3/g |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| R-věty | R11 |
| S-věty | S9 S16 S29 S33 |
| Teplota vzplanutí | 26 °C (299 K) |
Některá data mohou pocházet z datové položky. | |
Cyklohexa-1,3-dien je organická sloučenina, cyklický dien izomerní s cyklohexa-1,4-dienem. V přírodě se vyskytuje jeho derivát terpinen, jenž je složkou borovicové silice.
Příprava[editovat | editovat zdroj]
Cyklohexa-1,3-dien se připravuje dehydrobromací 1,2-dibromcyklohexanu:[2]
- (CH2)4(CHBr)2 + 2 NaH → (CH2)2(CH)4 + 2 NaBr + 2 H2
Lze jej také získat elektrocyklickou reakcí z benzenu jak fotochemickou reakcí, tak i tepelnou reakcí při teplotách nad 110 °C.[3]
Reakce[editovat | editovat zdroj]
Cyklohexa-1,3-dien lze jakožto konjugovaný dien použít při cykloadicích, jako je Dielsova–Alderova reakce.[4]
Přeměna cyklohexa-1,3-dienu na benzen a vodík je exotermní, změna entalpie při reakci je asi 25 kJ/mol.[5][6]
- cyklohexan → cyklohexa-1,3-dien + 2 H2 ΔH +231,5 kJ/mol (endotermní reakce)
- cyklohexan → benzen + 3 H2 ΔH +205 kJ (endotermní reakce)
- cyklohexa-1,3-dien → benzen + H2 ΔH -26,5 kJ (exotermní reakce)
V porovnání s izomerním cyklohexa-1,4-dienem je cyklohexa-1,3-dien o 1,6 kJ/mol stabilnější.[7]
Cyklohexadieny a jejich deriváty tvoří komplexy s kovy; příkladem takového komplexu je [C6H8)Fe(CO)3], což je oranžová kapalina. Tento komplex reaguje s látkami odstraňujícími hydridovou skupinu za vzniku cyklohexadienylového derivátu[C6H7)Fe(CO)3]+.[8]
Odkazy[editovat | editovat zdroj]
Související články[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Cyklohexa-1,3-dien na Wikimedia Commons
Obrázky, zvuky či videa k tématu Cyklohexa-1,3-dien na Wikimedia Commons
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku 1,3-Cyclohexadiene na anglické Wikipedii.
- ↑ a b 1,3-Cyclohexadiene. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ JOHN P. SCHAEFER AND LELAND ENDRES. 1,3-Cyclohexadiene. Org. Synth.. 1967, s. 31. Dostupné online.; Coll. Vol.. S. 285.
- ↑ Stanley Roberts. Comprehensive Organic Functional Group Transformations: Synthesis: Carbon with No Attached Heteroatoms. Cambridge: Elsevier Science Ltd., 1995. Dostupné online. ISBN 0080423221. S. 419.
- ↑ Sanjeeva Rao Guppi, George A. O'Doherty, "1,3-Cyclohexadiene" Encyclopedia of Reagents for Organic Synthesis, 2008 John Wiley & Sons. DOI:10.1002/047084289X.rn00921
- ↑ US National Institute of Standards and Technology, NIST Chemistry WebBook 1,3-Cyclohexadiene Benzene
- ↑ J. Sherman The heats of hydrogenation of unsaturated hydrocarbons Archivováno 14. 7. 2011 na Wayback Machine. Journal of the American Oil Chemists' Society; Volume 16, Number 2 / February, 1939
- ↑ NIST Chemistry WebBook 1,4-Cyclohexadiene
- ↑ Anthony J. Pearson; Huikai Sun. Cyclohexadieneiron Tricarbonyl. =e-EROS Encyclopedia of Reagents for Organic Synthesis. 2008.


