Chlorid ytterbitý
| Chlorid ytterbitý | |
|---|---|
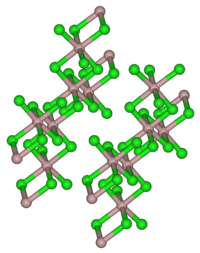 Krystalická struktura YbCl3 | |
 Chlorid ytterbitý | |
| Obecné | |
| Systematický název | Chlorid ytterbitý |
| Anglický název | Ytterbium(III) chloride |
| Německý název | Ytterbium(III)-chlorid |
| Sumární vzorec | YbCl3 |
| Vzhled | bílý prášek |
| Identifikace | |
| Registrační číslo CAS | 19423-81-1 |
| PubChem | 9860484 |
| SMILES | Cl[Yb](Cl)Cl |
| InChI | 1S/3ClH.Yb/h3*1H;/q;;;+3/p-3 |
| Vlastnosti | |
| Molární hmotnost | 279,40 g/mol |
| Teplota tání | 854 °C |
| Hustota | 4,06 g/cm3 |
| Rozpustnost ve vodě | 17 g/100 g |
Některá data mohou pocházet z datové položky. | |
Chlorid ytterbitý je anorganická sloučenina se vzorcem YbCl3. S chloridem nikelnatým vytváří velmi účinný katalyzátor pro reduktivní dehalogenaci arylhalogenidů.[1]
Chemické vlastnosti[editovat | editovat zdroj]
Elektronová konfigurace valenční slupky iontu Yb3+ je 4f13, což má výrazný vliv na jeho vlastnosti, stejně jako iontový poloměr. Díky jeho poměrně malé velikosti dokáže vystupovat jako rychlý katalyzátor a jeho atomový poloměr (0,99 Å) je srovnatelný s mnoha biologicky důležitými ionty.
Termodynamická vlastnosti v plynné fázi jsou obtížně zjistitelné, protože dochází k disproporcionaci na [YbCl6]3− nebo dimeraci.[2]
Příprava[editovat | editovat zdroj]
Chlorid ytterbitý lze připravit reakcí oxidu ytterbitého s plynným tetrachlormethanem za vysoké teploty nebo s kyselinou chlorovodíkovou:[3]
- 2 Yb2O3 (s) + 3 CCl4 (g) → 4 YbCl3 (s) + 3 CO2 (g)
- Yb2O3 (s) + 6 HCl (aq) → 2 YbCl3 (aq) + 3 H2O
Využití[editovat | editovat zdroj]
Katalýza[editovat | editovat zdroj]
Chlorid ytterbitý se chová jako Lewisova kyselina, díky jednomu nepárovému elektronu v orbitalu 4f. To mu umožňuje koordinaci (zpravidla jako [YbCl2]+) v tranzitním stavu při katalýze alkylačních reakcí, např. aldolové reakce nebo Pictetovy–Spenglerovy reakce.
Aldolová reakce[editovat | editovat zdroj]
Aldolová reakce je univerzální reakcí v organické syntéze. YbCl3 slouží jako katalyzátor, který napomáhá dekarboxylační aldolové reakci mezi enolátem ketonu a aldehydem katalyzované Pd(0). Tranzitní stavy A a B ukazují koordinaci ytterbité soli jako Lewisovy kyseliny.[4] Pro znázorněnou dekarboxylační reakci s R = terc-butyl a R' = -(CH2)2Ph ukazují výtěžky, že je YbCl3 velmi efektivním katalyzátorem:
| Kovová sůl | % výtěžku sloučeniny 2 |
|---|---|
| FeCl3 | 40 |
| ZnCl2 | 68 |
| CuCl2 | 40 |
| LaCl3 | 60 |
| YbCl3 | 93 |
Odkazy[editovat | editovat zdroj]
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku Ytterbium(III) chloride na anglické Wikipedii.
- ↑ ZHANG, Yuankui; LIAO, Shijian; XU, Yun. Reductive Dehalogenation of Aryl Halides by the Nanometric Sodium Hydride Using Lanthanide Chloride as Catalyst. Synthetic Communications. 1997-12, roč. 27, čís. 24, s. 4327–4334. Dostupné online [cit. 2021-12-25]. ISSN 0039-7911. DOI 10.1080/00397919708005057. (anglicky)
- ↑ (PDF) Vaporisation studies of dysprosium and ytterbium chlorides. ResearchGate [online]. [cit. 2021-12-25]. Dostupné online. (anglicky)
- ↑ SEBASTIAN, Jörg; SEIFERT, Hans-Joachim. Ternary chlorides in the systems ACl/YbCl3 (A=Cs,Rb,K). Thermochimica Acta. 1998-09, roč. 318, čís. 1–2, s. 29–37. Dostupné online [cit. 2021-12-25]. DOI 10.1016/S0040-6031(98)00326-8. (anglicky)
- ↑ LOU, Sha; WESTBROOK, John A.; SCHAUS, Scott E. Decarboxylative Aldol Reactions of Allyl β-Keto Esters via Heterobimetallic Catalysis. Journal of the American Chemical Society. 2004-09-01, roč. 126, čís. 37, s. 11440–11441. Dostupné online [cit. 2021-12-25]. ISSN 0002-7863. DOI 10.1021/ja045981k. (anglicky)
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Chlorid ytterbitý na Wikimedia Commons
Obrázky, zvuky či videa k tématu Chlorid ytterbitý na Wikimedia Commons

