Izotop
Izotop je označení pro nuklid v rámci souboru nuklidů jednoho chemického prvku. Jádra atomů izotopů jednoho prvku mají stejný počet protonů, ale mohou mít rozdílný počet neutronů. Mají tedy stejné atomové číslo a rozdílné hmotové číslo a atomovou hmotnost. Název pochází z řecké předpony iso- (stejno-) a topos (místo), protože v periodické tabulce se nacházejí na stejném místě.
Izotopy téhož prvku mají prakticky totožné chemické vlastnosti; hlavní rozdíl spočívá v tom, že těžší izotopy reagují poněkud pomaleji. Tento efekt je nejvýraznější u lehkého vodíku a deuteria, které je dvakrát těžší. U těžších prvků s větším počtem nukleonů je relativní rozdíl mnohem menší a jeho vliv obvykle zanedbatelný.
Fyzikální vlastnosti izotopů se odlišují. Kromě jejich hmotnosti a tedy hustoty jejich sloučenin bývá nejčastější odlišností mezi izotopy jejich stálost. Některé izotopy (vzdalující se od ideálního středního poměru počtu neutronů a protonů na kteroukoli stranu) totiž nejsou stabilní a podléhají radioaktivnímu rozpadu. Tyto radioaktivní izotopy jsou buď přirozené vznikající jadernými reakcemi samovolně, nebo umělé, vznikající v laboratoři. Odlišnosti lze také pozorovat v teplotách tání a varu sloučenin s odlišnými isotopy téhož prvku. Například voda H2O má za normálního tlaku teplotu varu 100 °C, kdežto voda těžká, D2O, má za stejných podmínek kvůli těžší molekule teplotu varu o 1,5 °C vyšší.
Jednotlivé izotopy mohou mít různý vliv na živé organismy. Deuterium je pro lidské tělo kvůli odlišné velikosti a tvaru molekul jedovaté.
Příklady izotopů
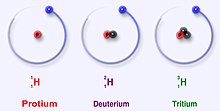
Izotopy vodíku
- 1
1 H – protium (běžný vodík) - 2
1 H – deuterium, též označované 2
1 D - 3
1 H – tritium, též označované 3
1 T
Izotopy uhlíku
- 12
6 C – uhlík 12 - 13
6 C – uhlík 13, využívaný v NMR spekroskopii - 14
6 C – uhlík 14 (radiouhlík)
Související články
Externí odkazy
 Obrázky, zvuky či videa k tématu izotop na Wikimedia Commons
Obrázky, zvuky či videa k tématu izotop na Wikimedia Commons  Slovníkové heslo izotop ve Wikislovníku
Slovníkové heslo izotop ve Wikislovníku
