Racemizace: Porovnání verzí
pokračování |
dokončení |
||
| Řádek 1: | Řádek 1: | ||
{{Pracuje se}} |
|||
'''Racemizace''' je chemický proces, při němž se enantiomerně čistá (je přítomen pouze jeden [[chiralita|enantiomer]]) látka mění na směs několika enantiomerů. Při racemizaci dojde k vytvoření stejného množství <small>D</small> a <small>L</small> enantiomerů, vzniká tak [[racemická směs]].<ref name="streitwieser">Streitwieser & Heathcock (1985) pp. 122–124</ref><ref name=Lehninger>{{cite book|last1 = Nelson|first1 = D. L.|last2 = Cox|first2 = M. M.|title=Lehninger Principles of Biochemistry|year = 2013|publisher =W. H. Freeman|location = New York|isbn = 1429234148|edition=6th}}</ref> |
'''Racemizace''' je chemický proces, při němž se enantiomerně čistá (je přítomen pouze jeden [[chiralita|enantiomer]]) látka mění na směs několika enantiomerů. Při racemizaci dojde k vytvoření stejného množství <small>D</small> a <small>L</small> enantiomerů, vzniká tak [[racemická směs]].<ref name="streitwieser">Streitwieser & Heathcock (1985) pp. 122–124</ref><ref name=Lehninger>{{cite book|last1 = Nelson|first1 = D. L.|last2 = Cox|first2 = M. M.|title=Lehninger Principles of Biochemistry|year = 2013|publisher =W. H. Freeman|location = New York|isbn = 1429234148|edition=6th}}</ref> |
||
| Řádek 8: | Řádek 6: | ||
Chirální molekuly mají dvě formy (na každém chirálním centru), které se liší svými optickými vlastnostmi: ''(−)'' izomer stáčí rovinu [[polarizace (elektrodynamika)|polarizovaného světla]] doleva, zatímco ''(+)'' izomer ji stáčí doprava. Tyto dvě formy se nazývají ''enantiomery''. Tato +/- notace by neměla být zaměňována s označováním <small>D</small> a <small>L</small>, které je odvozeno od struktury <small>D-</small> a <small>L-</small>[[glyceraldehyd]]u. |
Chirální molekuly mají dvě formy (na každém chirálním centru), které se liší svými optickými vlastnostmi: ''(−)'' izomer stáčí rovinu [[polarizace (elektrodynamika)|polarizovaného světla]] doleva, zatímco ''(+)'' izomer ji stáčí doprava. Tyto dvě formy se nazývají ''enantiomery''. Tato +/- notace by neměla být zaměňována s označováním <small>D</small> a <small>L</small>, které je odvozeno od struktury <small>D-</small> a <small>L-</small>[[glyceraldehyd]]u. |
||
Při racemizaci se jeden čistý enantiomer mění na stejná množství obou enantiomerů za vzniku racemické směsi. Je-li přítomno stejné množství (+) a (−) formy, pak k [[optická otáčivost|optické otáčivosti]] nedochází.<ref name="streitwieser"/> Enantiomery nejsou totéž jako diastereomery, druh stereoizomerů, které se |
Při racemizaci se jeden čistý enantiomer mění na stejná množství obou enantiomerů za vzniku racemické směsi. Je-li přítomno stejné množství (+) a (−) formy, pak k [[optická otáčivost|optické otáčivosti]] nedochází.<ref name="streitwieser"/> Enantiomery nejsou totéž jako diastereomery, druh stereoizomerů, které se liší strukturou molekuly kolem stereocentra a nejsou zrcadlovými obrazy. |
||
== Objev optické aktivity == |
|||
Roku 1843 objevil [[Louis Pasteur]] optickou aktivitu u kyseliny parahroznové (racemické [[kyselina vinná|kyseliny vinné]]). Dokázal izolovat krystaly dvou enantiomerů, které otáčely rovinu polarozovaného světla opačným směrem.<ref name="Lehninger"/> |
|||
== Vliv na fyzikální vlastnosti == |
== Vliv na fyzikální vlastnosti == |
||
| Řádek 14: | Řádek 15: | ||
== Biologický význam == |
== Biologický význam == |
||
Většina biochemických reakcí je stereoselektivní, takže se jen jeden stereoizomer účastní reakce a druhý nereaguje nebo způsobuje vedlejší účinky; například u [[aminokyselina|aminokyselin]] jsou obvykle biologicky aktivní <small>L</small> izomery a u [[sacharidy|sacharidů]] (hlavně [[glukóza|glukózy]]) <small>D</small>-izomery, což je způsobeno tím, že mnoho biomolekul je [[chiralita|chirálních]] a tak reakcemi se specifickými enantiomery vznikají čisté stereoizomery.<ref name="Voet, Voet, Pratt">{{cite book|last1 = Voet|authorlink1 = Donald Voet|first1 = D.|last2 = Voet|first2 = J. G.|authorlink2 = Judith G. Voet|last3 = Pratt|first3 = C. W.|title = Fundamentals of Biochemistry: Life at the Molecular Level|year = 2013|publisher = |
Většina biochemických reakcí je stereoselektivní, takže se jen jeden stereoizomer účastní reakce a druhý nereaguje nebo způsobuje vedlejší účinky; například u [[aminokyselina|aminokyselin]] jsou obvykle biologicky aktivní <small>L</small> izomery a u [[sacharidy|sacharidů]] (hlavně [[glukóza|glukózy]]) <small>D</small>-izomery, což je způsobeno tím, že mnoho biomolekul je [[chiralita|chirálních]] a tak reakcemi se specifickými enantiomery vznikají čisté stereoizomery.<ref name="Voet, Voet, Pratt">{{cite book|last1 = Voet|authorlink1 = Donald Voet|first1 = D.|last2 = Voet|first2 = J. G.|authorlink2 = Judith G. Voet|last3 = Pratt|first3 = C. W.|title = Fundamentals of Biochemistry: Life at the Molecular Level|year = 2013|publisher = John Wiley & Sons|location = Hoboken, NJ|isbn = 0470547847|edition = 4th}}</ref> Důležitá je rovněž skutečnost, že všechny aminokyseliny se většinou vyskytují v <small>L</small> formě. Některé bakterie ovšem vytvářejí <small>D</small> aminokyselinové zbytky, z nichž se vytvářejí krátké polypeptidy, které lze nalézt vcnbsp;buněčných stěnách těchto bakterií. Zmíněné polypeptidy jsou hůře zpracovávány peptidázami a jsou syntetizovány bakteriálními enzymy namísto mRNA translace, při které se tvoří peptidy z <small>L</small>-aminokyselin.<ref name="Voet, Voet, Pratt"/> |
||
| ⚫ | Stereoselektivní povaha většiny biochemických reakcí znamená, že různé enantiomery téže látky mají rozdílné chemické vlastnosti a účinky na organismy. Mnoho psychotropních látek má různou aktivitu či účinnost v závislosti na izomerech, například [[amfetamin]] se často dodává jako racemická směs, ovšem [[dextroamfetamin]] je aktivnější. Podobná situace je u [[metadon]]u, kde je jeden z izomerů opioidovým antagonistou, zatímco druhý je antagonistou NMDA.<ref>{{cite journal|last1 = Arnold|first1 = L. E.|last2 = Wender|first2 = P. H.|last3 = McCloskey|first3 = K.|last4 = Snyder|first4 = S. H.|title = |
||
| ⚫ | Stereoselektivní povaha většiny biochemických reakcí znamená, že různé enantiomery téže látky mají rozdílné chemické vlastnosti a účinky na organismy. Mnoho psychotropních látek má různou aktivitu či účinnost v závislosti na izomerech, například [[amfetamin]] se často dodává jako racemická směs, ovšem [[dextroamfetamin]] je aktivnější. Podobná situace je u [[metadon]]u, kde je jeden z izomerů opioidovým antagonistou, zatímco druhý je antagonistou NMDA.<ref>{{cite journal|last1 = Arnold|first1 = L. E.|last2 = Wender|first2 = P. H.|last3 = McCloskey|first3 = K.|last4 = Snyder|first4 = S. H.|title = Levoamphetamine and Dextroamphetamine: Comparative Efficacy in the Hyperkinetic Syndrome: Assessment by Target Symptoms.|journal = Arch. Gen. Psychiatry|year = 1972|volume = 27|issue = 6|pages = 816–822|doi=10.1001/archpsyc.1972.01750300078015|pmid= 4564954}}</ref> |
||
Racemizace [[léčivo|léčiv]] může probíhat ''in vivo''. ''R'' enantiomer [[thalidomid]]u je účinný proti ranním nevolnostem, zatímco jeho ''S'' enantiomer je [[teratogen]]ní, způsobuje poškození [[embryo|zárodku]] v prvním trimestru těhotenství. Pokud je podán pouze jeden enantiomer, později lze v krevním séru najtít oba;<ref>{{cite journal|journal = Clin. Pharmacokinet.|year = 2004|volume = 43|issue = 5|pages = 311–327|title = Clinical pharmacokinetics of thalidomide|pmid = 15080764|author1 = Teo, S. K.|author2 = Colburn, W. A.|author3 = Tracewell, W. G.|author4 = Kook, K. A.|author5 = Stirling, D. I.|author6 = Jaworsky, M. S.|author7 = Scheffler, M. A.|author8 = Thomas S. D.|author9 = Laskin, O. L.|doi = 10.2165/00003088-200443050-00004}}</ref> látka tak není považována za bezpečnou pro ženy v produktivním věku a i v ostatních případech je její používání pod přísným dohledem.<ref name="nyt-fda">{{cite news|url = https://www.nytimes.com/1998/07/17/us/thalidomide-approved-to-treat-leprosy-with-other-uses-seen.html|title = Thalidomide Approved to Treat Leprosy, With Other Uses Seen|newspaper =[[The New York Times]]|first = S. G.|last = Stolberg|accessdate = 8 January 2012|date = 17 July 1998}}</ref><ref>{{cite web |url = http://www.who.int/lep/research/thalidomide/en/index.html|title = Use of thalidomide in leprosy|work = WHO:leprosy elimination|publisher = [[Světová zdravotnická organizace|World Health Organisation]]|accessdate = 22 April 2010}}</ref> |
|||
U [[ibuprofen]]u má protizánětlivé účinky pouze jeden enantiomer, zatímco druhý je biologicky neúčinný. |
|||
Obdobně je ''S'' stereoisomer [[citalopram]]u mnohem reaktivnější než ''R'' enantiomer.<ref name="Lehninger"/><ref name="Voet, Voet, Pratt"/><ref>{{cite journal|last1 = Jacquot|first1 = C.|first2 = D. J.|last2 = David|last3 = Gardier|first3 = A. M.|first4 = C.|last4 = Sánchez|title = Escitalopram and citalopram: the unexpected role of the ''R''-enantiomer|year = 2007|volume = 33|issue = 2|pages = 179–187|pmid = 17675913|journal = Encéphale}}</ref> |
|||
Konfigurační stabilita léčiv je z těchto důvodů předmětem zájmu ve farmaceutickém výzkumu.<ref name="reist">{{cite book |title=Stereochemical Aspects of Drug Action and Disposition|volume =153| series =Handbook of Experimental Pharmacology |url=https://books.google.com/books?id=0U_xCAAAQBAJ&pg=PA91&lpg=PA91 |pages= 91–112 |chapter=Drug Racemization and Its Significance in Pharmaceutical Research |editors= Michel F. Eichelbaum, Bernard Testa, Andrew Somogyi |authors=M. Reist, B. Testa, P.-A. Carrupt |doi= 10.1007/978-3-642-55842-9_4}}</ref> Tvorba a analýza enantiomerů ve farmaceutickém průmyslu se studuje v oblasti chirální organické syntézy. |
|||
== Tvorba racemických směsí == |
|||
Racemizace lze dosáhnout pouhým smísením stejných množství dvou čistých enantiomerů. |
|||
K racemizaci může dojít během následujících procesů: |
|||
* Substituční reakce, při nichž vzniká [[karbokation]]tový meziprodukt, jako jsou [[SN1 reakce|jednomolekulární substituce]], vedou k stereonespecifické adici substituentů, která vyústí v racemizaci. |
|||
* I když u jednomolekulárních eliminačních reakcí také vzniká karbokation, tak nedochází ke vzniku chirálních center. Místo toho se vytvoří několik [[cis-trans izomerie|geometrických izomerů]] v (''E''/''Z'') formách. |
|||
* Pokud při jednomolekulové alifatické [[elektrofilní substituce|elektrofilní substituci]] vzniká [[karbanion]], který je rovinný nebo nemůže zůstat v pyramidální struktuře, pak někdy, ovšem ne vždy, proběhne racemizace.<ref>March (1985) pp. 517–518</ref> |
|||
* Pokud při [[radikálová substituce|radikálové substituci]] vzniknou volné radikály na chirálním uhlíku, pak dojde téměř vždy k ;racemizaci.<ref>March (1985) p. 610</ref> |
|||
Zjišťování míry racemizace <small>L</small>-forem na směs <small>L</small>- a <small>D</small>-forem) je jednou z metod datování biologických vzorků ve tkáních s nízkou mírou obratu, forenzních vzorků a zkaměnělin. Tato metoda se nazývá [[aminokyselinové datování]]. |
|||
== Odkazy == |
|||
=== Související články === |
|||
* [[Chiralita]] |
|||
* [[Racemická směs]] |
|||
=== Reference === |
|||
{{Překlad|jazyk=en|článek=Racemization|revize=821604039}} |
|||
<references /> |
|||
{{Portály|Chemie}} |
|||
[[Kategorie:Chemické reakce]] |
[[Kategorie:Chemické reakce]] |
||
Verze z 25. 2. 2018, 16:24
Racemizace je chemický proces, při němž se enantiomerně čistá (je přítomen pouze jeden enantiomer) látka mění na směs několika enantiomerů. Při racemizaci dojde k vytvoření stejného množství D a L enantiomerů, vzniká tak racemická směs.[1][2]
Stereochemie
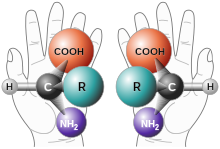
Chirální molekuly mají dvě formy (na každém chirálním centru), které se liší svými optickými vlastnostmi: (−) izomer stáčí rovinu polarizovaného světla doleva, zatímco (+) izomer ji stáčí doprava. Tyto dvě formy se nazývají enantiomery. Tato +/- notace by neměla být zaměňována s označováním D a L, které je odvozeno od struktury D- a L-glyceraldehydu.
Při racemizaci se jeden čistý enantiomer mění na stejná množství obou enantiomerů za vzniku racemické směsi. Je-li přítomno stejné množství (+) a (−) formy, pak k optické otáčivosti nedochází.[1] Enantiomery nejsou totéž jako diastereomery, druh stereoizomerů, které se liší strukturou molekuly kolem stereocentra a nejsou zrcadlovými obrazy.
Objev optické aktivity
Roku 1843 objevil Louis Pasteur optickou aktivitu u kyseliny parahroznové (racemické kyseliny vinné). Dokázal izolovat krystaly dvou enantiomerů, které otáčely rovinu polarozovaného světla opačným směrem.[2]
Vliv na fyzikální vlastnosti
Racemát má často odlišné fytzikální vlastnosti než každý jednotlivý enantiomer kvůli odlišným vnitromolekulárním interakcím. Přeměna z čistého enantiomeru na racemát může způsobit změnu hustoty, teploty tání, rozpustnosti, slučovacího tepla, indexu lomu a také různých spekter. Krystalizací racemické směsi mohou vzniknout oddělené (+) a (−) formy nebo jediná racemická látka.
Biologický význam
Většina biochemických reakcí je stereoselektivní, takže se jen jeden stereoizomer účastní reakce a druhý nereaguje nebo způsobuje vedlejší účinky; například u aminokyselin jsou obvykle biologicky aktivní L izomery a u sacharidů (hlavně glukózy) D-izomery, což je způsobeno tím, že mnoho biomolekul je chirálních a tak reakcemi se specifickými enantiomery vznikají čisté stereoizomery.[3] Důležitá je rovněž skutečnost, že všechny aminokyseliny se většinou vyskytují v L formě. Některé bakterie ovšem vytvářejí D aminokyselinové zbytky, z nichž se vytvářejí krátké polypeptidy, které lze nalézt vcnbsp;buněčných stěnách těchto bakterií. Zmíněné polypeptidy jsou hůře zpracovávány peptidázami a jsou syntetizovány bakteriálními enzymy namísto mRNA translace, při které se tvoří peptidy z L-aminokyselin.[3]
Stereoselektivní povaha většiny biochemických reakcí znamená, že různé enantiomery téže látky mají rozdílné chemické vlastnosti a účinky na organismy. Mnoho psychotropních látek má různou aktivitu či účinnost v závislosti na izomerech, například amfetamin se často dodává jako racemická směs, ovšem dextroamfetamin je aktivnější. Podobná situace je u metadonu, kde je jeden z izomerů opioidovým antagonistou, zatímco druhý je antagonistou NMDA.[4]
Racemizace léčiv může probíhat in vivo. R enantiomer thalidomidu je účinný proti ranním nevolnostem, zatímco jeho S enantiomer je teratogenní, způsobuje poškození zárodku v prvním trimestru těhotenství. Pokud je podán pouze jeden enantiomer, později lze v krevním séru najtít oba;[5] látka tak není považována za bezpečnou pro ženy v produktivním věku a i v ostatních případech je její používání pod přísným dohledem.[6][7]
U ibuprofenu má protizánětlivé účinky pouze jeden enantiomer, zatímco druhý je biologicky neúčinný. Obdobně je S stereoisomer citalopramu mnohem reaktivnější než R enantiomer.[2][3][8]
Konfigurační stabilita léčiv je z těchto důvodů předmětem zájmu ve farmaceutickém výzkumu.[9] Tvorba a analýza enantiomerů ve farmaceutickém průmyslu se studuje v oblasti chirální organické syntézy.
Tvorba racemických směsí
Racemizace lze dosáhnout pouhým smísením stejných množství dvou čistých enantiomerů.
K racemizaci může dojít během následujících procesů:
- Substituční reakce, při nichž vzniká karbokationtový meziprodukt, jako jsou jednomolekulární substituce, vedou k stereonespecifické adici substituentů, která vyústí v racemizaci.
- I když u jednomolekulárních eliminačních reakcí také vzniká karbokation, tak nedochází ke vzniku chirálních center. Místo toho se vytvoří několik geometrických izomerů v (E/Z) formách.
- Pokud při jednomolekulové alifatické elektrofilní substituci vzniká karbanion, který je rovinný nebo nemůže zůstat v pyramidální struktuře, pak někdy, ovšem ne vždy, proběhne racemizace.[10]
- Pokud při radikálové substituci vzniknou volné radikály na chirálním uhlíku, pak dojde téměř vždy k ;racemizaci.[11]
Zjišťování míry racemizace L-forem na směs L- a D-forem) je jednou z metod datování biologických vzorků ve tkáních s nízkou mírou obratu, forenzních vzorků a zkaměnělin. Tato metoda se nazývá aminokyselinové datování.
Odkazy
Související články
Reference
V tomto článku byl použit překlad textu z článku Racemization na anglické Wikipedii.
- ↑ a b Streitwieser & Heathcock (1985) pp. 122–124
- ↑ a b c NELSON, D. L.; COX, M. M. Lehninger Principles of Biochemistry. 6th. vyd. New York: W. H. Freeman, 2013. ISBN 1429234148.
- ↑ a b c VOET, D.; VOET, J. G.; PRATT, C. W. Fundamentals of Biochemistry: Life at the Molecular Level. 4th. vyd. Hoboken, NJ: John Wiley & Sons, 2013. ISBN 0470547847.
- ↑ ARNOLD, L. E.; WENDER, P. H.; MCCLOSKEY, K.; SNYDER, S. H. Levoamphetamine and Dextroamphetamine: Comparative Efficacy in the Hyperkinetic Syndrome: Assessment by Target Symptoms.. Arch. Gen. Psychiatry. 1972, s. 816–822. DOI 10.1001/archpsyc.1972.01750300078015. PMID 4564954.
- ↑ Teo, S. K.; COLBURN, W. A.; TRACEWELL, W. G.; KOOK, K. A.; STIRLING, D. I.; JAWORSKY, M. S.; SCHEFFLER, M. A. Clinical pharmacokinetics of thalidomide. Clin. Pharmacokinet.. 2004, s. 311–327. DOI 10.2165/00003088-200443050-00004. PMID 15080764.
- ↑ STOLBERG, S. G. Thalidomide Approved to Treat Leprosy, With Other Uses Seen. The New York Times. 17 July 1998. Dostupné online [cit. 8 January 2012].
- ↑ Use of thalidomide in leprosy [online]. World Health Organisation [cit. 2010-04-22]. Dostupné online.
- ↑ JACQUOT, C.; DAVID, D. J.; GARDIER, A. M.; SÁNCHEZ, C. Escitalopram and citalopram: the unexpected role of the R-enantiomer. Encéphale. 2007, s. 179–187. PMID 17675913.
- ↑ M. Reist, B. Testa, P.-A. Carrupt. Stereochemical Aspects of Drug Action and Disposition. Redakce Michel F. Eichelbaum, Bernard Testa, Andrew Somogyi. [s.l.]: [s.n.] (Handbook of Experimental Pharmacology; sv. 153). Dostupné online. DOI 10.1007/978-3-642-55842-9_4. Kapitola Drug Racemization and Its Significance in Pharmaceutical Research, s. 91–112.
- ↑ March (1985) pp. 517–518
- ↑ March (1985) p. 610
