Dichlor(1,3-bis(difenylfosfino)propan)nikl
| Dichlor(1,3-bis(difenylfosfino)propan)nikl | |
|---|---|
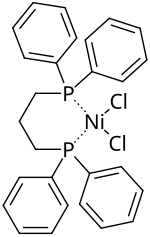 Strukturní vzorec | |
| Obecné | |
| Systematický název | dichlor[propan-1,3-diylbis(difenylfosfanuid-κP)]nikl |
| Sumární vzorec | C27H26Cl2NiP2 |
| Vzhled | oranžový až červenooranžový prášek |
| Identifikace | |
| Registrační číslo CAS | 15629-92-2 |
| EC-no (EINECS/ELINCS/NLP) | 605-052-3 |
| PubChem | 6329934 |
| SMILES | Cl[Ni]3(Cl)P(CCCP3(c1ccccc1)c2ccccc2)(c4ccccc4)c5ccccc5 |
| InChI | InChI=1S/C27H26P2.2ClH.Ni/c1-5-14-24(15-6-1)28(25-16-7-2-8-17-25)22-13-23-29(26-18-9-3-10-19-26)27-20-11-4-12-21-27;;;/h1-12,14-21H,13,22-23H2;2*1H; |
| Vlastnosti | |
| Molární hmotnost | 542,04 g/mol |
| Teplota tání | 213 °C (486 K) |
| Rozpustnost ve vodě | nerozpustný |
| Bezpečnost | |
| H-věty | H315 H317 H319 H334 H335 H350 |
| P-věty | P201 P261 P280 P305+351+338 P308+313 |
Některá data mohou pocházet z datové položky. | |
Dichlor(1,3-bis(difenylfosfino)propan)nikl je komplexní sloučenina se vzorcem NiCl2(dppp), kde dppp je 1,3-bis(difenylfosfino)propan. Používá se v organické syntéze jako katalyzátor.
Struktura a vlastnosti
[editovat | editovat zdroj]Vlastnosti této látky v pevné podobě nejsou dobře prozkoumány, protože se ve většině běžných rozpouštědel nerozpouští; bylo však provedeno několik studií zabývajících se odpovídajícími komplexy bromu a jodu.[1]
Tyto komplexy mohou při určitých teplotách v polárních organických rozpouštědlech přecházet mezi čtvercově rovinnou a tetraedrickou geometrií (v první jsou diamagnetické a ve druhé paramagnetické). Od těchto látek se liší dichlor(1,3-bis(difenylfosfino)ethan)nikl, který má v roztocích stálou čtvercově rovinnou (diamagnetickou) strukturu.
Příprava
[editovat | editovat zdroj]NiCl2(dppp)se připravuje smícháním stejných látkových množství hexahydrátu chloridu nikelnatého a 1,3-bis(difenylfosfino)propanu v propan-2-olu.[2]
- Ni(H2O)6Cl2 + dppp → NiCl2(dppp) + 6 H2O
Reakce
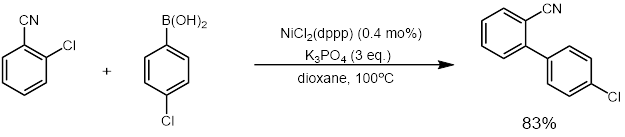
[editovat | editovat zdroj]NiCl2(dppp) je účinným katalyzátorem reakcí jako jsou Kumadovo[2] a Suzukiovo párování.[3] Může katalyzovat i jiné reakce, přeměňující enolethery, dithioacetaly, a vinylsulfidy na alkeny.[4][5]
Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Dichloro(1,3-bis(diphenylphosphino)propane)nickel na anglické Wikipedii.
- ↑ Gerald R. Van Hecke; William W. Horrocks. Ditertiary Phosphine Complexes of Nickel. Spectral, Magnetic, and Proton Resonance Studies. A Planar-Tetrahedral Equilibrium. Inorganic Chemistry. 1966, s. 1968–1974. DOI 10.1021/ic50045a029.
- ↑ a b Makota Kumada; Kohei Tamao; Koji Sumitani. Phosphine-Nickel Complex Catalyzed Cross-Coupling of Grignard Reagents with Aryl and Alkenyl Halides: 1,2-Dibutylbenzene. Organic Syntheses. 1978, s. 127. DOI 10.15227/orgsyn.058.0127.
- ↑ Yu-Long Zhao; You Li; Shui-Ming Li; Yi-Guo Zhou; Feng-Yi Sun; Lian-Xun Gao; Fu-She Han. A Highly Practical and Reliable Nickel Catalyst for Suzuki-Miyaura Coupling of Aryl Halides. Advanced Synthesis & Catalysis. 2011, s. 1543–1550. DOI 10.1002/adsc.201100101.
- ↑ Tien-Yau Luh; Tien-Min Yuan. Cross-Coupling Reactions Encyclopedia of Reagents for Organic Synthesis DOI:10.1002/047084289X.rd100.pub2
- ↑ Thomas Ljungdahl; Timmanna Bennur; Andrea Dallas; Hans Emtenaes; Jerker Maartensson. Two Competing Mechanisms for the Copper-Free Sonogashira Cross-Coupling Reaction. Organometallics. 2008, s. 2490–2498. DOI 10.1021/om800251s.
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu Dichlor(1,3-bis(difenylfosfino)propan)nikl na Wikimedia Commons
Obrázky, zvuky či videa k tématu Dichlor(1,3-bis(difenylfosfino)propan)nikl na Wikimedia Commons


