Bromaceton
| Bromaceton | |
|---|---|
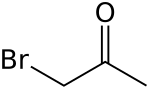 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | 1-brompropan-2-on |
| Funkční vzorec | CH2BrC(O)CH3 |
| Sumární vzorec | C3H5BrO |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 598-31-2 |
| PubChem | 11715 |
| ChEBI | 51845 |
| SMILES | BrCC(=O)C |
| InChI | 1/C3H5BrO/c1-3(5)2-4/h2H2,1H3 |
| Vlastnosti | |
| Molární hmotnost | 136,98 g/mol |
| Teplota tání | −36,5 °C (236,6 K) |
| Teplota varu | 137 °C (410 K) |
| Hustota | 1,634 g/cm3 |
| Tlak páry | 1,1 kPa (20 °C) |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
Některá data mohou pocházet z datové položky. | |
Bromaceton (systematický název 1-brompropan-2-on) je organická sloučenina se vzorcem CH3C(O)CH2Br. Používá se na přípravu dalších organických látek.
Výskyt[editovat | editovat zdroj]
Bromaceton se (v koncentracích pod 1 %) vyskytuje v mořské řase Asparagopsis taxiformis rostoucí v okolí Havajských ostrovů.[2]
Výroba[editovat | editovat zdroj]
Bromaceton je komerčně dostupný, často bývá stabilizován oxidem hořečnatým.
Vyrábí se reakcí acetonu s bromem v kyselém prostředí.[3] Aceton se, podobně jako ostatní ketony, za přítomnosti kyseliny či zásady přeměňuje na enol. Na alfa uhlík se následně elektrofilní substitucí naváže brom; přitom může dojít k přebromování, kdy se naváže více atomů bromu, než je potřeba, čímž vznikají dibromované a tribromované produkty. V zásaditém prostředí se tvoří bromoform, jelikož dojde k haloformové reakci.[4]
Použití[editovat | editovat zdroj]
Bromaceton se v první světové válce používal jako chemická zbraň. V organické syntéze se používá například na přípravu hydroxyacetonu.[5]
Odkazy[editovat | editovat zdroj]
Související články[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Bromaceton na Wikimedia Commons
Obrázky, zvuky či videa k tématu Bromaceton na Wikimedia Commons
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku Bromoacetone na anglické Wikipedii.
- ↑ a b Bromoacetone. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ B. J. Burreson; R. E. Moore; P. P. Roller. Volatile halogen compounds in the alga Asparagopsis taxiformis (Rhodophyta). Journal of Agricultural and Food Chemistry. 1976, s. 856–861.
- ↑ LEVENE, P. A. Bromoacetone. Org. Synth.. 1930, s. 12. Dostupné online.; Coll. Vol.. S. 88.
- ↑ W. Reusch. Virtual Textbook of Organic Chemistry [online]. Michigan State University, 5.5. 2013 [cit. 2007-10-27]. Kapitola Carbonyl Reactivity. Dostupné v archivu pořízeném z originálu dne 21.6. 2010.
- ↑ LEVENE, P. A.; WALTI, A. Acetol. Org. Synth.. 1930, s. 1. Dostupné online.; Coll. Vol.. S. 5.



