Diazosloučeniny: Porovnání verzí
m odebrána Kategorie:Diazosloučeniny; přidána Kategorie:Diazolátky za použití HotCat |
pokračování |
||
| Řádek 28: | Řádek 28: | ||
Při'''diazo přesunu reagují některé [[Karboanion#Karbonové kyseliny|karbonové kyseliny]] s tosylazidem: |
Při'''diazo přesunu reagují některé [[Karboanion#Karbonové kyseliny|karbonové kyseliny]] s tosylazidem: |
||
:[[ |
:[[Soubor:Preparation of diazomalonic acid ester by Dimroth.svg|500px|Příprava esteru kyseliny diazomalonové]] |
||
Tato reakce se také nazývá '''Regitzův diazo přesun'''.<ref>M. Regitz, Angew. Chem., 79, 786 (1967); Angew. Chem. Intern. Ed. Engl., 6, 733 (1967).</ref> Dalšími příklady jsou syntéza ''terc-butyldiazoacetátu''<ref>Organic Syntheses, Coll. Vol. 5, p.179 (1973); Vol. 48, p.36 (1968). [http://www.orgsyn.org/orgsyn/prep.asp?prep=cv5p0179 Link]</ref> a ''di-terc-butyldiazomalonátu''.<ref>Organic Syntheses, Coll. Vol. 6, p.414 (1988); Vol. 59, p.66 (1979). [http://www.orgsyn.org/orgsyn/prep.asp?prep=cv6p0414 Link]</ref> |
Tato reakce se také nazývá '''Regitzův diazo přesun'''.<ref>M. Regitz, Angew. Chem., 79, 786 (1967); Angew. Chem. Intern. Ed. Engl., 6, 733 (1967).</ref> Dalšími příklady jsou syntéza ''terc-butyldiazoacetátu''<ref>Organic Syntheses, Coll. Vol. 5, p.179 (1973); Vol. 48, p.36 (1968). [http://www.orgsyn.org/orgsyn/prep.asp?prep=cv5p0179 Link]</ref> a ''di-terc-butyldiazomalonátu''.<ref>Organic Syntheses, Coll. Vol. 6, p.414 (1988); Vol. 59, p.66 (1979). [http://www.orgsyn.org/orgsyn/prep.asp?prep=cv6p0414 Link]</ref> |
||
| Řádek 35: | Řádek 35: | ||
Diazosloučeniny lze získat [[eliminace (chemie)|eliminační reakcí]] N-alkyl-N-nitrososloučenin,<ref>Example: Organic Syntheses, Coll. Vol. 6, p.981 (1988); Vol. 57, p.95 (1977). [http://www.orgsynth.org/orgsyn/pdfs/CV6P0981.pdf Link]</ref> jako například při přípravě diazomethanu z diazaldu nebo [[methylnitronitrosoguanidin|MNNG]]: |
Diazosloučeniny lze získat [[eliminace (chemie)|eliminační reakcí]] N-alkyl-N-nitrososloučenin,<ref>Example: Organic Syntheses, Coll. Vol. 6, p.981 (1988); Vol. 57, p.95 (1977). [http://www.orgsynth.org/orgsyn/pdfs/CV6P0981.pdf Link]</ref> jako například při přípravě diazomethanu z diazaldu nebo [[methylnitronitrosoguanidin|MNNG]]: |
||
:[[ |
:[[Soubor:Diazo Synthesis.svg|400px|Příprava diazosloučenin z N-alkyl-N-nitrososloučenin]] |
||
=== Z hydrazonů === |
=== Z hydrazonů === |
||
Diazosloučeniny se dají připravit také z [[hydrazon]]ů. Hydrazony se [[redoxní reakce|oxidují]] (vlastně [[dehydrogenace|dehydrogenují]]), například [[oxid stříbrný|oxidem stříbrným]]; příkladem může být příprava ''2-diazopropanu'' z acetonhydrazonu''.<ref>Organic Syntheses, Coll. Vol. 6, p.392 (1988); Vol. 50, p.27 (1970). [http://www.orgsynth.org/orgsyn/pdfs/CV6P0392.pdf Link]</ref> Jako [[oxidační činidlo]] lze použít rovněž [[octan olovičitý]], [[oxid manganičitý]] nebo [[Swernova oxidace|Swernovo činidlo]]. Při syntéze ''krotyldiazoacetátu'' reagují tosylhydrazony (obecný vzorec RRC=N-NHTs) se zásadou jako je například [[triethylamin]].<ref>Organic Syntheses, Coll. Vol. 5, p.258 (1973); Vol. 49, p.22 (1969). [http://www.orgsyn.org/orgsyn/prep.asp?prep=CV5P0258 Link]</ref> |
|||
Reakcí [[karbonylové sloučeniny|karbonylových sloučenin]] s derivátem [[hydrazin]]u ''1,2-bis(terc-butyldimethylsilyl)hydrazinem'' vzniká hydrazom; ten se následně působením ''difluorjodbenzenu'' mění na diazosloučeninu:<ref>{{Cite journal| last1 = Lei | first1 = X.| last2 = Porco Ja | first2 = J.| title = Total synthesis of the diazobenzofluorene antibiotic (-)-kinamycin C1| journal = Journal of the American Chemical Society| volume = 128| issue = 46| pages = 14790–14791| year = 2006| pmid = 17105273 | doi = 10.1021/ja066621v}}</ref><ref>''Elusive Natural Product Is Synthesized'' Stu Borman [[Chemical & Engineering News]] October 31, 2006 [http://pubs.acs.org/cen/news/84/i45/8445notw4.html Link].</ref> |
|||
:[[Soubor:KinamycinCSynthesis.png|400px|Syntéza kinamycinu C]] |
|||
=== Příprava fragmentací === |
|||
1,3-disubstituované alkylaryl[[triazen]]y mohou být fragmentovány za tvorby diazosloučenin. Tyto triazeny (ArN=NNH-CH<sub>2</sub>R) lze připravit spárováním [[diazoniové soli|diazoniových solí]] s primárními aminy. |
|||
=== Z azidů === |
|||
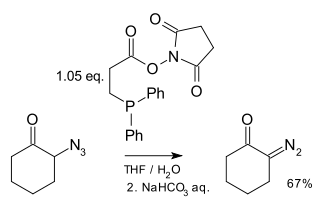
Byl popsán způsob pžípravy diazosloučenin z [[azidy|azidů]] za použití derivátů [[fosfan]]u.<ref>''A Phosphine-Mediated Conversion of Azides into Diazo Compounds'' Eddie L. Myers and Ronald T. Raines [[Angew. Chem. Int. Ed.]] '''2009''', 48, 2359 –2363 {{DOI|10.1002/anie.200804689}}</ref> |
|||
:[[Soubor:AzidetoDiazo Myers 2009.svg|Přeměna azidu na diazosloučeninu]] |
|||
== Reakce == |
|||
[[Kategorie:Funkční skupiny]] |
[[Kategorie:Funkční skupiny]] |
||
Verze z 26. 6. 2018, 14:52

Diazosloučeniny jsou organické sloučeniny, které mají jako koncovou funkční skupinu atomy dusíku spojené trojnou vazbou; obecný vzorec je R-(C=N2)-R'. Nejjednodušší takovou sloučeninou je diazomethan.
Elektronová struktura těchto sloučenin se skládá z kladného náboje na centrálním dusíkovém atomu a záporného náboje distribuovaného mezi koncovým dusíkem a uhlíkem, na nějž jsou tyto dusíky navázány. K nejstabilnějším diazosloučeninám patří α-diazo-ß-diketony a α-diazo-ß-diestery, a to díky delokalizaci záporného náboje v karbonylových skupinách; většina alkyldiazosloučenin patří mezi výbušniny.
Skupinou izomerních sloučenin, které však nemají mnoho podobných vlastností, jsou diaziriny, u nichž jsou uhlík a dva dusíky propojené v cyklickém řetězci.
Diazosloučeniny existují ve čtyřech rezonančních strukturách:[1]
Historie
První diazosloučeniny připravil roku 1858 německý chemik Peter Griess, když objevil novou všestrannou reakci.[2][3]
Příprava
Je známo několik laboratorních postupů na přípravu diazosloučenin.[4]
Z aminů
Alfa akceptory substituované primární alifatické aminy R-CH2-NH2 (R = COOR, CN, CHO, COR) reagují s kyselinou dusitou za vzniku diazosloučenin.
Z diazomethylových sloučenin
Příkladem elektrofilní substituce za použití diazomethylové sloučeniny je reakce acylhalogenidu s diazomethanem.[5], jenž je mimo jiné prvním krokem v Arndt-Eistertově syntéze.
Diazo přesunem
Přidiazo přesunu reagují některé karbonové kyseliny s tosylazidem:
Tato reakce se také nazývá Regitzův diazo přesun.[6] Dalšími příklady jsou syntéza terc-butyldiazoacetátu[7] a di-terc-butyldiazomalonátu.[8]
Z N-alkyl-N-nitrososloučenin
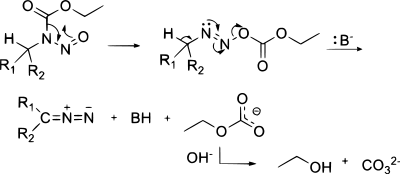
Diazosloučeniny lze získat eliminační reakcí N-alkyl-N-nitrososloučenin,[9] jako například při přípravě diazomethanu z diazaldu nebo MNNG:
Z hydrazonů
Diazosloučeniny se dají připravit také z hydrazonů. Hydrazony se oxidují (vlastně dehydrogenují), například oxidem stříbrným; příkladem může být příprava 2-diazopropanu z acetonhydrazonu.[10] Jako oxidační činidlo lze použít rovněž octan olovičitý, oxid manganičitý nebo Swernovo činidlo. Při syntéze krotyldiazoacetátu reagují tosylhydrazony (obecný vzorec RRC=N-NHTs) se zásadou jako je například triethylamin.[11]
Reakcí karbonylových sloučenin s derivátem hydrazinu 1,2-bis(terc-butyldimethylsilyl)hydrazinem vzniká hydrazom; ten se následně působením difluorjodbenzenu mění na diazosloučeninu:[12][13]
Příprava fragmentací
1,3-disubstituované alkylaryltriazeny mohou být fragmentovány za tvorby diazosloučenin. Tyto triazeny (ArN=NNH-CH2R) lze připravit spárováním diazoniových solí s primárními aminy.
Z azidů
Byl popsán způsob pžípravy diazosloučenin z azidů za použití derivátů fosfanu.[14]
Reakce
- ↑ F.A. Carey R.J. Sundberg Advanced Organic Chemistry, 2nd Edition
- ↑ Trevor I. Williams, ‘Griess, (Johann) Peter (1829–1888)’, Oxford Dictionary of National Biography, Oxford University Press, 2004
- ↑ Peter Griess (1858) "Vorläufige Notiz über die Einwirkung von salpetriger Säure auf Amidinitro- und Aminitrophenylsäure," (Preliminary notice of the reaction of nitrous acid with picramic acid and aminonitrophenol), Annalen der Chemie und Pharmacie, 106 : 123-125.
- ↑ New Syntheses of Diazo Compounds Gerhard Maas Angew. Chem. Int. Ed. 2009, 48, 8186 – 8195 DOI:10.1002/anie.200902785
- ↑ Example Organic Syntheses, Coll. Vol. 3, p.119 (1955); Vol. 26, p.13 (1946).Link
- ↑ M. Regitz, Angew. Chem., 79, 786 (1967); Angew. Chem. Intern. Ed. Engl., 6, 733 (1967).
- ↑ Organic Syntheses, Coll. Vol. 5, p.179 (1973); Vol. 48, p.36 (1968). Link
- ↑ Organic Syntheses, Coll. Vol. 6, p.414 (1988); Vol. 59, p.66 (1979). Link
- ↑ Example: Organic Syntheses, Coll. Vol. 6, p.981 (1988); Vol. 57, p.95 (1977). Link
- ↑ Organic Syntheses, Coll. Vol. 6, p.392 (1988); Vol. 50, p.27 (1970). Link
- ↑ Organic Syntheses, Coll. Vol. 5, p.258 (1973); Vol. 49, p.22 (1969). Link
- ↑ LEI, X.; PORCO JA, J. Total synthesis of the diazobenzofluorene antibiotic (-)-kinamycin C1. Journal of the American Chemical Society. 2006, s. 14790–14791. DOI 10.1021/ja066621v. PMID 17105273.
- ↑ Elusive Natural Product Is Synthesized Stu Borman Chemical & Engineering News October 31, 2006 Link.
- ↑ A Phosphine-Mediated Conversion of Azides into Diazo Compounds Eddie L. Myers and Ronald T. Raines Angew. Chem. Int. Ed. 2009, 48, 2359 –2363 DOI:10.1002/anie.200804689