Oktachlorodimolybdenatan draselný
| Oktachlorodimolybdenatan draselný | |
|---|---|
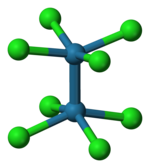
 Strukturní vzorec | |
 Vzorek K4Mo2Cl8 | |
| Obecné | |
| Systematický název | oktachlorodimolybdenatan draselný |
| Sumární vzorec | K4Mo2Cl8 |
| Vzhled | červenohnědá pevná látka |
| Identifikace | |
| Registrační číslo CAS | 106-93-4 |
| EC-no (EINECS/ELINCS/NLP) | 203-444-5 |
| PubChem | 472218179 |
| SMILES | C(CBr)Br |
| InChI | InChI=1S/C2H4Br2/c3-1-2-4/h1-2H2 |
| Vlastnosti | |
| Molární hmotnost | 631,94 g/mol |
| Hustota | 2,54 g/cm3 |
| Rozpustnost ve vodě | rozpustný |
Některá data mohou pocházet z datové položky. | |
Oktachlorodimolybdenatan draselný je anorganická sloučenina se vzorcem K4[Mo2Cl8]. Jeho anion se stal jedním z prvních známých příkladů čtverné vazby. Bezvodá sůl je červenohnědá, ale obvykle vytváří růžově zbarvený dihydrát.
Příprava
[editovat | editovat zdroj]Tento komplex se připravuje dvoukrokovým postupem z hexakarbonylu molybdenu:[1][2]
- 2 Mo(CO)6 + 4 CH3COOH → (CH3COO)4Mo2 + 2 H2 + 12 CO
U reakce HCl s octanem se původně předpokládalo, že se vytváří sloučenina trimolybdenu,[3] ale následnou krystalografickou analýzou se ukázalo, že sloučenina obsahuje anionty [Cl4Mo≣MoCl4]4–, se symetrií D4h, ve které jsou dva atomy molybdenu spojeny čtvernou vazbou. Jednotlivé atomy Mo jsou navázány na čtyři Cl− ligandy jednoduchými vazbami. Skupiny MoCl4 jsou čtvercově pyramidální,kde vrchol tvoří atom Mo a základnu atomy Cl. Délka vazby Mo–Mo je 214 pm.[4]
Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Potassium octachlorodimolybdate na anglické Wikipedii.
- ↑ A. B. Brignole; F. A. Cotton. Rhenium and Molybdenum Compounds Containing Quadruple Bonds. Inorganic Syntheses. 1972, s. 81–89. ISBN 978-0-470-13244-9. DOI 10.1002/9780470132449.ch15.
- ↑ G. S. Girolami; T. B. Rauchfuss. Synthesis and Technique in Inorganic Chemistry. Mill Valley, CA: University Science Books, 1999. Dostupné online. ISBN 978-0-935702-48-4.
- ↑ G. B. Allison; I. R. Anderson. The Preparation of Halogenotrimolybdate(II) Compounds. Australian Journal of Chemistry. 1967, s. 869–876. DOI 10.1071/CH9670869.
- ↑ Jurij V. Brencic; F. A. Cotton. Octachlorodimolybdate(II) Ion. Species with a Quadruple Metal–Metal Bond. Inorganic Chemistry. 1969, s. 7–10. DOI 10.1021/ic50071a002.
