Disilen
| Disilen | |
|---|---|
 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | disilen |
| Funkční vzorec | H2Si=SiH2 |
| Sumární vzorec | Si2H4 |
| Vzhled | bílé krystaly[1] |
| Identifikace | |
| Registrační číslo CAS | 106-93-4 |
| EC-no (EINECS/ELINCS/NLP) | 203-444-5 |
| PubChem | 139934 |
| SMILES | C(CBr)Br |
| InChI | InChI=1S/C2H4Br2/c3-1-2-4/h1-2H2 |
| Vlastnosti | |
| Molární hmotnost | 60,203 g/mol |
Některá data mohou pocházet z datové položky. | |
Disilen je anorganická sloučenina se vzorcem Si2H4. Jedná se o nejjednodušší silen.
Struktura[editovat | editovat zdroj]
Molekula disilenu obsahuje jednu vazbu Si=Si a čtyři rovnocenné vazby Si-H.
Na rozdíl od ethenu, jehož je analogem, je disilen kineticky nestálý a náchylný k tautomerizaci. Má další dva tautomery, s velmi podobnými energiemi: (μ2-H)disilen a disilanyliden.[2]
Organodisileny[editovat | editovat zdroj]
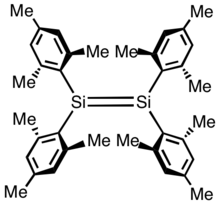
Disileny se stericky zatíženými substituenty mohou být izolovány a jejich vlastnosti jsou podrobně prozkoumány, přestože jde hlavně o předmět akademického zájmu. Prvním stabilizovaným disilenem byl tetramesityldisilen, (C6Me3H2)4Si2. Vazba Si=Si v této molekule má délku 215 pm, přibližně o 10 % menší, než je běžné u jednoduchých vazeb Si–Si. Si2C4 jádra jsou zhruba rovinná.[3] Organodisileny se většinou připravují redukcemi organokřemíkových halogenidů:
- 2 R2SiCl2 + 4 Na → R2Si=SiR2 + 4 NaCl
Další způsob představuje fotolýza trisilacyklopropanů. Pokud substituent nevytváří výraznější sterické efekty, tak jsou produkty, cyklické nebo polymerní, polysilany.
V jedné studii[4] byl získán disilen vnitromolekulární reakcí 1,1-dibromsilanu s grafitem draselným. Dvojná vazba mezi atomy křemíku u vytvořené sloučeniny měla, jak bylo zjištěno rentgenovou krystalografií, délku 227 pm, druhou největší, jež byla kdy zjištěna.
Substituenty okolo vazby Si-Si byly posunuty o 43°. Disilen bylo možné převést na tetracyklickou sloučeninu zahřátím na 110 °C v xylenu.
Odkazy[editovat | editovat zdroj]
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku Disilene na anglické Wikipedii.
- ↑ https://pubchem.ncbi.nlm.nih.gov/compound/15337
- ↑ M. C. McCarthy; Z. Yu; L. Sari; H. F. Schaefer; P. Thaddeus. Monobridged Si2H4. The Journal of Chemical Physics. 2006-02-15, s. 074303. DOI 10.1063/1.2168150. PMID 16497032. Bibcode 2006JChPh.124g4303M.
- ↑ GREENWOOD, Norman N.; EARNSHAW, Alan. Chemistry of the Elements. 2. vyd. [s.l.]: Butterworth-Heinemann, 1997. ISBN 978-0-08-037941-8.
- ↑ Fused Tricyclic Disilenes with Highly Strained Si-Si Double Bonds: Addition of a Si-Si Single Bond to a Si-Si Double Bond Ryoji Tanaka, Takeaki Iwamoto, and Mitsuo Kira Angewandte Chemie International Edition volume 45, issue 38 , pages 6371 - 6373 2006 DOI:10.1002/anie.200602214
Související články[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu disilen na Wikimedia Commons
Obrázky, zvuky či videa k tématu disilen na Wikimedia Commons

