1,8-bis(dimethylamino)naftalen
| 1,8-bis(dimethylamino)naftalen | |
|---|---|
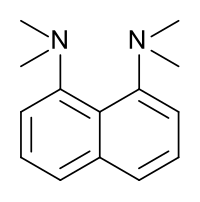 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | N1,N1,N8,N8-tetramethylnaftalen-1,8-diamin |
| Ostatní názvy | N,N,N',N'-tetramethylnaftalen-1,8-diamin |
| Funkční vzorec | C10H6[N(CH3)2]2 |
| Sumární vzorec | C14H18N2 |
| Vzhled | bílý krystalický prášek |
| Identifikace | |
| Registrační číslo CAS | 106-23-0 |
| EC-no (EINECS/ELINCS/NLP) | 203-376-6 |
| PubChem | 88675 |
| SMILES | CN(C)C1=CC=CC2=C1C(=CC=C2)N(C)C |
| InChI | InChI=1S/C14H18N2/c1-15(2)12-9-5-7-11-8-6-10-13(14(11)12)16(3)4/h5-10H,1-4H3 |
| Vlastnosti | |
| Molární hmotnost | 214,31 g/mol |
| Teplota tání | 47,8 °C (321,0 K) |
| Rozpustnost ve vodě | 3,12 mg/100 ml[1] |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H301 H302 H315 H319 H335[1] |
| P-věty | P261 P264 P270 P271 P280 P301+310 P301+312 P302+352 P304+340 P305+351+338 P312 P321 P330 P332+313 P337+313 P362 P403+233 P405 P501[1] |
Některá data mohou pocházet z datové položky. | |
1,8-Bis(dimethylamino)naftalen, triviálním názvem protonová houba je organická sloučenina se vzorcem C10H6[N(CH3)2]2. Patří mezi perinaftaleny, 1,8-disubstituované deriváty naftalenu. Díky své neobvyklé struktuře je velmi silnou zásadou.
Struktura a vlastnosti
[editovat | editovat zdroj]Tato látka je diaminem s dvěma dimethylaminovými skupinami navázanými na stejnou stranu (v poloze peri) na molekulu naftalenu. Vykazuje neobvykle silnou zásaditost a má též zajímavé spektroskopické vlastnosti.
S pKa 12,34[2] u konjugované kyseliny ve vodném roztoku je 1,8-bis(dimethylamino)naftalen jednou z nejsilnějších organických zásad. Takováto zásaditost je způsobována snížením napětí při protonaci a silnými interakcemi mezi volnými elektronovými páry na atomech dusíku.[3] Mnoho aromatických aminů má zásaditost naopak omezenou kvůli sp2 hybridizaci orbitalů dusíku, jehož volný pár zaujímá orbital 2p, interaguje s aromatickým jádrem a je z něj vytlačen. Toto u 1,8-bis(dimethylamino)naftalenu není možné, kvůli methylovým skupinám zabraňujícím molekule přejít do rovinného tvaru, ke kterému by bylo třeba tyto methylové skupiny odstranit a zásaditost tak není omezována vlivem, který se uplatňuje u jiných molekul. V molekule se vyskytují sterické efekty; díky jejich přítomnosti a současně silné zásaditosti se 1,8-bis(dimethylamino)naftalen používá v organické syntéze jako velmi selektivní nenukleofilní zásada.[2]
Tato látka má také vysokou afinitu k boru a může odštěpovat hydridové skupiny z boranu za vzniku párů boroniových a borohydridových iontů.[4]
Příprava
[editovat | editovat zdroj]1,8-Bis(dimethylamino)naftalen lze zakoupit, dá se rovněž připravit methylací 1,8-diaminonaftalenu jodmethanem nebo dimethylsulfátem.[5]
Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku 1,8-Bis(dimethylamino)naphthalene na anglické Wikipedii.
- ↑ a b c d e 1,8-Bis(dimethylamino)naphthalene. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ a b Alexander F. Pozharskii and Valery A. Ozeryanskii „Proton sponges and hydrogen transfer phenomena“ Mendeleev Commun., 2012, 22, 117–124. DOI:10.1016/j.mencom.2012.05.001
- ↑ R. W. Alder. Strain effects on amine basicities. Chemical Reviews. 1989, s. 1215–1223. DOI 10.1021/cr00095a015.
- ↑ Marc-André Légaré; Marc-André Courtemanche; Frédéric-Georges Fontaine. Lewis base activation of borane–dimethylsulfide into strongly reducing ion pairs for the transformation of carbon dioxide to methoxyboranes. Chemical Communications. 2014-08-28. Dostupné online. ISSN 1364-548X. DOI 10.1039/c4cc04857a.
- ↑ Vladimir I. Sorokin; Valery A. Ozeryanskii; Alexander F. Pozharskii. A Simple and Effective Procedure for the N-Permethylation of Amino-Substituted Naphthalenes. European Journal of Organic Chemistry. 2003, s. 496. DOI 10.1002/ejoc.200390085.
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu 1,8-bis(dimethylamino)naftalen na Wikimedia Commons
Obrázky, zvuky či videa k tématu 1,8-bis(dimethylamino)naftalen na Wikimedia Commons


