Elektroforéza

Elektroforéza je soubor separačních metod, které využívají k dělení látek jejich odlišnou pohyblivost ve stejnosměrném elektrickém poli. Na principu rozdílných elektroforetických mobilit se při ní dělí nabité molekuly (ionty).
Při separaci látek v kapiláře se zde vedle elektroforetického principu (pohyb nabitých molekul v elektrickém poli) uplatňuje též elektroosmotický tok (angl. electroosmotic flow, EOF), což je spontánní tok kapaliny v kapiláře v důsledku náboje (obvykle záporného) na vnitřní stěně kapiláry.
Historie[editovat | editovat zdroj]
V roce 1892 bylo publikováno, že anorganické částice v koloidním roztoku pod vlivem elektrického pole nenáhodně putují. Nedlouho poté byl tento jev popsán i u proteinů ve vodných roztocích.
V roce 1948 byl Nobelovou cenou oceněn švédský chemik Arne Tiselius, který ve 30. letech minulého století postavil aparaturu separující proteiny krevního séra na základě jejich elektroforetických mobilit.
Dělení[editovat | editovat zdroj]
Podle prostředí, ve kterém k separaci dochází, se elektroforetické metody dále dělí na:
- Kapilární zónová elektroforéza (CZE)
- Kapilární gelová elektroforéza (CGE)
- Elektroforéza v plynné fázi
- Iontová mobilní spektrometrie (IMS)
- Kapilární izotachoforéza (CITP)
- Kapilární izoelektrická fokusace (CIEF)
- Micelární elektrokinetická kapilární elektrochromatografie (MEKC)
- Kapilární elektrochromatografie (CEC)
Metody[editovat | editovat zdroj]
Kapilární zónová elektroforéza[editovat | editovat zdroj]

Kapilární zónová elektroforéza (též CZE z angl. Capillary Zone Electrophoresis) je druh elektroforézy, při níž jsou nabité molekuly unášeny elektroosmotickým tokem separačního pufru uvnitř kapiláry až k detektoru. Protože tyto ionty migrují v pufru rozdílnými elektroforetickými rychlostmi, dochází k separaci. Během jediného experimentu lze dělit a detekovat jak kladně, tak záporně nabité molekuly (ionty), ale také neutrální částice.
Kapilární gelová elektroforéza[editovat | editovat zdroj]
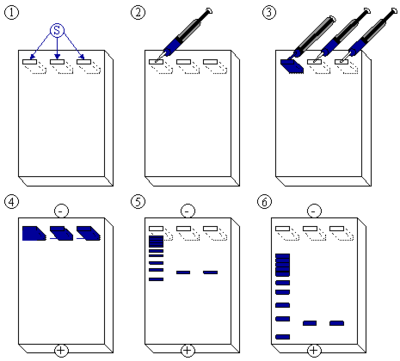
Kapilární gelová elektroforéza ( též CGE z angl. Capillary Gel Electrophoresis) je druh elektroforézy, při níž se látky rozdělují na základě pohyblivosti v gelu. V kapiláře se nachází gel, jenž maximalizuje diference mezi elektroforetickými rychlostmi velkých iontů různých tvarů, které různě úspěšně migrují póry gelu. Gel zabraňuje vzniku elektroosmotického toku, a proto jen jeden druh kladných či záporných iontů putuje směrem k detektoru.
Pohyblivost v gelu závisí na náboji separované molekuly a její molekulové hmotnosti, intenzitě elektrického pole a samozřejmě typu a porozitě gelu (k nejběžnějším gelům patří polyakrylamidový a agarosový gel).
Na rozdíl od CZE při CGE může být separován a detekován během jednoho experimentu pouze jeden typ iontů. Kapilární gelová elektroforéza se využívá zejména pro velké ionty, jakými jsou sacharidy, peptidy, bílkoviny, sestřihy DNA a RNA.
Existují i varianty této metody (elektroforéza v polyakrylamidovém gelu v přítomnosti dodecylsíranu sodného, angl. sodium-dodecyl-sulphate-polyacrylamide-gel-electrophoresis, SDS-PAGE), kde se molekuly bílkovin dělí téměř výhradně podle své molekulové hmotnosti.
Gelová elektroforéza je v současnosti nejrozšířenější elektroforetickou metodou.
Rychlost[editovat | editovat zdroj]
Rychlost elektroforézy lze vyjádřit následujícím vztahem:
- υ = C.E.ζ.εr.ε0/η
kde
- υ je lineární rychlost pohybu částice,
- C je parametr závisející na tvaru částic a tloušťce elektrické dvojvrstvy
- E je intenzita elektrického pole
- ζ je elektrokinetický potenciál
- εr je relativní permitivita kapaliny
- ε0 je permitivita vakua
- η je viskozita prostředí
Odkazy[editovat | editovat zdroj]
Literatura[editovat | editovat zdroj]
- GAŠ, Bohuslav. Kapilární elektroforéza. Vesmír. 2001, roč. 80, čís. 7, s. 370–373. Dostupné online. ISSN 1214-4029.
- BARTOVSKÁ, Lída; Marie. Co je co v povrchové a koloidní chemii [online]. Praha: VŠCHT, 2005. Kapitola Elektroforéza. Dostupné online.
- BARTOVSKÁ, Lída; Marie. Co je co v povrchové a koloidní chemii [online]. Praha: VŠCHT, 2005. Kapitola Měření elektrokinetických jevů. Dostupné online.
Související články[editovat | editovat zdroj]
- Izoelektrický bod
- Izoelektrická fokusace
- Kapilární elektroforéza
- Gelová elektroforéza
- SDS-PAGE
- Nativní elektroforéza proteinů
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu elektroforéza na Wikimedia Commons
Obrázky, zvuky či videa k tématu elektroforéza na Wikimedia Commons - (anglicky) Seznam relativní pohyblivosti
- (německy) Odborný portál elektrophorese.de
