Triethylboritan
| Triethylboritan | |
|---|---|
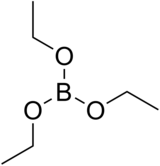 Vzorec | |
| Obecné | |
| Systematický název | Triethylboritan |
| Ostatní názvy | Triethoxid boritý; TEB; Triethylester kyseliny borité |
| Sumární vzorec | C6H15BO3 |
| Vzhled | Bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 150-46-9 |
| Vlastnosti | |
| Molární hmotnost | 149,99 g/mol |
| Teplota tání | −85 °C (188 K) |
| Teplota varu | 118 °C (391 K) |
| Hustota | 0,86 g/cm3 |
| Rozpustnost ve vodě | reaguje za vzniku CH3CH2OH a B(OH)3 |
| Rozpustnost v polárních rozpouštědlech | rozpustný v ethanolu |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| H-věty | H225 |
| P-věty | P210 P233 P260 |
| Teplota vznícení | 11 °C |
Některá data mohou pocházet z datové položky. | |
Triethylboritan (Někdy též triethoxid boritý či nepříliš správně triethylester kyseliny borité), někdy zkráceno na TEB je bezbarvá organická kapalná látka se vzorcem B(OCH2CH3)3.
Výroba[editovat | editovat zdroj]
Tato látka se vyrábí reakcí kyseliny borité a ethanolu:
B(OH)3 + 3CH3CH2OH ⇌ B(OCH2CH3)3 + 3H2O
V neutrálním prostředí reakce neprobíhá a udržuje se rovnováha mezi oběma stranami rovnice. S klesajícím pH (v kyselém prostředí) stoupá množství TEB a vody, zatímco v zasaditém prostředí vzniká více kyseliny borité (popř. boritanu) a vody.
Při výrobě se tedy používá okyselení kyselinou sírovou, následně se vzniklé produkty destilují. Na rozdíl od trimethylboritanu triethylboritan má vyšší teplotu varu, než voda, proto se „oddestilovává“ voda a nezreagovaný ethanol, a následně se oddělí novou destilací TEB od kyseliny sírové a nezreagované kyseliny borité.
Reakce[editovat | editovat zdroj]

TEB reaguje s vodou za vzniku ethanolu a kyseliny borité, proto musí být chráněn před vzdušnou vlhkostí.
Reaguje také se zásadami, např. hydroxidem sodným, dle rovnice:
B(OCH2CH3)3 + 3NaOH → 3CH3CH2OH + B(ONa)3
Látka je značně hořlavá. Teplota vzplanutí je asi 11 °C, tato látka hoří díky boru zeleným plamenem, ale podstatně méně výrazně než trimethylboritan (v porovnání s tím je plamen TEB namodralý). V případě, že TEB je kontaminován TMB, dojde ke značnému zbarvení do zelena (při výrobě TEB z technického lihu je plamen zelený pro obsah methanolu a následně i TMB). Tohoto efektu se užívá při kvalitativní analýze přítomnosti methanolu v ethanolu.
Hoření probíhá dle rovnice:
4B(OCH2CH3)3 + 39O2 → 4B2O3 + 30H2O + 24CO2
Reference[editovat | editovat zdroj]
- ↑ a b Triethyl borate. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
Související články[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Triethylboritan na Wikimedia Commons
Obrázky, zvuky či videa k tématu Triethylboritan na Wikimedia Commons



