Grubbsovy katalyzátory
| Grubbsův katalyzátor první generace | |
|---|---|
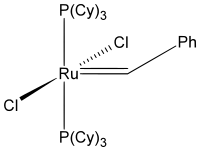 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | benzylidene-bis(tricyklohexylfosfino)-dichlororuthenium |
| Sumární vzorec | C43H72Cl2P2Ru |
| Vzhled | fialová pevná látka |
| Identifikace | |
| Registrační číslo CAS | 172222-30-9 |
| PubChem | 86306055 |
| SMILES | Cl[Ru-2](Cl)([P+](C1CCCCC1)(C1CCCCC1)C1CCCCC1)([P+](C1CCCCC1)(C1CCCCC1)C1CCCCC1)=Cc1ccccc1 |
| InChI | InChI=1S/C43H72P2.2ClH.Ru/c1-8-22-36(23-9-1)43(44(37-24-10-2-11-25-37,38-26-12-3-13-27-38)39-28-14-4-15-29-39)45(40-30-16-5-17-31-40,41-32-18-6-19-33-41)42-34-20-7-21-35-42;;;/h1,8-9,22-23,37-43H,2-7,10-21,24-35H2;2*1H;/q+2;;;+2/p-2 |
| Vlastnosti | |
| Molární hmotnost | 822,97 g/mol |
| Teplota tání | 153 °C (426 K) (rozklad) |
Některá data mohou pocházet z datové položky. | |
| Grubbsův katalyzátor druhé generace | |
|---|---|
 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | [1,3-bis-(2,4,6-trimethylfenyl)-2-imidazolidinyliden]dichloro(fenylmethylen)(tricyklohexylfosfino)ruthenium |
| Sumární vzorec | C46H65Cl2N2PRu |
| Vzhled | narůžověle hnědá pevná látka |
| Identifikace | |
| Registrační číslo CAS | 246047-72-3 |
| PubChem | 11147261 |
| SMILES | Cl[Ru-2](Cl)([c+]0n(-c1c(C)cc(C)cc1C)CCn0-c1c(C)cc(C)cc1C)([P+](C1CCCCC1)(C1CCCCC1)C1CCCCC1)=Cc1ccccc1 |
| InChI | InChI=1S/C21H26N2.C18H33P.C7H6.2ClH.Ru/c1-14-9-16(3)20(17(4)10-14)22-7-8-23(13-22)21-18(5)11-15(2)12-19(21)6;1-4-10-16(11-5-1)19(17-12-6-2-7-13-17)18-14-8-3-9-15-18;1-7-5-3-2-4-6-7;;;/h9-12H,7-8H2,1-6H3;16-18H,1-15H2;1-6H;2*1H;/q;;;;;+2/p-2 |
| Vlastnosti | |
| Molární hmotnost | 848,98 g/mol |
| Teplota tání | 143,5 až 148,5 °C (416,6 až 421,6 K) |
| Bezpečnost | |
| H-věty | H228 |
| P-věty | P210 P240 P241 P280 P378 |
Některá data mohou pocházet z datové položky. | |
| Hoveydův–Grubbsův katalyzátor první generace | |
|---|---|
 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | dichloro(o-isopropoxyfenylmethylen)(tricyklohexylfosfin)ruthenium |
| Sumární vzorec | C28H45Cl2OPRu |
| Vzhled | hnědá pevná látka |
| Identifikace | |
| Registrační číslo CAS | 203714-71-0 |
| PubChem | 24880901 |
| SMILES | Cl[Ru-2]2(Cl)([P+](C1CCCCC1)(C1CCCCC1)C1CCCCC1)=Cc1ccccc1[O+]2C(C)C |
| InChI | InChI=1S/C18H33P.C10H12O.2ClH.Ru/c1-4-10-16(11-5-1)19(17-12-6-2-7-13-17)18-14-8-3-9-15-18;1-8(2)11-10-7-5-4-6-9(10)3;;;/h16-18H,1-15H2;3-8H,1-2H3;2*1H;/q;;;;+2/p-2 |
| Vlastnosti | |
| Molární hmotnost | 600,61 g/mol |
| Teplota tání | 195 až 197 °C (468 až 470 K) |
| Bezpečnost | |
| H-věty | H228 |
| P-věty | P210 P240 P241 P280 P378 |
Některá data mohou pocházet z datové položky. | |
| Hoveydův–Grubbsův katalyzátor druhé generace | |
|---|---|
 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | [1,3-Bis-(2,4,6-trimethylfenyl)-2-imidazolidinyliden]dichloro(o-isopropoxyfenylmethylen)ruthenium |
| Sumární vzorec | C31H38Cl2N2ORu |
| Vzhled | zelená pevná látka |
| Identifikace | |
| Registrační číslo CAS | 301224-40-8 |
| EC-no (EINECS/ELINCS/NLP) | 608-446-3 |
| PubChem | 11763533 |
| SMILES | Cl[Ru-2]2(Cl)([c+]0n(-c1c(C)cc(C)cc1C)CCn0-c1c(C)cc(C)cc1C)=Cc1ccccc1[O+]2C(C)C |
| InChI | InChI=1S/C21H26N2.C10H12O.2ClH.Ru/c1-14-9-16(3)20(17(4)10-14)22-7-8-23(13-22)21-18(5)11-15(2)12-19(21)6;1-8(2)11-10-7-5-4-6-9(10)3;;;/h9-12H,7-8H2,1-6H3;3-8H,1-2H3;2*1H;/q;;;;+2/p-2 |
| Vlastnosti | |
| Molární hmotnost | 626,63 g/mol |
| Teplota tání | 216 až 220 °C (489 až 493 K) |
Některá data mohou pocházet z datové položky. | |
Grubbsovy katalyzátory jsou organické sloučeniny patřící mezi komplexy přechodných kovů, používané jako katalyzátory metateze olefinů; objevil je chemik Robert H. Grubbs. Bylo vyvinuto několik generací těchto katalyzátorů.[1][2]
Grubbsovy katalyzátory mohou být použity na mnoho různých funkčních skupin na alkenových substrátech i ve velkém počtu rouzdílných rozpouštědel a jsou na vzduchu stabilní.[3][4]
Díky těmto vlastnostem našly Grubbsovy katalyzátory široké využití v organické syntéze.[5]
Robert H. Grubbs byl za rozvoj metatezních reakcí oceněn v roce 2005 Nobelovou cenou za chemii, tu společně s ním získali také Richard Schrock a Yves Chauvin.
Katalyzátor první generace
[editovat | editovat zdroj]V 60. letech 20. století bylo zjištěno, že chlorid ruthenitý může katalyzovat metatezi olefinů a byly vytvořeny průmyslové procesy využívající tento objev. Tyto špatně definované, ale vysoce aktivní homogenní katalyzátory se poté začaly využívat průmyslově.[6] První dobře definovaný katalyzátor založený na rutheniu byl popsán v roce 1992.[7] Tento katalyzátor byl připraven z RuCl2(PPh3)4 a difenylcyklopropenu.
V roce 1995 nísledoval objev sloučeniny nyní známé jako Grubbsův katalyzátor první generace. Připravuje se z RuCl2(PPh3)3, fenyldiazomethanu a tricyklohexylfosfinu.[8][9]
Grubbsův katalyzátor první generace se stal prvním vytvořeným dobře definovaným katalyzátorem založeným na rutheniu a je také prekurzorem ostatních katalyzátorů Grubbsova typu.
Katalyzátor druhé generace
[editovat | editovat zdroj]Grubbsův katalyzátor druhé generace má stejné využití v organické syntéze jako katalyzátor první generace, ovšem vyznačuje se vyšší aktivitou. Je odolný vůči vlhkosti a stabilní na vzduchu, díky čemuž se v laboratoři snadněji skladuje.
Krátce před objevem Grubbsova katalyzátoru druhé generace byl nezávisle na sobě třemi různými týmy objeven katalyzátor odvozený od nenasyceného N-heterocyklického karbenu (1,3-bis(2,4,6-trimethylfenyl)imidazolu).[10][11][12] Následně Grubbs oznámil objev katalyzátoru druhé generace odvozeného od nasyceného N-heterocyklického karbenu (1,3-bis(2,4,6-trimethylfenyl)dihydroimidazolu):[13]
U nasycených i nenasycených katalytických komplexů je fosfinový ligand nahrazen N-heterocyklickým karbenem, který se vyskytuje i u všech odvozených katalyzátorů.[3]
Katalyzátory první i druhé generace jsou komerčně dostupné, stejně jako mnoho derivátů katalyzátoru druhé generace.
Hoveydovy–Grubbsovy katalyzátory
[editovat | editovat zdroj]U Hoveydových–Grubbsových katalyzátorů jsou na benzylidenové ligandy navázané chelatující ortho-isopropoxyskupiny napojené na benzenové kruhy. O-isopropoxybenzylidenová skupina bývá někdy nazývaná Hoveydův chelát. Chelatující atom kyslíku nahrazuje fosfinový ligand Grubbsova katalyzátoru druhé generace, což mu dodává úplně nefosfinovou strukturu. Hoveydův–Grubbsův katalyzátor první generace byl popsán roku 1999,[14] o rok později popsaly dva týmy téměř současně Hoveydův–Grubbsův katalyzátor druhé generace.[15][16] Hoveydovy–Grubbsovy katalyzátory jsou dražší a pomaleji iniciují reakce než příslušné Grubbsovy katalyzátory, ovšem díky lepší stabilitě se také používají často.[3] Změnou sterických a elektronových vlastností chelátu lze ovlivňovat rychlost iniciace.[17][18] Hoveydovy–Grubbsovy katalyzátory se snadno připravují z odpovídajících Grubbsových katalyzátorů adicí chelatujícího ligandu a látky zachytávající fosfinové skupiny, jako je například chlorid měďný:[16]
Hoveydovy–Grubbovy katalyzátory druhé generace lze také získat z Hoveydova–Grubbsova katalyzátoru první generace adicí N-heterocyklického karbenu:[15]
V jedné studii byl připraven ve vpdě rozpustný Grubbsův katalyzátor připojením polyethylenglykolového řetězce na imidazolidinovou skupinu.[19]
Tento katalyzátor se používá při metatezních reakcích s uzavíráním kruhu dienů s připojenými amonnými solemi (díky čemuž jsou rozpustné ve vodě) ve vodném prostředí.
Grubbsovy katalyzátory třetí generace (rychle iniciující katalyzátory)
[editovat | editovat zdroj]Rychlost reakcí využívajících Grubbsovy katalyzátory lze změnit nahrazením fosfinových ligandů méně stabilními pyridinovými ligandy. Při použití 3-brompyridinu probíhá iniciace více než milionkrát rychleji.[20]
Používají se pyridinové i 3-brompyridinové ligandy, přičemž bromovaný je 4,8krát nestabilnější, což vede k ještě rychlejším iniciacím.[21]
Katalyzátor se obvykle izoluje jako dvoupyridinový komplex, jeden pyridin se však ztrácí při rozpouštění a vratně inhibuje rutheniové centrum.
Hlavní využití rychle iniciujících katalyzátorů je při iniciaci polymerizací metatezemi s otevíráním kruhu. Díky této užitečnosti se rychle iniciující katalyzátory někdy označují jako Grubbsovy katalyzátory třetí generace.[22]
Vysoká rychlost iniciace oproti rychlosti propagace umožňuje využití těchto katalyzátorů při žįvých polymerizacích, přičemž vznikají polymery s nízkou polydisperzitou.[23]
Použití
[editovat | editovat zdroj]Grubbsovy katalyzátory se používají při metatezích olefinů. Při průmyslovém využití metateze olefinů se většinou používají heterogenní katalyzátory nebo katalytické systémy založené na chloridu ruthenitém.[6]
Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Grubbs catalyst na anglické Wikipedii.
- ↑ Robert H. Grubbs. Handbook of Metathesis. Weinheim: Wiley-VCH, 2003. ISBN 978-3-527-30616-9.
- ↑ Robert H. Grubbs; T. M. Trnka. Ruthenium in Organic Synthesis. Weinheim: Wiley-VCH, 2004. ISBN 9783527603831. DOI 10.1002/3527603832.ch6. Kapitola Ruthenium-Catalyzed Olefin Metathesis, s. 153–177.
- ↑ a b c G. C. Vougioukalakis; Robert H. Grubbs. Ruthenium-Based Heterocyclic Carbene-Coordinated Olefin Metathesis Catalysts. Chemical Reviews. 2010, s. 1746–1787. DOI 10.1021/cr9002424. PMID 20000700.
- ↑ T. M. Trnka; R. H. Grubbs. The Development of L2X2Ru=CHR Olefin Metathesis Catalysts: An Organometallic Success Story. Accounts of Chemical Research. 2001, s. 18–29. DOI 10.1021/ar000114f. PMID 11170353.
- ↑ Janine Cossy; Stellios Arseniyadis; Christophe Meyer. Metathesis in Natural Product Synthesis: Strategies, Substrates and Catalysts. Weinheim: Wiley-VCH, 2010. ISBN 978-3-527-32440-8.
- ↑ a b Lionel Delaude; Alfred F. Noels. Controlled Kirk-Othmer Encyclopedia of Chemical Technology. Weinheim: Wiley-VCH, 2005. ISBN 978-0471238966. DOI 10.1002/0471238961.metanoel.a01. Kapitola Metathesis.
- ↑ S. T. Nguyen; L. K. Johnson; R. H. Grubbs; J. W. Ziller. Ring-opening metathesis polymerization (ROMP) of norbornene by a Group VIII carbene complex in protic media. Journal of the American Chemical Society. 1992, s. 3974–3975. Dostupné online. DOI 10.1021/ja00036a053.
- ↑ P. Schwab; M. B. France; J. W. Ziller; R. H. Grubbs. A Series of Well-Defined Metathesis Catalysts – Synthesis of [RuCl2(=CHR′)(PR3)2] and Its Reactions. Angewandte Chemie International Edition. 1995, s. 2039–2041. DOI 10.1002/anie.199520391.
- ↑ P. Schwab; R. H. Grubbs; J. W. Ziller. Synthesis and Applications of RuCl2(=CHR′)(PR3)2: The Influence of the Alkylidene Moiety on Metathesis Activity. Journal of the American Chemical Society. 1996, s. 100–110. DOI 10.1021/ja952676d.
- ↑ J.-K. Huang; E. D. Stevens; S. P. Nolan; J. L. Petersen. Olefin Metathesis-Active Ruthenium Complexes Bearing a Nucleophilic Carbene Ligand. Journal of the American Chemical Society. 1999, s. 2674–2678. DOI 10.1021/ja9831352.
- ↑ M. Scholl; T. M. Trnka; J. P. Morgan; R. H. Grubbs. Increased Ring Closing Metathesis Activity of Ruthenium-Based Olefin Metathesis Catalysts Coordinated with Imidazolin-2-ylidene Ligands. Tetrahedron Letters. 1999, s. 2247–2250. DOI 10.1016/S0040-4039(99)00217-8.
- ↑ L. Ackermann; A. Fürstner; T. Weskamp; F. J. Kohl; W. A. Herrmann. Ruthenium Carbene Complexes with Imidazolin-2-ylidene Ligands Allow the Formation of Tetrasubstituted Cycloalkenes by RCM. Tetrahedron Letters. 1999, s. 4787–4790. DOI 10.1016/S0040-4039(99)00919-3.
- ↑ M. Scholl; S. Ding; C. W. Lee; R. H. Grubbs. Synthesis and Activity of a New Generation of Ruthenium-Based Olefin Metathesis Catalysts Coordinated with 1,3-Dimesityl-4,5-dihydroimidazol-2-ylidene Ligands. Organic Letters. 1999, s. 953–956. DOI 10.1021/ol990909q. PMID 10823227.
- ↑ Jason S. Kingsbury; Joseph P. A. Harrity; Peter J. Bonitatebus; Amir H. Hoveyda. A Recyclable Ru-Based Metathesis Catalyst. Journal of the American Chemical Society. 1999, s. 791–799. DOI 10.1021/ja983222u.
- ↑ a b S. Gessler; S. Randl; S. Blechert. Synthesis and metathesis reactions of phosphine-free dihydroimidazole carbene ruthenium complex. Tetrahedron Letters. 2000, s. 9973–9976. DOI 10.1016/S0040-4039(00)01808-6.
- ↑ a b S. B. Garber; J. S. Kingsbury; B. L. Gray; A. H. Hoveyda. Efficient and Recyclable Monomeric and Dendritic Ru-Based Metathesis Catalysts. Journal of the American Chemical Society. 2000, s. 8168–8179. DOI 10.1021/ja001179g.
- ↑ Origins of Initiation Rate Differences in Ruthenium Olefin Metathesis Catalysts Containing Chelating Benzylidenes. Journal of the American Chemical Society. 2015, s. 5782–5792. DOI 10.1021/jacs.5b01144. PMID 25897653.
- ↑ An Initiation Kinetics Prediction Model Enables Rational Design of Ruthenium Olefin Metathesis Catalysts Bearing Modified Chelating Benzylidenes. ACS Catalysis. 2018, s. 4600–4611. DOI 10.1021/acscatal.8b00843.
- ↑ Soon Hyeok Hong; Robert H. Grubbs. Highly Active Water-Soluble Olefin Metathesis Catalyst. Journal of the American Chemical Society. 2006, s. 3508–3509. Dostupné online. DOI 10.1021/ja058451c. PMID 16536510.
- ↑ J. A. Love; J. P. Morgan; T. M. Trnka; R. H. Grubbs. A Practical and Highly Active Ruthenium-Based Catalyst that Effects the Cross Metathesis of Acrylonitrile. Angewandte Chemie International Edition. 2002, s. 4035–4037. DOI 10.1002/1521-3773(20021104)41:21<4035::AID-ANIE4035>3.0.CO;2-I. PMID 12412073.
- ↑ Dylan J. Walsh; Sii Hong Lau; Michael G. Hyatt; Damien Guironnet. Kinetic Study of Living Ring-Opening Metathesis Polymerization with Third-Generation Grubbs Catalysts. Journal of the American Chemical Society. 2017-09-25, s. 13644–13647. ISSN 0002-7863. DOI 10.1021/jacs.7b08010. PMID 28944665.
- ↑ Anita Leitgeb; Julia Wappel; Christian Slugovc. The ROMP toolbox upgraded. Polymer. 2010, s. 2927–2946. DOI 10.1016/j.polymer.2010.05.002.
- ↑ T.-L. Choi; R. H. Grubbs. Controlled Living Ring-Opening-Metathesis Polymerization by a Fast-Initiating Ruthenium Catalyst. Angewandte Chemie International Edition. 2003, s. 1743–1746. DOI 10.1002/anie.200250632. PMID 12707895.
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu Grubbsovy katalyzátory na Wikimedia Commons
Obrázky, zvuky či videa k tématu Grubbsovy katalyzátory na Wikimedia Commons








