Mevalonátová dráha
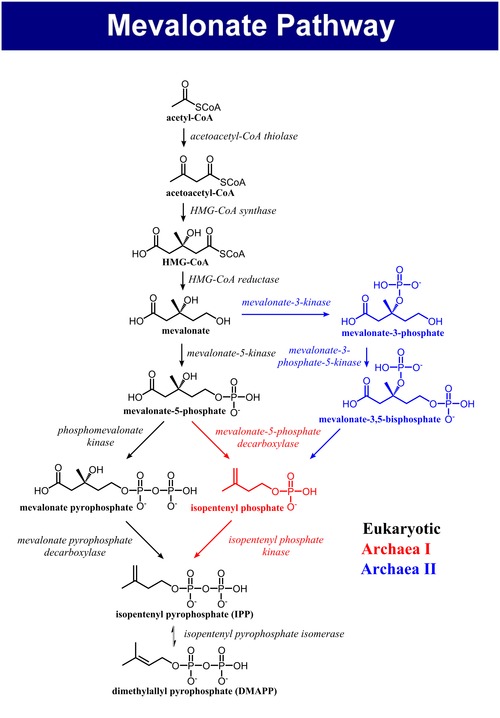
Mevalonátová dráha, také nazývaná isoprenoidová dráha nebo HMG-CoA reduktázová dráha je metabolická dráha přítomná u eukaryot, archeí a některých bakterií.[1] Vznikají při ní dva pětiuhlíkaté stavební prvky - isopentenylpyrofosfát (IPP) a dimethylallylpyrofosfát (DMAPP), které slouží k syntéze izoprenoidů, skupiny biomolekul, kam patří například cholesterol, vitamin K, koenzym Q10 a steroidní hormony.[2]
Výchozí látkou mevalonátové dráhy je acetylkoenzym A (acetyl-CoA) a konečnými produkty IPP a DMAPP.[3] Na mevalonátovou dráhu jsou zaměřena léčiva ze skupiny statinů, sloužící ke snižování koncentrace cholesterolu v krvi, která inhibují HMG-CoA-reduktázu, enzym, jenž je součástí této dráhy.
Svrchní část
[editovat | editovat zdroj]Mevalonátová dráha má u eukaryot, archeí i bakterií stejný začátek. Zdrojem uhlíku je acetyl-CoA. V prvním kroku kondenzují dvě molekuly acetyl-CoA na acetoacetyl-CoA. Následně dojde ke druhé kondenzací, čímž vznikne HMG-CoA (3-hydroxy-3-methyl-glutaryl-CoA). Redukcí HMG-CoA se tvoří (R)-mevalonát. Tyto kroky se označují jako svrchní mevalonátová dráha.[4]
Spodní část
[editovat | editovat zdroj]Spodní mevalonátová dráha přeměňuje (R)-mevalonát na IPP a DMAPP a má 3 varianty. U eukaryot je mevalonát dvakrát fosforylován v pozici 5-OH a poté dekarboxylován na IPP.[4] U některých archeí, jako je Haloferax volcanii, je mevalonát jednou fosforylován v pozici 5-OH, dekarboxylován na izopentenylfosfát (IP) a nakonec fosforylován za vzniku IPP, tato varianta se nazývá archeální mevalonátová dráha I.[5] Třetí variantou, popsanou například u Thermoplasma acidophilum, dochází k fosforylaci mevalonátu v pozici 3-OH a poté v pozici 5-OH. Vzniklý metabolit, mevalonát-3,5-bisfosfát, se dekarboxyluje na IP a nakonec fosforyluje na IPP (zde jde o archeální mevalonátovou dráhu I).[6][7]
Regulace
[editovat | editovat zdroj]Existuje několik enzymů, které mohou být aktivovány transkripční regulací pomocí aktivace SREBP. Tento nitrobuněčný senzor detekuje nízké koncentrace cholesterolu a stimuluje jeho endogenní tvorbu v HMG-CoA reduktázové dráze, podobně jako navýšení vstřebávání lipoproteinů regulací LDL receptoru. Regulace této dráhy může také probíhat skrz ovlivňování translace mRNA, degradace reduktázy a fosforylace.[1]
Farmakologický význam
[editovat | editovat zdroj]Na mevalonátovou dráhu se zaměřuje několik druhů léčiv:
- Statiny (snižují koncentraci cholesterolu v krvi);
- Bisfosfonáty (používané k léčbě kostních degenerativních onemocnění)
Vliv nemocí
[editovat | editovat zdroj]Mevalonátovou dráhu ovlivňují tyto nemoci:
- Deficit mevalonátkinázy
- Mevalonová acidurie
- Hyperimunoglobulinemický D syndrom (HIDS).
Alternativní dráhy
[editovat | editovat zdroj]Rostliny, většina bakterií a někteří prvoci mohou vytvářet izoprenoidy jiným způsobem nazývaným methylerythritolfosfátová (MEP) nebo nemevalonátová dráha.[8] Konečnými produkty mevalonátové i MEP dráhy jsou IPP a DMAPP, enzymatické reakce přeměňující acetyl-CoA na IPP jsou však odlišné. U vyšších rostlin MEP probíhá v plastidech, zatímco mevalonátová dráha v cytosolu.[8] K bakteriím využívajícím MEP dráhu patří například Escherichia coli a Mycobacterium tuberculosis.
Přehled reakcí
[editovat | editovat zdroj]| Enzym | Reakce | Popis |
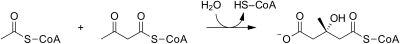
| Acetoacetyl-CoA thioláza |  |
Acetyl-CoA (citrátový cyklus) kondenzuje s dalším acetyl-CoA za vzniku acetoacetyl-CoA |
| HMG-CoA syntáza | Acetoacetyl-CoA kondenzuje s acetyl-CoA na 3-hydroxy-3-methylglutaryl-CoA (HMG-CoA). | |
| HMG-CoA reduktáza |  |
HMG-CoA je pomocí NADH redukován na mevalonát. Tento krok při syntéze cholesterolu určuje rychlost reakce, a proto je vhodným cílem léčiv (statinů). |
| Mevalonát-5-kináza | 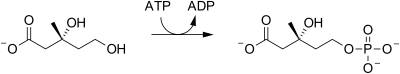 |
Mevalonát je fosforylován v pozici 5-OH za vzniku mevalonát-5-fosfátu. |
| mevalonát-3-kináza | 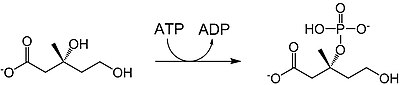 |
Mevalonát je fosforylován na pozici 3-OH za tvorby mevalonát-3-fosfátu. Spotřebuje se jeden ekvivalent ATP. |
| mevalonát-3-fosfát-5-kináza |  |
Mevalonát-3-fosfát je fosforylován na pozici 5-OH za vzniku fosfomevalonátu. Spotřebuje se jeden ekvivalent ATP. |
| fosfomevalonátkináza |  |
Mevalonát-5-fosfát se fosforyluje na mevalonát-5-pyrofosfát. Spotřebuje se jeden ekvivalent ATP. |
| mevalonát-5-pyrofosfátdekarboxyláza |  |
Mevalonát-5-pyrofosfát se dekarboxyluje za tvorby isopentenylpyrofosfátu (IPP). Spotřebuje se 1 ekvivalent ATP. |
| isopentenylpyrofosfátizomeráza | 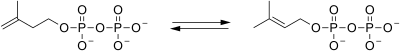 |
Isopentenylpyrofosfát je izomerizován na dimethylallylpyrofosfát. |
Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Mevalonate pathway na anglické Wikipedii.
[1] [2] [3] [4] [5] [6] [7] [8]
- ↑ a b c Buhaescu I, Izzedine H (2007) Mevalonate pathway: areview of clinical and therapeutical implications. ClinBiochem 40:575–584.
- ↑ a b Holstein, S. A., and Hohl, R. J. (2004) Isoprenoids: Remarkable Diversity of Form and Function. Lipids 39, 293–309
- ↑ a b Goldstein, J. L., and Brown, S. B. (1990) Regulation of the mevalonate pathway. Nature 343, 425–430
- ↑ a b c Miziorko H (2011) Enzymes of the mevalonate pathway of isoprenoid biosynthesis. Arch Biochem Biophys 505:131-143.
- ↑ a b Dellas, N., Thomas, S. T., Manning, G., and Noel, J. P. (2013) Discovery of a metabolic alternative to the classical mevalonate pathway. eLife 2, e00672
- ↑ a b Vinokur JM, Korman TP, Cao Z, Bowie JU (2014) Evidence of a novel mevalonate pathway in archaea. Biochemistry 53:4161–4168.
- ↑ a b Azami Y, Hattori A, Nishimura H, Kawaide H, YoshimuraT, Hemmi H (2014) (R)-mevalonate-3-phosphate is an intermediate of the mevalonate pathway in Thermoplasma acidophilum. J Biol Chem 289:15957–15967.
- ↑ a b c Banerjee A, Sharkey TD. (2014) Methylerythritol 4-phosphate (MEP) pathway metabolic regulation. Nat Prod Rep 31:10431055
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu Mevalonátová dráha na Wikimedia Commons
Obrázky, zvuky či videa k tématu Mevalonátová dráha na Wikimedia Commons