Jappova–Klingemannova reakce
Jappova–Klingemannova reakce je organická reakce sloužící k přípravě hydrazonů z β-ketokyselin (nebo jejich esterů) a arylových diazoniových solí.[1][2][3][4][5][6] Objevili ji němečtí chemici Francis Robert Japp a Felix Klingemann.
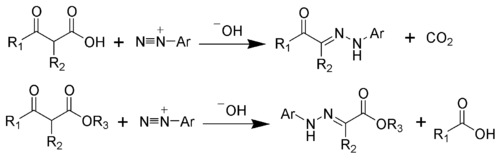
Hydrazony získané Jappovou–Klingemannovou reakcí se používají jako meziprodukty při syntéze složitějších organických sloučenin, například fenylhydrazony mohou být zahřívány za přítomnosti silné kyseliny a vytvářet tak indoly ve Fischerově syntéze.[7][8]
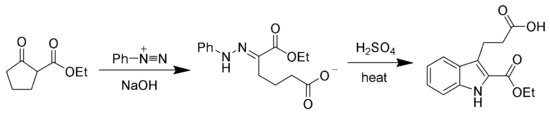
Mechanismus
K popisu mechanismu Jappovy–Klingemannovy reakce je použita reakce esteru β-ketokyseliny. V prvním kroku je β-ketoester deprotonován. Nukleofilní adicí enolátového aniontu 2 na diazoniovou sůl vznikne azosloučenina 3, která se hydrolýzou přemění na meziprodukt 4, jenž se rychle rozkládá na karboxylovou kyselinu 6. Po výměně vodíku se vytvoří konečný produkt 7.

Reference
V tomto článku byl použit překlad textu z článku Japp–Klingemann reaction na anglické Wikipedii.
- ↑ Francis Robert Japp; Felix Klingemann. Ueber Benzolazo- und Benzolhydrazofettsäuren. Berichte der deutschen chemischen Gesellschaft. 1887, s. 2942–2944. Dostupné online. DOI 10.1002/cber.188702002165.
- ↑ Francis Robert Japp; Felix Klingemann. Zur Kenntniss der Benzolazo- und Benzolhydrazopropionsäuren. Berichte der deutschen chemischen Gesellschaft. 1887, s. 3284–3286. DOI 10.1002/cber.188702002234.
- ↑ Francis Robert Japp; Felix Klingemann. Ueber sogenannte »gemischte Azoverbindungen. Berichte der deutschen chemischen Gesellschaft. 1887, s. 3398–3401 url = https://zenodo.org/record/1425491. DOI 10.1002/cber.188702002268.
- ↑ Francis Robert Japp; Felix Klingemann. Ueber die Constitution einiger sogenannten gemischten Azoverbindungen. Liebigs Annalen der Chemie. 1888, s. 190–225. DOI 10.1002/jlac.18882470208.
- ↑ Phillips, R. R. Org. React. 1959, 10, 143.
- ↑ Reynolds, G. A.; VanAllan, J. A. Organic Syntheses, Coll. Vol. 4, p.633 (1963); Vol. 32, p.84 (1952)(Article Archivováno 16. 7. 2012 na Wayback Machine.)
- ↑ R. E. Bowman; T. G. Goodburn; A. A. Reynolds. 1,3,4,5-Tetrahydrobenz[cd]indoles and related compounds. Part I. A new synthesis of 3,4-dihydrobenz[cd]indol-5(1H)-one (Uhle's ketone). Journal of the Chemical Society, Perkin Transactions 1. 1972, s. 1121. DOI 10.1039/P19720001121.
- ↑ M. D. Meyer; L. I. Kruse. Ergoline synthons: Synthesis of 3,4-dihydro-6-methoxybenz[cd]indol-5(1H)-one (6-methoxy-Uhle's ketone) and 3,4-dihydrobenz[cd]indol-5(1H)-one (Uhle's ketone) via a novel decarboxylation of indole-2-carboxylates. The Journal of Organic Chemistry. 1984, s. 3195–3199. DOI 10.1021/jo00191a028.
Externí odkazy
 Obrázky, zvuky či videa k tématu Jappova-Klingemannova reakce na Wikimedia Commons
Obrázky, zvuky či videa k tématu Jappova-Klingemannova reakce na Wikimedia Commons
