Čtvercově pyramidální molekulová geometrie
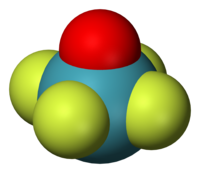
Čtvercově pyramidální molekulová geometrie je druh molekulové geometrie u molekul typu ML5, kde L je ligand. Pokud jsou atomy ligandu navzájem propojeny, tak molekula zaujme tvar čtyřbokého jehlanu a grupa symetrie je pak C4v. Tato geometrie je častá u některých sloučenin prvků hlavní skupiny, které mají, podle teorie VSEPR, stereochemicky aktivní volné elektronové páry. Některé sloučeniny, například [Ni(CN)5]3− vytváří trigonálně bipyramidální i čtvercově pyramidální struktury.[1]
Jako přechodný stav při Berryho pseudorotacích
[editovat | editovat zdroj]Trigonálně bipyramidální molekuly procházejí Berryho pseudorotací, která probíhá přes meziprodukt se čtvercově pyramidální geometrií; z tohoto důvodu se taková geometrie málokdy vyskytuje v základních stavech molekul, ale lze ji vytvořit i malým narušením trigonální bipyramidy.
Pseudorotace nastává i u čtvercově pyramidálních molekul. Takové molekuly se vyznačují, oproti trigonálně bipyramidálním, silnějšími vibracemi. Mechanismus je podobný Berryovu.
Příklady
[editovat | editovat zdroj]Ke sloučeninám se čtvercově pyramidální geometrií patří mimo jiné oxyfluorid xenonový (XeOF4),[2] pentafluoridy halogenů (XF5, kde X = Cl, Br, I).[3][4] a vanadičité komplexy, například vanadylacetylacetonát, [VO(acac)2] (acac = acetylacetonát, anion odvozený od acetylacetonu).
Odkazy
[editovat | editovat zdroj]Reference
[editovat | editovat zdroj]V tomto článku byl použit překlad textu z článku Square pyramidal molecular geometry na anglické Wikipedii.
- ↑ Thomas G. Spiro; Aristides Terzis; Kenneth N. Raymond. tructure of Ni(CN) 3−
5 . Raman, infrared, and x-ray crystallographic evidence. Inorganic Chemistry. 1970, s. 2415. DOI 10.1021/ic50093a006. - ↑ Square Pyramidal Molecular Geometry. VSEPR [online]. Dostupné v archivu pořízeném z originálu dne 2009-11-02.
- ↑ Square Pyramidal Molecular Geometry [online]. Dostupné online.
- ↑ G. L. Miessler; D. A. Tarr. Inorganic Chemistry. [s.l.]: Pearson/Prentice Hall, 2004. Dostupné online. ISBN 0-13-035471-6.
