Fosfidy
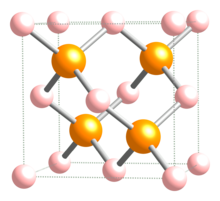

Fosfid je sloučenina fosforu s nějakým méně elektronegativním prvkem nebo prvky. Dvouprvkové sloučeniny tvoří fosfor s většinou prvků s výjimkou rtuti, olova, antimonu, bizmutu, telluru a polonia.[1] Poměr prvků ve fosfidech může být poměrně variabilní, například draslík tvoří devět fosfidů: K3P, K4P3, K5P4, KP, K4P6 K3P7, K3P11, KP10.3, KP15), nikl jich má osm (Ni3P, Ni5P2, Ni12P5, NiP2, Ni5P4, NiP, NiP2, NiP3).[1] Většina jich je dobře rozpustná v tucích.
Třídění
Třídění fosfidů je komplikované.[2] Na základě struktury a reaktivity mohou být fosfidy klasifikovány do těchto skupin:[1]:
- fosfidy iontové, obsahující anionty P3−. Tvoří je alkalické kovy (M3P, např. Na3P) a kovy alkalických zemin (M3P2, např. Ca3P2)
- polyfosfidy obsahující např. iont P24−, iont P113−; polymerní řetězcovité ionty (např. šroubovicovitý P−)n a některé trojrozměrné složité struktury)
- fosfidy s jedním atomem fosforu, polovodiče (např. GaP) až vodiče (TaP)[3]
Polyfosfidové ionty P34− (vyskytující se v K4P3) a P45− (vyskytující se v K5P4) jsou radikálové anionty s lichým počtem valenčních elektronů, což z nich činí paramagnetické látky.[1]
Výskyt v přírodě
Schreibersit – vzorec (Fe,Ni)3P, je běžně přítomen v některých druzích meteoritů.[4][5]
Reference
V tomto článku byl použit překlad textu z článku phosphide na anglické Wikipedii.
- ↑ a b c d VON SCHNERING,, H.G.; HÖNLE, W. Encyclopedia of Inorganic Chemistry. [s.l.]: John wiley & Sons, 1994. ISBN 0471936200. Kapitola Phosphides - Solid state chemistry.
- ↑ GREENWOOD, Norman N.; EARNSHAW, A. Chemistry of the Elements. 2. vyd. Oxford: Butterworth-Heinemann, 1997. ISBN 0-7506-3365-4.
- ↑ C. S. Blackman, C. J. Carmalt, S. A. O'Neill, I. P. Parkin, K. C. Molloy, L. Apostolico. Chemical vapour deposition of group Vb metal phosphide thin films. J. Mater. Chem.. 2003, čís. 13.
- ↑ Mindat
- ↑ Handbook of Mineralogy

