Elektrosprejová ionizace

Elektrosprejová ionizace (ESI) je ionizační technika v hmotnostní spektrometrii, která k tvorbě iontů využívá elektrosprej, ve kterém je na kapalinu aplikováno vysoké elektrické napětí, čímž se utvoří aerosol. Tato metoda je vhodná k ionizaci makromolekul, protože překonává tendence těchto molekul k fragmentaci při ionizování. ESI se od ostatních způsobů ionizace (například matricí asistované laserové desorpce/ionizace (MALDI) liší tím, že může vytvářet ionty s vícenásobným nábojem, čímž rozšiřuje oblast molekulových hmotností sloučenin, které lze analyzovat (kDa až MDa).[1][2]
Hmotnostní spektrometrie využívající ESI se nazývá hmotnostní spektrometrie s elektrosprejovou ionizací (ESI-MS) nebo, méně často, elektrosprejová hmotnostní spektrometrie (ES-MS). ESI patří mezi „měkké“ ionizační metody, protože u ní dochází jen k minimální fragmentaci. Toto může být výhodné tím, že jsou téměř vždy pozorovány molekulové ionty, nevýhodou je malé množství informací o struktuře, které lze získat z jednoduchého spektra. Tuto nevýhodu lze vyrovnat spojením ESI a tandemové hmotnostní spektrometrie (ESI-MS/MS).
Elektrosprejová ionizace byla popsána v roce 1984.[3] Za rozvoj jejího využití k analýze biologických makromolekul[4] získal John Bennett Fenn v roce 2002 Nobelovu cenu za chemii.[5]
Historie[editovat | editovat zdroj]

V roce 1882 Lord Rayleigh teoreticky odhadl největší náboj, který může být na kapce před jejím rozpadem na proud kapaliny.[6] Ten se označuje jako Rayleighova mez.
V roce 1914 John Zeleny prozkoumal vlastnosti kapek na koncích skleněných kapilár a našel možnost existence několika režimů elektrospreje.[7]
Ve 20. letech 20. století se výzkumem elektrospreje zabývali C. T. Wilson a Geoffrey Ingram Taylor,[8] stejně jako J. J. Nolan,[9] a v roce 1931 zveřejnil práci na toto téma W. A. Macky.[10]
Geoffrey Ingram Taylor vyvinul elektrosprejový kužel (nyní nazývaný Taylorův kužel).[11]
První propojení elektrosprejové ionizace s hmotnostní spektrometrií popsal Malcolm Dole roku 1968.[12][13]
John Bennett Fenn získal v roce 2002 Nobelovu cenu za chemii za rozvoj hmotnostní spektrometrie s elektrosprejovou ionizací v 80. letech 20. století.[14]
Mechanismus ionizace[editovat | editovat zdroj]

Kapalina obsahující zkoumané analyty se elektrosprejem rozptyluje do podoby jemného aerosolu.[15] Jelikož se při tvorbě iontů prudce odpařuje rozpouštědlo, tak se rozpouštědla pro elektrosprejovou ionizaci obvykle připravují smícháním vody s těkavou organickou sloučeninou (například methanolem[16] nebo acetonitrilem). Aby se zmenšila velikost kapek, tak se do vzorků často přidávají sloučeniny zvyšující elektrickou vodivost, jako je kyselina octová. Tyto látky také slouží jako zdroje protonů usnadňující ionizaci. Vysokoprůtokové elektrospreje mohou být rozprašovány zahřátým inertním plynem, například dusíkem nebo oxidem uhličitým, který se za vysoké teploty aplikuje do ESI zdroje.[17] Aerosol se aplikuje do první vakuové komory hmotnostního spektrometru kapilárou s rozdílem potenciálů okolo 3000 V, která může být zahřívána, aby se usnadnilo odpařování rozpouštědla z nabitých kapek. Rozpouštědlo se odpařuje tak dlouho, dokud se kapky nestanou nestabilními kvůli dosažení Rayleighovy meze. V tuto chvíli se kapky v důsledku elektrostatického odpuzování souhlasných nábojů začnou rozpadat.[18] V tomto okamžiku u kapek dojde ke coulombovskému štěpení, kdy původní kapky 'explodují' za vzniku mnoha menších a stabilnějších. U nich se po odpaření rozpouštědla objevují další coulombovská štěpení. Během štěpení kapky ztrácejí část hmotnosti (1,0 až 2,3 %) a náboje (10 až 18 %).[19][20]
Existují dvě hlavní teorie vysvětlující tvorbu iontů v plynné fázi: model iontového odpařování (IEM) a model nabitých zbytků (CRM). IEM předpokládá, že jakmile průměr kapky dosáhne určité hodnoty, tak se intenzita elektrického pole na jejím povrchu zvětší natolik, že začne přispívat k desorpci solvatovaných iontů.[21][22]
Podle CRM kapky elektrospreje podstupují cykly odpařování a štěpení, což vede ke vzniku drobných kapek obsahujících průměrně jeden ion analytu nebo i méně.[12] Ionty v plynné fázi se vytvoří po odpaření zbývajících molekul rozpouštědla a výsledkem je analyt s nábojem původních kapek.
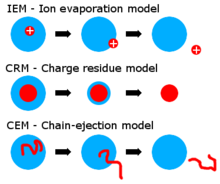
Byla získána řada přímých i nepřímých důkazů o tom, že malé ionty (vzniklé z malých molekul) jsou do plynné fáze uvolňovány iontovým odpařováním,[22][23][24] zatímco větší ionty (například odvozené od bílkovin) se vytváří mechanismem nabitých zbytků.[24]
Existuje také třetí model, který spojuje oba výše uvedené.[25] Pro nesložené bílkoviny byl navržen další model označovaný CEM.[26] Ionty pozorované ve hmotnostní spektrometrii mohou být kvazimolekulární ionty vzniklé adicí vodíkového kationtu a být označovány [M + H]+, nebo jiného kationtu, například sodného (vzniklé ionty mají vzorec [M + Na]+) nebo odstraněním vodíkového kationtu (pak je vzorec iontu [M − H]−). Často bývají pozorovány rovněž ionty s vícenásobnými náboji ([M + nH]n+). U makromolekul může vznikat velké množství nabitých stavů, čímž se tvoří charakteristická obálka. Všechny tyto částice obsahují sudý počet elektronů: samotné elektrony nejsou na rozdíl od mnoha jiných ionizačních metod připojovány ani odštěpovány. Analyty někdy vstupují do elektrochemických dějů, které mění vzhled hmotnostního spektra. Tento jev je možné ukázat u přímé ionizace ušlechtilých kovů, jako jsou měď, stříbro a zlato, pomocí elektrospreje.[27]
Účinnost tvorby iontů v plynné fázi u malých molekul závisí na struktuře sloučeniny, použitém rozpouštědle a vlastnostech přístroje.[28]
Rozdíl v účinnosti ionizace může být více než milionnásobný.
Varianty[editovat | editovat zdroj]
Elektrospreje vznikající při nízkých průtocích vytvářejí menší původní kapky, což vede k vyšší účinnosti ionizace. V roce 1993 D. C. Gale a Richard D. Smith popsali výrazný nárůst citlivosti při nízkých průtocích vzorku, které se podařilo snížit až na 200 nl/min.[29] V roce 1994 použily dvě výzkumné skupiny pro elektrospreje vznikající za nízkých průtoků označení mikroelektrosprej (mikrosprej). Emmett a Caprioli přišli na to, že výkonnost analýzy pomocí HPLC-MS lze zlepšit úpravou průtoku na 300–800 nl/min.[30]
M. S. Wilm a M. Mann ukázali, že kapilární průtok o hodnotě kolem 25 nl/min může udržet velikost kapek elektrospreje na několika mikrometrech.[31] Mann pro tento postup použil v roce 1996 označení nanoelektrosprej (nanosprej).[32]
Hranice mezi elektrosprejem, mikrosprejem a nanosprejem není přesně určena.[33] V jedné studii byly zkoumány „změny v rozdělení analytu během štěpení kapek před uvolněním iontů“.[33] V této práci byly porovnávány výsledky získané třemi jinými skupinami.[31][34][35] a následně byl měřen poměr intenzity signálu [Ba2+ + Ba+]/[BaBr+] při různých hodnotách průtoku.
Ionizace chladným sprejem je elektrosprejová ionizace, při které vzorek prochází tenkou chladnou kapilárou (o teplotě 10 až 80 °C) do elektrického pole, kde vytváří mlhu chladných nabitých kapek.[36] Tato metoda se používá například při analýze málo odolných molekul a interakcí, které nelze zkoumat při použití běžné elektrosprejové ionizace.
Elektrosprejovou ionizaci lze provést i za tlaku okolo 3 kPa a vyšších teplot pomocí nanoelektrospreje v dvoufázovém rozhraní (SPIN); tento postup vyvinul Richard D. Smith.[37] Zavedení metody SPIN umožnilo navýšit citlivost analýzy díky možnosti přesunout ionty do oblastí s nižším tlakem. Nanoelektrosprejové přístroje obsahují tenké kapiláry o vnitřním průměru 1 až 3 mikrometrů. K zajištění dostatečné vodivosti jsou tyto kapiláry pokryty vodivými materiály, například zlatem. Při nanoelektrosprejové ionizaci se použije pouze několik mikrolitrů vzorku a tvoří se menší kapky.[38]
Provedení za nízkého tlaku je obzvláště vhodné pro nízké průtoky, kde menší velikost kapek elektrospreje umožňuje účinnou desolvataci a tvorbu iontů. Podařilo se dosáhnout až 50% účinnosti ionizace při přesunu iontů z kapalné do plynné fáze a přes duální rozhraní do hmotnostního spektrometru.[39]

Tvorbu iontů lze také provést mimo hmotnostní spektrometr bez přípravy vzorku.[40][41][42]
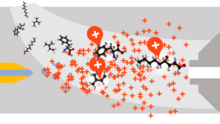
Desorpční elektrosprejová ionizace (DESI) je metoda ionizace, při níž je elektrosprej rozpouštědla nasměrován na vzorek.[43][44]
Elektrosprej je přitahován povrchem vzorku díky působení elektrického napětí. Sloučeniny obsažené ve vzorku jsou extrahovány do rozpouštědla, které je opětovně aerosolizováno na nabité kapky, jež se odpařují a zanechávají vysoce nabité ionty. Po ionizaci procházejí ionty tlakovým rozhraním hmotnostního spektrometru. DESI umožňuje ionizaci za atmosférického tlaku s minimální přípravou vzorku.
Další metodou je extrakční elektrosprejová ionizace, při které se používají dva spojené spreje, přičemž jeden z nich je vytvářen elektrosprejem.[41]
Laserová elektrosprejová ionizace je dvoufázový postup, při kterém se používá pulsní laser k desorbci vzorku, který interaguje s elektrosprejem, čímž se tvoří ionty.[41] Vzorek se shromažďuje na terči v blízkosti elektrospreje. Laser desorbuje nebo ablatuje materiál vzorku, ten se oddělí z povrchu a vstupuje do elektrospreje, kde vznikají ionty. Příklady metod založených na tomto postupu jsou elektrosprejová laserová desorpční ionizace, matricí asistovaná laserová desorpce s elektrosprejovou ionizací a elektrosprejová ionizace s laserovou ablací.
Elektrostatická sprejová ionizace (ESTASI) je metoda analýzy vzorků uložených na plochém či porézním povrchu, případně v mikrokanálu. Kapky obsahující analyty se ukládají do místa pro vzorek, na které je přivedeno pulsní vysoké napětí. Jakmile je elektrostatický tlak větší než povrchové napětí, tak se uvolní sprej iontů a kapek.
Při sekundární elektrosprejové ionizaci (SESI) se vytváří nabíjející ionty podobným způsobem jako elektrosprej. Tyto ionty následně srážkami nabíjí molekuly páry.[45][46]
U papírové sprejové ionizace se vzorek aplikuje na kousek papíru, přidá se rozpouštědlo a na papír je přivedeno vysoké napětí, čímž začnou vznikat ionty.
Použití[editovat | editovat zdroj]

Elektrosprejová ionizace se používá při výzkumu skládání proteinů.[47][48][49]
Kapalinová chromatografie s hmotnostní spektrometrií[editovat | editovat zdroj]
Elektrosprejová ionizace je jedním z možných zdrojů iontů při spojení kapalinové chromatografie s hmotnostní spektrometrií (LC-MS). Analýzu je možné provést elucí vzorku z chromatografického sloupce přímo do elektrospreje nebo shromážděním částí vzorku, které jsou později analyzovány nanoelektrosprejovou hmotnostní spektrometrií. Jedním z řady provozních parametrů ESI-MS při analýze bílkovin[50] je napětí elektrospreje.[51] Byl také zkoumán vliv složení rozpouštědla,[52] (například kyseliny trifluoroctové[53] nebo octanu amonného[20] či supernabíjejících činidel[54][55][56][57], derivatizující skupiny[58]) či podmínek tvorby spreje[59] na spektra LCMS s elektrosprejovou ionizací a na nanoESI-MS spektra.[60]
Kapilární elektroforéza s hmotnostní spektrometrií (CE-MS)[editovat | editovat zdroj]
Použití kapilární elektroforézy s hmotnostní spektrometrií s elektrosprejovým rozhraním vyvinul Richard D. Smith se svými spolupracovníky a potvrdil jeho využitelnost při analýze směsí malých molekul a rozšířil jej na úroveň celé biologické buňky.
Výzkum nekovalentních interakcí v plynné fázi[editovat | editovat zdroj]
Electrosprejovou ionizaci je také možné využít k výzkumu nekovalentních interakcí v plynné fázi. Elektrosprejový proces může přenášet nekovalentní komplexy z kapalné do plynné fáze bez narušení nekovalentních interakcí. Při tomto použití se vyskytují potíže,[20][61] jako jsou nespecifické interakce[62] zjištěné při zkoumání ligand-substrátových komplexů pomocí ESI-MS nebo nanoESI-MS. Příkladem může být výzkum interakcí mezi enzymy a léčivy, která je inhibují.[63][64][65]
Při studiích interakcí mezi STAT6 a inhibitory[65][66][67] byla elektrosprejová ionizace použita jako nástroj k hledání možných nových léčiv.
Odkazy[editovat | editovat zdroj]
Související články[editovat | editovat zdroj]
Literatura[editovat | editovat zdroj]
- Cole, Richard. Electrospray ionization mass spectrometry: fundamentals, instrumentation, and applications. New York: Wiley, 1997. ISBN 978-0-471-14564-6.
- Gross, Michael; PRAMANIK, BIRENDRA N.; GANGULY, A. K. Applied electrospray mass spectrometry. New York, N.Y: Marcel Dekker, 2002. ISBN 978-0-8247-0618-0.
- Snyder, A. Peter. Biochemical and biotechnological applications of electrospray ionization mass spectrometry. Columbus, OH: American Chemical Society, 1996. ISBN 978-0-8412-3378-2.
- ALEXANDROV, M. L.; L. N. GALL; N. V. KRASNOV; V. I. NIKOLAEV; V. A. PAVLENKO; V. A. SHKUROV. Extraction of ions from solutions under atmospheric pressure as a method for mass spectrometric analysis of bioorganic compounds. Rapid Communications in Mass Spectrometry. 2008, s. 267–270. DOI 10.1002/rcm.3113. PMID 18181250. Bibcode 2008RCMS...22..267A.
Externí odkazy[editovat | editovat zdroj]
- Electrospray Ionization Primer National High Magnetic Field Laboratory
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku Electrospray ionization na anglické Wikipedii.
- ↑ Electrospray Ionisation Mass Spectrometry: Principles and Clinical Applications. Clin Biochem Rev. 2003. PMID 18568044.
- ↑ James J. Pitt. Principles and Applications of Liquid Chromatography-Mass Spectrometry in Clinical Biochemistry. Clin Biochem Rev. 2009. PMID 19224008.
- ↑ Masamichi Yamashita; John B. Fenn. Electrospray ion source. Another variation on the free-jet theme. The Journal of Physical Chemistry. 1984, s. 4451–4459. DOI 10.1021/j150664a002.
- ↑ J. B. Fenn; M. Mann; C. K. Meng; S. F. Wong; C. M. Whitehouse. Electrospray ionization for mass spectrometry of large biomolecules. Science. 1989, s. 64–71. DOI 10.1126/science.2675315. PMID 2675315. Bibcode 1989Sci...246...64F.
- ↑ K. Markides; A. Gräslund. Advanced information on the Nobel Prize in Chemistry 2002 [online]. Dostupné online.
- ↑ L. Rayleigh. On the Equilibrium of Liquid Conducting Masses charged with Electricity. Philosophical Magazine. 1882, s. 184–186. Dostupné online. DOI 10.1080/14786448208628425.
- ↑ J. Zeleny. The electrical discharge from liquid points, and a hydrostatic method of measuring the electric intensity at their surfaces. Physical Review. 1914, s. 69–91. Dostupné online. DOI 10.1103/PhysRev.3.69. Bibcode 1914PhRv....3...69Z.
- ↑ C. T. Wilson; G. I. Taylor. The bursting of soap bubbles in a uniform electric field. Proceedings of the Cambridge Philosophical Society. 1925, s. 728. DOI 10.1017/S0305004100009609. Bibcode 1925PCPS...22..728W.
- ↑ J. J. Nolan. Universal scaling laws for the disintegration of electrified drops. Proceedings of the Royal Irish Academy. 1926, s. 28.
- ↑ W. A. Macky. Some Investigations on the Deformation and Breaking of Water Drops in Strong Electric Fields. Proceedings of the Royal Society A. 1931-10-01, s. 565–587. DOI 10.1098/rspa.1931.0168. Bibcode 1931RSPSA.133..565M.
- ↑ Geoffrey Taylor. Some Investigations on the Deformation and Breaking of Water Drops in Strong Electric Fields. Proceedings of the Royal Society A. 1964, s. 383–397. DOI 10.1098/rspa.1964.0151. Bibcode 1964RSPSA.280..383T.
- ↑ a b M. Dole; L. L. Mack; R. L. Hines; R. C. Mobley; L. D. Ferguson; M. B. Alice. Molecular Beams of Macroions. Journal of Chemical Physics. 1968, s. 2240–2249. Bibcode 1968JChPh..49.2240D.
- ↑ Birendra N. Pramanik; A. K. Ganguly; Michael L. Gross. Applied Electrospray Mass Spectrometry: Practical Spectroscopy Series. [s.l.]: CRC Press, 2002-02-28. ISBN 978-0-8247-4419-9. S. 4–.
- ↑ Press Release: The Nobel Prize in Chemistry 2002 [online]. The Nobel Foundation, 2002-10-09 [cit. 2011-04-02]. Dostupné online.
- ↑ B. P. Pozniak; R. B. Cole. Current Measurements within the Electrospray Emitter. JASMS. 2007, s. 737–748. DOI 10.1016/j.jasms.2006.11.012. PMID 17257852.
- ↑ Droplet Dynamics Changes in Electrostatic Sprays of Methanol-Water Mixtures. The Journal of Physical Chemistry A. 1998, s. 9154–9160. DOI 10.1021/jp982027z. Bibcode 1998JPCA..102.9154O.
- ↑ J. Fernández De La Mora. The Fluid Dynamics of Taylor Cones. Annual Review of Fluid Mechanics. 2007, s. 217–243. DOI 10.1146/annurev.fluid.39.050905.110159. Bibcode 2007AnRFM..39..217F.
- ↑ Richard B. Cole. Electrospray and MALDI Mass Spectrometry: Fundamentals, Instrumentation, Practicalities, and Biological Applications. [s.l.]: Wiley, 2010. Dostupné online. ISBN 978-0471741077. S. 4.
- ↑ K. Y. Li; A. K. Ray. Charge limits on droplets during evaporation. Langmuir. 2005, s. 3786–3794. DOI 10.1021/la047973n. PMID 15835938.
- ↑ a b c P. Kebarle; U. H. Verkerk. Electrospray: from ions in solution to ions in the gas phase, what we know now. Mass Spectrometry Reviews. 2009, s. 898–917. DOI 10.1002/mas.20247. PMID 19551695. Bibcode 2009MSRv...28..898K.
- ↑ J. V. Iribarne; B. A. Thomson. On the evaporation of small ions from charged droplets. Journal of Chemical Physics. 1976, s. 2287–2294. DOI 10.1063/1.432536. Bibcode 2007PNAS..104.1111N.
- ↑ a b S. Nguyen; J. B. Fenn. Gas-phase ions of solute species from charged droplets of solutions. Proceedings of the National Academy of Sciences of the United States of America. 2007, s. 1111–1117. DOI 10.1073/pnas.0609969104. PMID 17213314. Bibcode 1976JChPh..64.2287I.
- ↑ M. Gamero-Castaño. Direct measurement of ion evaporation kinetics from electrified liquid surfaces. Journal of Chemical Physics. 2000, s. 815. DOI 10.1063/1.481857. Bibcode 2000JChPh.113..815G.
- ↑ a b de la Mora Fernandez. Electrospray ionization of large multiply charged species proceeds via Dole's charged residue mechanism. Analytica Chimica Acta. 2000, s. 93–104. DOI 10.1016/S0003-2670(99)00601-7.
- ↑ C. J. Hogan; J. A. Carroll; H. W. Rohrs; P. Biswas; M. L. Gross. Combined charged residue-field emission model of macromolecular electrospray ionization. Analytical Chemistry. 2009, s. 369–377. DOI 10.1021/ac8016532. PMID 19117463.
- ↑ Lars Konermann. Unraveling the Mechanism of Electrospray Ionization. Analytical Chemistry. 2013, s. 2–9. DOI 10.1021/ac302789c. PMID 23134552.
- ↑ Anyin Li; Qingjie Luo; So-Jung Park; R. Graham Cooks. Synthesis and Catalytic Reactions of Nanoparticles formed by Electrospray Ionization of Coinage Metals. Angewandte Chemie International Edition. 2014, s. 3147–3150. ISSN 1433-7851. DOI 10.1002/anie.201309193. PMID 24554582.
- ↑ Anneli Kruve; Karl Kaupmees; Jaanus Liigand; Ivo Leito. Negative Electrospray Ionization via Deprotonation: Predicting the Ionization Efficiency. Analytical Chemistry. 2014, s. 4822–4830. ISSN 1433-7851. DOI 10.1021/ac404066v. PMID 24731109.
- ↑ G. C. Gale; R. D. Smith. Small Volume and Low Flow Rate Electrospray Ionization Mass Spectrometry for Aqueous Samples. Rapid Communications in Mass Spectrometry. 1993, s. 1017–1021. Dostupné online. DOI 10.1002/rcm.1290071111. Bibcode 1993RCMS....7.1017G.
- ↑ M. R. Emmett; R. M. Smith. Micro-electrospray mass spectrometry: ultra-high-sensitivity analysis of peptides and proteins. Journal of the American Society for Mass Spectrometry. 1994, s. 605–613. DOI 10.1016/1044-0305(94)85001-1. PMID 24221962.
- ↑ a b M. S. Wilm; M. Mann. Electrospray and Taylor-Cone theory, Dole's beam of macromolecules at last?. International Journal of Mass Spectrometry. 1994, s. 167–180. DOI 10.1016/0168-1176(94)04024-9. Bibcode 1994IJMSI.136..167W.
- ↑ Samuel M. Mugo; Richard D. Oleschuk. Nanoelectrospray emitters: Trends and perspective. Mass Spectrometry Reviews. 2009, s. 918–936. DOI 10.1002/mas.20248. PMID 19479726. Bibcode 2009MSRv...28..918G.
- ↑ a b A. Schmidt; M. Karas; T. Dülcks. Electrospray and Taylor-Cone theory, Dole's beam of macromolecules at last?. Journal of the American Society for Mass Spectrometry. 2003, s. 492–500. DOI 10.1016/S1044-0305(03)00128-4. PMID 12745218.
- ↑ J. Fernandez de la Mora; I. G. Loscertales. The Current Emitted by Highly Conducting Taylor Cones. Journal of Fluid Mechanics. 2006, s. 155–184. DOI 10.1017/S0022112094003472. Bibcode 1994JFM...260..155D.
- ↑ R. J. Pfeifer. Parametric Studies of Electrohydrodynamic Spraying. AIAA J.. 1968, s. 496–502. DOI 10.2514/3.4525. Bibcode 1968AIAAJ...6..496H.
- ↑ RSC Chemical Methods Ontology, Cold-spray ionisation mass spectrometry
- ↑ J. S. Page; K. Tang; R. T. Kelly; R. D. Smith. A subambient pressure ionization with nanoelectrospray (SPIN) source and interface for improved sensitivity in mass spectrometry. Analytical Chemistry. 2008, s. 1800–1805. DOI 10.1021/ac702354b. PMID 18237189.
- ↑ M. Karas; U. Bahr; T. Dülcks. Nano-electrospray ionization mass spectrometry: addressing analytical problems beyond routine. Fresenius' Journal of Analytical Chemistry. 2000-03-01, s. 669–676. ISSN 0937-0633. DOI 10.1007/s002160051561. PMID 11225778.
- ↑ I. Marginean; J. S. Page; A. V. Tolmachev; K. Tang; R. D. Smith. Achieving 50% Ionization Efficiency in Subambient Pressure Ionization with Nanoelectrospray. Analytical Chemistry. 2010, s. 9344–9349. DOI 10.1021/ac1019123. PMID 21028835.
- ↑ R. Graham Cooks; Zheng Ouyang; Zoltan Takats; Justin M. Wiseman. Ambient Mass Spectrometry. Science. 2006, s. 1566–1570. DOI 10.1126/science.1119426. PMID 16543450. Bibcode 2006Sci...311.1566C.
- ↑ a b c María Eugenia Monge; Glenn A. Harris; Prabha Dwivedi; Facundo M. Fernández. Mass Spectrometry: Recent Advances in Direct Open Air Surface Sampling/Ionization. Chemical Reviews. 2013, s. 2269–2308. ISSN 0009-2665. DOI 10.1021/cr300309q. PMID 23301684.
- ↑ Min-Zong Huang; Cheng-Hui Yuan; Sy-Chyi Cheng; Yi-Tzu Cho; Jentaie Shiea. Ambient Ionization Mass Spectrometry. Annual Review of Analytical Chemistry. 2010, s. 43–65. ISSN 1936-1327. DOI 10.1146/annurev.anchem.111808.073702. PMID 20636033. Bibcode 2010ARAC....3...43H.
- ↑ Z. Takáts; J. M. Wiseman; B. Gologan; R. G. Cooks. Mass Spectrometry Sampling Under Ambient Conditions with Desorption Electrospray Ionization. Science. 2004, s. 471–473. DOI 10.1126/science.1104404. PMID 15486296. Bibcode 2004Sci...306..471T.
- ↑ Z. Takáts; J. M. Wiseman; R. G. Cooks. Ambient mass spectrometry using desorption electrospray ionization (DESI): instrumentation, mechanisms and applications in forensics, chemistry, and biology. Journal of Mass Spectrometry. 2005, s. 1261–1275. DOI 10.1002/jms.922. PMID 16237663. Bibcode 2005JMSp...40.1261T.
- ↑ G. Vidal-de-Miguel; M. Macía; P. Pinacho; J. Blanco. Low-Sample Flow Secondary Electrospray Ionization: Improving Vapor Ionization Efficiency. Analytical Chemistry. 2012-10-16, s. 8475–8479. ISSN 0003-2700. DOI 10.1021/ac3005378. PMID 22970991.
- ↑ César Barrios-Collado; Guillermo Vidal-de-Miguel; Pablo Martinez-Lozano Sinues. Numerical modeling and experimental validation of a universal secondary electrospray ionization source for mass spectrometric gas analysis in real-time. Sensors and Actuators B: Chemical. 2016, s. 217–225. DOI 10.1016/j.snb.2015.09.073.
- ↑ L. Konermann; D. J. Douglas. Equilibrium unfolding of proteins monitored by electrospray ionization mass spectrometry: Distinguishing two-state from multi-state transitions. Rapid Communications in Mass Spectrometry. 1998, s. 435–442. DOI 10.1002/(SICI)1097-0231(19980430)12:8<435::AID-RCM181>3.0.CO;2-F. PMID 9586231. Bibcode 1998RCMS...12..435K.
- ↑ Nemes; Samita Goyal; Akos Vertes. Conformational and Noncovalent Complexation Changes in Proteins during Electrospray Ionization. Analytical Chemistry. 2008, s. 387–395. DOI 10.1021/ac0714359. PMID 18081323.
- ↑ Sobott; Robinson. Characterising electrosprayed biomolecules using tandem-MS—the noncovalent GroEL chaperonin assembly. International Journal of Mass Spectrometry. 2004, s. 25–32. DOI 10.1016/j.ijms.2004.05.010. Bibcode 2004IJMSp.236...25S.
- ↑ S. Vaidyanathan; D. R. Kell; R. Goodacre. Selective detection of proteins in mixtures using electrospray ionization mass spectrometry: influence of instrumental settings and implications for proteomics. Analytical Chemistry. 2004, s. 5024–5032. DOI 10.1021/ac049684+. PMID 15373437.
- ↑ T. Marginean; R. T. Kelly; R. J. Moore; D. C. Prior; B. L. LaMarche; K. Tang; R. D. Smith. Selection of the optimum electrospray voltage for gradient elution LC-MS measurements. Journal of the American Society for Mass Spectrometry. 2009, s. 682–688. DOI 10.1016/j.jasms.2008.12.004. PMID 19196520.
- ↑ Iavarone; John C. Jurchen; Evan R. Williams. Effects of solvent on the maximum charge state and charge state distribution of protein ions produced by electrospray ionization. Journal of the American Society for Mass Spectrometry. 2000, s. 976–985. DOI 10.1016/S1044-0305(00)00169-0. PMID 11073261.
- ↑ Garcia. The effect of the mobile phase additives on sensitivity in the analysis of peptides and proteins by high-performance liquid chromatography–electrospray mass spectrometry. Journal of Chromatography B. 2005, s. 111–123. DOI 10.1016/j.jchromb.2005.03.041. PMID 16213445.
- ↑ C. A. Teo; W. A. Donald. Solution additives for supercharging proteins beyond the theoretical maximum proton-transfer limit in electrospray ionization mass spectrometry. Analytical Chemistry. 2014, s. 4455–4462. DOI 10.1021/ac500304r. PMID 24712886.
- ↑ S. H. Lomeli; I. X. Peng; S. Yin; R. R. Loo; J. A. Loo. New reagents for increasing ESI multiple charging of proteins and protein complexes. Journal of the American Society for Mass Spectrometry. 2010, s. 127–131. DOI 10.1016/j.jasms.2009.09.014. PMID 19854660.
- ↑ S. H. Lomeli; S. Yin; R. R. Loo; J. A. Loo. Increasing charge while preserving noncovalent protein complexes for ESI-MS. Journal of the American Society for Mass Spectrometry. 2009, s. 593–596. DOI 10.1016/j.jasms.2008.11.013. PMID 19101165.
- ↑ S. Yin; J. A. Loo. Top-Down Mass Spectrometry of Supercharged Native Protein-Ligand Complexes. International Journal of Mass Spectrometry. 2011, s. 118–122. DOI 10.1016/j.ijms.2010.06.032. Bibcode 2011IJMSp.300..118Y.
- ↑ C. J. Krusemark; B. L. Frey; P. J. Belshaw; L. M. Smith. Modifying the charge state distribution of proteins in electrospray ionization mass spectrometry by chemical derivatization. Journal of the American Society for Mass Spectrometry. 2009, s. 1617–1625. DOI 10.1016/j.jasms.2009.04.017. PMID 19481956.
- ↑ P. Nemes; S. Goyal; A. Vertes. Conformational and noncovalent complexation changes in proteins during electrospray ionization. Analytical Chemistry. 2008, s. 387–395. DOI 10.1021/ac0714359. PMID 18081323.
- ↑ R. Ramanathan; R. Zhong; N. Blumenkrantz; S. K. Chowdhury; A. B. Alton. Response normalized liquid chromatography nanospray ionization mass spectrometry. Journal of the American Society for Mass Spectrometry. 2007, s. 1891–1899. DOI 10.1016/j.jasms.2007.07.022. PMID 17766144.
- ↑ V. Gabelica; C. Vreuls; P. Filée; V. Duval; B. Joris; E. D. Pauw. Advantages and drawbacks of nanospray for studying noncovalent protein-DNA complexes by mass spectrometry. Rapid Communications in Mass Spectrometry. 2002, s. 1723–1728. Dostupné online. DOI 10.1002/rcm.776. Bibcode 2002RCMS...16.1723G.
- ↑ T. Daubenfeld; A. P. Bouin; G. van der Rest. A deconvolution method for the separation of specific versus nonspecific interactions in noncovalent protein-ligand complexes analyzed by ESI-FT-ICR mass spectrometry. Journal of the American Society for Mass Spectrometry. 2006, s. 1239–1248. DOI 10.1016/j.jasms.2006.05.005. PMID 16793278.
- ↑ F. Rosu; E. Pauw; V. Gabelica. Electrospray mass spectrometry to study drug-nucleic acids interactions. Biochimie. 2008, s. 1074–1087. DOI 10.1016/j.biochi.2008.01.005. PMID 18261993.
- ↑ A. Wortmann; M. C. Jecklin; D. Touboul; M. Badertscher; R. Zenobi. Binding constant determination of high-affinity protein-ligand complexes by electrospray ionization mass spectrometry and ligand competition. Journal of Mass Spectrometry. 2008, s. 600–608. DOI 10.1002/jms.1355. PMID 18074334. Bibcode 2008JMSp...43..600W.
- ↑ a b M. C. Jecklin; D. Touboul; C. Bovet; A. Wortmann; R. Zenobi. Which electrospray-based ionization method best reflects protein-ligand interactions found in solution? a comparison of ESI, nanoESI, and ESSI for the determination of dissociation constants with mass spectrometry. Journal of the American Society for Mass Spectrometry. 2008, s. 332–343. DOI 10.1016/j.jasms.2007.11.007. PMID 18083584.
- ↑ D. Touboul; L. Maillard; A. Grässlin; R. Moumne; M. Seitz; J. Robinson; R. Zenobi. How to deal with weak interactions in noncovalent complexes analyzed by electrospray mass spectrometry: cyclopeptidic inhibitors of the nuclear receptor coactivator 1-STAT6. Journal of the American Society for Mass Spectrometry. 2009, s. 303–311. DOI 10.1016/j.jasms.2008.10.008. PMID 18996720.
- ↑ N. Czuczy; M. Katona; Z. Takats. Selective detection of specific protein-ligand complexes by electrosonic spray-precursor ion scan tandem mass spectrometry. Journal of the American Society for Mass Spectrometry. 2009, s. 227–237. DOI 10.1016/j.jasms.2008.09.010. PMID 18976932.
