Fenolftalein: Porovnání verzí
Bez shrnutí editace |
|||
| Řádek 31: | Řádek 31: | ||
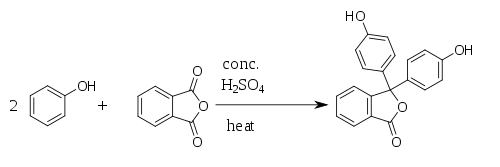
Fenolftalein byl poprvé připraven roku [[1871]] [[Němci|německým]] chemikem [[Adolf von Baeyer|Adolf von Baeyerem]] reakcí [[fenol]]u s [[Ftalanhydrid|ftalanhydridem]], z čehož pochází název fenolftalein. Reakce probíhá za katalýzy [[kyselina sírová|kyseliny sírové]] a za tepla (nesmí dojít k přehřátí, protože by se rozpadal ftalanhydrid). Při reakci vzniká jako vedlejší produkt voda. |
Fenolftalein byl poprvé připraven roku [[1871]] [[Němci|německým]] chemikem [[Adolf von Baeyer|Adolf von Baeyerem]] reakcí [[fenol]]u s [[Ftalanhydrid|ftalanhydridem]], z čehož pochází název fenolftalein. Reakce probíhá za katalýzy [[kyselina sírová|kyseliny sírové]] a za tepla (nesmí dojít k přehřátí, protože by se rozpadal ftalanhydrid). Při reakci vzniká jako vedlejší produkt voda. |
||
[[Soubor: |
[[Soubor:Phenolphthalein Synthesis.svg|500px|Výroba fenolftaleinu]] |
||
== Titrace == |
== Titrace == |
||
Verze z 17. 2. 2013, 14:24
Šablona:Infobox Chemická sloučenina
Fenolftalein je organická aromatická sloučenina. Často se používá při acidobazických titracích jako indikátor.
Výroba
Fenolftalein byl poprvé připraven roku 1871 německým chemikem Adolf von Baeyerem reakcí fenolu s ftalanhydridem, z čehož pochází název fenolftalein. Reakce probíhá za katalýzy kyseliny sírové a za tepla (nesmí dojít k přehřátí, protože by se rozpadal ftalanhydrid). Při reakci vzniká jako vedlejší produkt voda.
Titrace
Při acidobazických titracích se využívá barevného přechodu fenolftaleinu při změně pH. V kyselém prostředí je fenolftalein bezbarvý, v bazickém prostředí se zbarví fialově. K přechodu dochází při pH 8,2-9,8. Fenolftalein se používá ve formě roztoku v ethanolu.
Užití
Fenoltalein se používá jako projímadlo. V současné době se od jeho použití ustupuje z důvodu možné karcinogenity.
Fenolftalein společně s peroxidem vodíku se používá při testování přítomnosti krve, tzv. Kastle-Meyerův test.
Další použití nachází při výrobě hraček, např. mizejících inkoustů. Inkoust je smíchán s hydroxidem sodným, který reaguje se vzdušným oxidem uhličitým. Při reakci vzniká uhličitan sodný a klesá pH inkoustu. Pokles pH způsobí přechod fenolftaleinu z fialové do bezbarvé formy.

V tomto článku byl použit překlad textu z článku Phenolphtalein na anglické Wikipedii.