Nádorová kmenová buňka
| Nádorová kmenová buňka | |
|---|---|
Anatomie, fyziologie buňky | |
| Záznam kolonie kmenových buněk, pravděpodobně hemocytoblastů, postupně se vyvíjejících na rostoucí nádorové buňky procházející mitózu. (Cancer Cell International)
|
Nádorová kmenová buňka (CSC z angl. cancer stem cell) je typ nádorové buňky s některými vlastnostmi buňky kmenové – je schopná proliferovat a měnit se na jakýkoliv typ nádorové buňky v daném nádoru. Nádorové kmenové buňky byly nalezeny u mnoha druhů rakoviny[1] a předpokládá se, že se vyskytují u všech.[2] Jsou to často právě nádorové kmenové buňky, které odolávají chemoterapii.[1] První spolehlivý důkaz o existenci těchto buněk přinesla studie v Nature Medicine v roce 1997.[3]
Charakteristika
[editovat | editovat zdroj]Nádorové kmenové buňky tvoří malé procento všech buněk v nádoru. Od ostatních nádorových buněk se liší přítomností speciálních povrchových markerů na svých plazmatických membránách. Například nádorové kmenové buňky akutní myeloidní leukemie mají marker CD34 a nemají CD38; kmenové buňky nádorů mozku, jater či plic mají často marker CD133.[1] Od normálních kmenových buněk se liší nekontrolovaným růstem a množením (např. nejsou schopné kontaktní inhibice růstu).[1] Navíc mají velice nestabilní genom bohatý na chromozomové přestavby a chromozomové ztráty a také mají stabilní délku telomer. Pokud jsou s.c. (podkožně) injikovány do myší, dokáží na místě vytvořit nový nádor.[2]
Klinický význam
[editovat | editovat zdroj]
Pokud část nádorových kmenových buněk odolá chemoterapii, snadno dochází k relapsu (návratu) rakovinného bujení. Přitom právě nádorové kmenové buňky obvykle odolávají velice dobře, protože neproliferují a slouží tudíž jako „pojistka“ pro nádor.[2]
Součástí nových strategií léčby rakoviny je proto zacílení boje na nádorové kmenové buňky. Příkladem takové léčby je vlastně i transplantace kostní dřeně při onemocnění leukemií, protože kostní dřeň je právě místem, kde sídlí nádorové kmenové buňky zodpovědné za nekontrolované množení bílých krvinek v průběhu leukemie. V budoucnu by se měla léčba zaměřit na to, aby nádorové kmenové buňky zanikly tím, že by diferencovaly na normální nádorové buňky.[1](Obr. 1)
Modely propagace nádoru
[editovat | editovat zdroj]Nádorové buňky uvnitř různých typů nádorů se vyznačují funkční heterogenitou, jako je různá proliferační a diferenciační schopnost.[4] Objevení této funkční heterogenity buněk v nádorech vedlo k vzniku dvou modelů propagace nádorů.[5]
První model, označovaný jako model nádorových kmenových buněk nebo hierarchický model, popisuje skupinu nádorových buněk, které mají funkční vlastnosti charakteristické pro kmenové buňky, tj. schopnost sebeobnovy a diferenciace do různých typů nádorový buněk.[5] Tyto buňky byly pojmenovány jako nádorové kmenové buňky. Model nádorové kmenové buňky předpokládá, že buňky nádoru mají hierarchické uspořádání, na jehož vrcholu leží CSC.[6] (Obr. 3)


Druhý model popisující propagaci nádorů je označován jako model klonální evoluce. Základem modelu je, že mutované nádorové buňky s výhodou růstu jsou selektovány a následně pomnoženy. Buňky v této selektované populaci mají stejný potenciál pro zahájení růstu nebo regeneraci nádoru.[7] (Obr. 4).

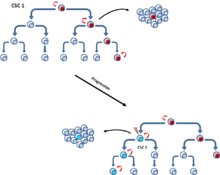
Oba modely se vzájemně nevylučuji, a právě naopak se předpokládá, že tyto modely jsou vzájemně spjaty. Vzájemná prolínavost modelů může vést k druhé populaci CSC, které mutace poskytla agresivnější vlastnosti.[8] (Obr. 5)
Původ CSC
[editovat | editovat zdroj]V roce 1997 Bonnet a Dick izolovali subpopulaci leukemických buněk, které exprimovaly specifický povrchový marker CD34 a zároveň na svém povrchu postrádaly marker CD38. Tato CD34+CD38− subpopulace buněk byla schopna iniciovat růst nádorů v NOD/SCID (non-obese diabetic mice with severe combined immunodeficiency disease) myších a byla pojmenována jako tumor iniciační buňky (tumor initiation cells) a později označována jako CSC (cancer stem cells). Podle modelu CSC, pouze malá frakce injikovaných buněk, nádorové kmenové buňky, má potenciál iniciovat nádor. Frekvence těchto buněk v akutní myeloidní leukemii představuje méně než 1 buňku na 10 000 nádorových buněk.[6] Bylo postulováno několik teorií o původu nádorových kmenových buněk, například mutanti embryonálních kmenových nebo progenitorových buněk, mutanti dospělých kmenových nebo progenitorových buněk, nebo také mutantní buňky, které získaly vlastnosti kmenových buněk.
Jedna z teorií předpokládá, že za vznik a vývoj CSC jsou zodpovědné mutace během vývoje buněk tvořících niku kmenových buněk. Následně dochází k vývoji mutovaných kmenových buněk v nice a jejich diferenciace vede k rozšíření mutace do diferencovaných stadií buněk. V důsledku získané mutace jsou dceřiné buňky náchylnější k získání nových mutací a k rozvoji nádorového bujení.[9] Další teorie popisující vznik a původ CSC zahrnuje dospělé kmenové buňky. Tato teorie je úzce spjata s tkáněmi s rychlou obměnou buněk, jako je kůže nebo gastrointestinální trakt (GIT). U těchto tkání se předpokládá, že tkáňově specifické kmenové buňky jsou zodpovědné za rozvoj nádorového bujení jako důsledek častého buněčného dělení v souvislosti s dlouhým životem kmenové buňky. Tato kombinace představuje vysoké riziko akumulace mutací, což je hlavní příčinou iniciace nádoru. Další možností vzniku CSC je schopnost mutovaných buněk de-diferenciace, která vede k získání vlastností kmenových buněk, jako je schopnost sebeobnovy a diferenciace v různé typy buněk.
Dalším konceptem příbuzným k těmto teoriím je předpoklad hierarchického uspořádání nádorů. Tento koncept vychází z předpokladu, že nádor je tvořen heterogenní populací buněk, které mají společné mutace, ale specificky se liší ve fenotypu. V tomto modelu je nádor tvořen několika typy CSC, které procházejí následnou selekcí mikroprostředí. výsledná sekundární selektovaná linie je tak adaptována na přítomné mikroprostředí.[10]
Izolace CSC
[editovat | editovat zdroj]Nádorové kmenové buňky byly identifikovány v mnoha nádorech. Pro jejich identifikace se používají stejné experimentální přístupy jako pro normální kmenové buňky.[11] Mezi tyto experimentální metody patří průtoková cytometrie pomocí protilátek směrovaných na markery nacházející se na buněčném povrchu, SP analýza (side population) nebo Aldefluor assay.[12] Populace obsahující lidské CSC purifikované těmito přístupy jsou následně implantovány v různých dávkách do imunodeficientních myší, kde se zjišťuje jejich schopnost iniciovat růst nádoru. Tato metoda in vivo je označována jako test limitního ředění (limiting dilution assay). Nádorová subpopulace schopná iniciovat růst nádoru v nízkém počtu je dále testována pro schopnost sebeobnovy.[13]
Nádorové kmenové buňky lze také identifikovat pomocí efektu MDR (multidrug resistence), za který jsou zodpovědné transportéry ABC (ATP-binding cassette), které umožní CSC transportovat z buňky do extracelulárního mikroprostředí barvivo Hoechst33242 vázající DNA a tím je odlišit od ostatních nádorových buněk.[12]
Další možný přístup při identifikaci subpopulace bohaté na CSC v in vitro systému představuje sphere-forming assay. Tato metoda je založena na schopnosti hematopoetických kmenových buněk a kmenových buněk tkání vytvářet za specifických podmínek sféroidy. Jedná se shluk buněk, uvnitř kterého dochází k diferenciaci buněk. Mnoho CSC izolovaných např. z mozku či z nádoru prostaty mělo schopnost vytvářet struktury podobné sféroidům.[14]
Heterogenita (znaky CSC)
[editovat | editovat zdroj]Mnohé studie demonstrovaly přítomnost nádorových kmenových buněk v mnoha solidních nádorech. Pro izolaci CSC ze solidních nádorů se nejčastěji používají specifické povrchové markery, ze kterých jsou některé charakteristické pro hematologické kmenové buňky nebo kmenové buňky tkání. Nicméně specifická skupina povrchových markerů se ukázala užitečná při identifikaci subpopulace bohaté na CSC. Jde zejména o molekuly CD133 (označován také jako PROM1), CD44, CD24, EpCAM (epithelial cell adhesion molecule, také znám jako ESA, epithelial specific marker), THY1, ATP-binding cassette B5 (ABCB5).[15]
- CD133 (prominin 1): glykoprotein obsahující 5 transmembránových domén, který je exprimován na CD34+ kmenových a progenitorových buňkách. Byl detekován pomocí glykosylovaného epitopu označovaného jako AC 133.
- EpCAM (epithelial cell adhesion molecule, ESA, TROP 1): adhezívní molekula exprimovaná na bazolaterálnim povrchu většiny epitelových buněk.
- CD90 (THY1): jedná se o glykoprotein ukotvený GPI kotvou v plazmatické membráně, který se podílí na signální transdukci. Je pravděpodobné, že se také podílí na adhesi thymocytů a stromatu thymu.
- CD44 (PGP1): adhezívní molekula, která hraje důležitou roli v mnoha procesech, jako migrace a signální transdukce. Bylo popsáno mnoho isoforem, jako je CD44H, která má vysokou afinitu k hyaluronátu, nebo CD44V, která se podílí na metastazování.
- CD24 (HSA): GPI kotvou vázána adhezívní molekula, která má důležitou roli v kostimulaci B a T lymfocytů. Hlavním ligandem této molekuly je P-selektin.
- ALDH1: aldehyd dehydrogenáza, která katalyzuje oxidaci aldehydů na karboxylové kyseliny. Například má také důležitou roli v procesu přeměny retinolu na kyselinu retinovou, který představuje důležitý fyziologický proces pro přežívání.[16]
Karcinom prsu představuje první solidní nádor, z kterého byly izolovány nádorové kmenové buňky. CSC izolovány z karcinomu prsu byly identifikovány jako CD44+CD24−/low[15], SP, ALDH+[17]. Nedávné studie ukázaly, že populace CSC nádoru prsu představují fenotypově heterogenní populaci buněk. Navíc bylo dokázáno, že CSC jsou heterogenní nejenom v expresi povrchových markérů, ale také že existuje celá řada subpopulací.[18] Nicméně, CSC z karcinomu prsu jsou nejčastěji identifikovány jako CD44+CD49fhiCD133hi.
Kmenové nádorové buňky byly také identifikovány u nádoru mozku. Pro jejich identifikaci se používají markery CD133[19], SSEA-1 (stage/specific embryonic antigen-1)[20], EGFR[21] a CD44.[22] Nicméně používání markeru CD133 pro identifikaci CSC je zatím velmi diskutabilní, protože obě populace CD133+ a CD133− jsou u některých gliomů tumorigenní a také populace CD133+ nemá schopnost iniciovat růst nádoru u všech nádorů mozku.[22]
Nádorové kmenové buňky byly také identifikovány v nádorech tlustého střeva.[23] Povrchové markery pro jejich identifikaci jsou CD133, CD44[24] a ABCB5.[25] Podobně jako v případě nádorů mozku, i u nádorů tlustého střeva, vedlo používání markeru CD133 pro pozitivní selekci k matoucím výsledkům. Nicméně, některé studie demonstrovaly, že AC133 epitop, ale nikoliv CD133 protein, je specificky exprimován na povrchu CSC a jeho exprese se ztrácí během diferenciace.[26]
CSC byly izolovány také z mnoha jiných nádorů, jako nádoru prostaty[27], plic, jater, pankreatu či ledvin.[28] U nádoru prostaty byly CSC identifikovány v CD44+[29] subpopulaci jako CD44+α2β1+[30], TRA-1-60+CD151+CD166+[31] nebo ALDH+[32] populace. Naopak například u nádoru plic byly pro identifikaci CSC použity markery, jako je CD133+[33], ALDH+CD44+[34] a onkofetální protein 5T4+.[35]
Metastatické nádorové kmenové buňky
[editovat | editovat zdroj]Metastazování nádoru představuje hlavní příčinu úmrtí u pacientů. Ne každá nádorová buňka má však schopnost metastazovat do vzdálených tkání. Tento potenciál závisí na mnoha faktorech, které ovlivňují základní procesy, jako je růst, angiogenese nebo invase nádorových buněk. U mnoha epiteliálních nádorů se epithelial-mesenchymal transition (EMT) předpokládá za hlavní proces při metastazování nádoru.[36] EMT a jemu opačný proces MET (mesenchymal-epithelial transition) se během embryonálního vývoje podílejí na migraci buněk.[37] Je pravděpodobné, že proces EMT je kontrolován WNT a TGF-β (transforming growth factor) signálními drahami.[38] Proces EMT je charakterizován ztrátou membránového E-cadherinu na membránových spojích. Důležitou roli v tomto procesu hraje β-catenin. Právě translokace β-cateninu z oblasti membránových spojů do jádra může vést k ztrátě E-cadherinu a následně k procesu EMT. Mnohé studie demonstrovaly, že β-catenin translokovaný do jádra může přímo ovlivňovat transkripční aktivitu EMT asociovaných genů, jako je represor genu pro E-cadherin SLUG (také označován jako SNA12).[39]
Nedávné studie podporují teorii, že nádorové buňky, u kterých proběhl proces EMT, mohou být prekurzory pro metastazující buňky, nebo dokonce metastazující CSC.[40] Na periferním okraji nádoru pankreatu byla identifikována populace buněk CD133+CXCR4+ (receptor pro chemokine CXCL12 známy také jako SDF1 ligand). Tato subpopulace vykazovala silnou migrační aktivitu na rozdíl od populace buněk CD133+CXCR4−, i když obě populace měly schopnost iniciovat rozvoj a metastazování nádorů.[41] Inhibice receptoru CXCR4 navíc vedla k redukci metastického potenciálu.[42]
Na druhou stranu, buňky CD44+CD24−/low byly identifikovány v pleurálním výpotku u nádoru prsu.[15] Navíc CD24+ populace buněk byla také identifikována ve vzdálených metastázách u pacientů s nádorem prsu.[43] Ačkoliv existuje velmi málo dat popisujících mechanismus metastazování nádorů prsu, je pravděpodobné, že CD44+CD24−/low populace buněk iniciuje metastázy a následně na novém místě dochází ke změně fenotypu a diferenciaci.[44] Na základě těchto výsledků byla postulována nová dynamická teorie dvoufázového expresního vzorce chování CSC. Principem tohoto konceptu je existence dvou forem nádorové kmenové buňky, stacionární kmenová buňka (SCS) a migrační nádorová kmenová buňka (MCS). SCS je zakotvena ve tkáni ve které perzistuje. Na druhé straně MSC nacházející se na rozhraní nádoru (tumor-host interface) představují hlavní příčinu metastazování nádorů. Navíc dokázáno, že MSC jsou derivované z SCS transientní aktivaci procesu EMT [45] (Obr. 6).

Využití v nádorové terapii
[editovat | editovat zdroj]Důkaz existence nádorových kmenových buněk vedl k novému nahlížení na léčbu a identifikaci nádorů, ale také ke vzniku nových přístupů při vývoji cytostatických léčiv. Normální kmenové buňky jsou přirozeně rezistentní na chemoterapeutická léčiva, jako důsledek exprese ABC transportérů, které jsou hlavní příčinou MDR (multidrug resistance) efektu. CSC, které vznikly z normálních kmenových buněk mutací, mohou také exprimovat na svém buněčném povrchu ABC pumpy a tím zvýšit rezistenci na chemoterapeutika, což vede k přežívání CSC a k relapsům nádorového onemocnění.[46]
V roce 2009 bylo identifikováno nové léčivo, Salinomycin, které selektivně redukuje počet CSC u nádorů prsu až 100 krát oproti klasickým cytostatickým léčivům, jako je paclitaxel, doxorubicin nebo docetaxel.[47]
Reference
[editovat | editovat zdroj]- ↑ a b c d e Stem Cells in Clinic and Research. [s.l.]: InTech, 2011. Dostupné online. ISBN 978-953-307-797-0.
- ↑ a b c Lucinei Roberto Oliveira, Andrielle de Castilho Fernandes, Alfredo Ribeiro-Silva. Cancer Stem Cells. Příprava vydání Stanley Shostak. [s.l.]: InTech, 2011. ISBN 978-953-307-580-8. Kapitola Stem Cells and Cancer Stem Cells.
- ↑ BONNET, D.; DICK, J. E. Human acute myeloid leukemia is organized as a hierarchy that originates from a primitive hematopoietic cell. Nat Med.. 1997, roč. 3, čís. 7, s. 730–7. Dostupné online. ISSN 1078-8956.
- ↑ HEPPNER, GH, Miller, BE. Tumor heterogeneity: biological implications and therapeutic consequences.. Cancer metastasis reviews. 1983, s. 5–23. PMID 6616442.
- ↑ a b REYA, T, Morrison, SJ; Clarke, MF; Weissman, IL. Stem cells, cancer, and cancer stem cells.. Nature. 2001 Nov 1, s. 105–11. PMID 11689955.
- ↑ a b BONNET, D, Dick, JE. Human acute myeloid leukemia is organized as a hierarchy that originates from a primitive hematopoietic cell.. Nature medicine. 1997 Jul, s. 730–7. PMID 9212098.
- ↑ BARABÉ, F, Kennedy, JA; Hope, KJ; Dick, JE. Modeling the initiation and progression of human acute leukemia in mice.. Science (New York, N.Y.). 2007 Apr 27, s. 600–4. PMID 17463288.
- ↑ CLARK, EA, Golub, TR; Lander, ES; Hynes, RO. Genomic analysis of metastasis reveals an essential role for RhoC.. Nature. 2000 Aug 3, s. 532–5. PMID 10952316.
- ↑ Wang Y, Yang J, Zheng H, Tomasek GJ, Zhang P, McKeever PE, Lee EY, Zhu Y. Expression of mutant p53 proteins implicates a lineage relationship between neural stem cells and malignant astrocytic glioma in a murine model. Cancer Cell. 2009, s. 514–26. DOI 10.1016/j.ccr.2009.04.001. PMID 19477430.
- ↑ Clarke MF, Dick JE, Dirks PB, Eaves CJ, Jamieson CH, Jones DL, Visvader J, Weissman IL, Wahl GM. Cancer stem cells--perspectives on current status and future directions: AACR Workshop on cancer stem cells. Cancer Research. 2006, s. 9339–44. DOI 10.1158/0008-5472.CAN-06-3126. PMID 16990346.
- ↑ GOLEBIEWSKA, A, Brons, NH; Bjerkvig, R; Niclou, SP. Critical appraisal of the side population assay in stem cell and cancer stem cell research.. Cell stem cell. 2011 Feb 4, s. 136–47. PMID 21295271.
- ↑ a b SCHARENBERG, CW, Harkey, MA; Torok-Storb, B. The ABCG2 transporter is an efficient Hoechst 33342 efflux pump and is preferentially expressed by immature human hematopoietic progenitors.. Blood. 2002 Jan 15, s. 507–12. PMID 11781231.
- ↑ PASTRANA, E, Silva-Vargas, V; Doetsch, F. Eyes wide open: a critical review of sphere-formation as an assay for stem cells.. Cell stem cell. 2011 May 6, s. 486–98. PMID 21549325.
- ↑ NICOLIS, SK. Cancer stem cells and "stemness" genes in neuro-oncology.. Neurobiology of disease. 2007 Feb, s. 217–29. PMID 17141509.
- ↑ a b c AL-HAJJ, M, Wicha, MS; Benito-Hernandez, A; Morrison, SJ; Clarke, MF. Prospective identification of tumorigenic breast cancer cells.. Proceedings of the National Academy of Sciences of the United States of America. 2003 Apr 1, s. 3983–8. PMID 12629218.
- ↑ VISVADER, JE, Lindeman, GJ. Cancer stem cells in solid tumours: accumulating evidence and unresolved questions.. Nature reviews. Cancer. 2008 Oct, s. 755–68. PMID 18784658.
- ↑ GINESTIER, C, Hur, MH; Charafe-Jauffret, E; Monville, F; Dutcher, J; Brown, M; Jacquemier, J; Viens, P; Kleer, CG; Liu, S; Schott, A; Hayes, D; Birnbaum, D; Wicha, MS; Dontu, G. ALDH1 is a marker of normal and malignant human mammary stem cells and a predictor of poor clinical outcome.. Cell stem cell. 2007 Nov, s. 555–67. PMID 18371393.
- ↑ DENG, S, Yang, X; Lassus, H; Liang, S; Kaur, S; Ye, Q; Li, C; Wang, LP; Roby, KF; Orsulic, S; Connolly, DC; Zhang, Y; Montone, K; Bützow, R; Coukos, G; Zhang, L. Distinct expression levels and patterns of stem cell marker, aldehyde dehydrogenase isoform 1 (ALDH1), in human epithelial cancers.. PloS one. 2010 Apr 21, s. e10277. PMID 20422001.
- ↑ SINGH, SK, Hawkins, C; Clarke, ID; Squire, JA; Bayani, J; Hide, T; Henkelman, RM; Cusimano, MD; Dirks, PB. Identification of human brain tumour initiating cells.. Nature. 2004 Nov 18, s. 396–401. PMID 15549107.
- ↑ SON, MJ, Woolard, K; Nam, DH; Lee, J; Fine, HA. SSEA-1 is an enrichment marker for tumor-initiating cells in human glioblastoma.. Cell stem cell. 2009 May 8, s. 440–52. PMID 19427293.
- ↑ MAZZOLENI, S, Politi, LS; Pala, M; Cominelli, M; Franzin, A; Sergi Sergi, L; Falini, A; De Palma, M; Bulfone, A; Poliani, PL; Galli, R. Epidermal growth factor receptor expression identifies functionally and molecularly distinct tumor-initiating cells in human glioblastoma multiforme and is required for gliomagenesis.. Cancer research. 2010 Oct 1, s. 7500–13. PMID 20858720.
- ↑ a b ANIDO, J, Sáez-Borderías, A; Gonzàlez-Juncà, A; Rodón, L; Folch, G; Carmona, MA; Prieto-Sánchez, RM; Barba, I; Martínez-Sáez, E; Prudkin, L; Cuartas, I; Raventós, C; Martínez-Ricarte, F; Poca, MA; García-Dorado, D; Lahn, MM; Yingling, JM; Rodón, J; Sahuquillo, J; Baselga, J; Seoane, J. TGF-β Receptor Inhibitors Target the CD44(high)/Id1(high) Glioma-Initiating Cell Population in Human Glioblastoma.. Cancer cell. 2010 Dec 14, s. 655–68. PMID 21156287.
- ↑ O'BRIEN, CA, Pollett, A; Gallinger, S; Dick, JE. A human colon cancer cell capable of initiating tumour growth in immunodeficient mice.. Nature. 2007 Jan 4, s. 106–10. PMID 17122772.
- ↑ DALERBA, P, Dylla, SJ; Park, IK; Liu, R; Wang, X; Cho, RW; Hoey, T; Gurney, A; Huang, EH; Simeone, DM; Shelton, AA; Parmiani, G; Castelli, C; Clarke, MF. Phenotypic characterization of human colorectal cancer stem cells.. Proceedings of the National Academy of Sciences of the United States of America. 2007 Jun 12, s. 10158–63. PMID 17548814.
- ↑ WILSON, BJ, Schatton, T; Zhan, Q; Gasser, M; Ma, J; Saab, KR; Schanche, R; Waaga-Gasser, AM; Gold, JS; Huang, Q; Murphy, GF; Frank, MH; Frank, NY. ABCB5 identifies a therapy-refractory tumor cell population in colorectal cancer patients.. Cancer research. 2011 Aug 1, s. 5307–16. PMID 21652540.
- ↑ KEMPER, K, Sprick, MR; de Bree, M; Scopelliti, A; Vermeulen, L; Hoek, M; Zeilstra, J; Pals, ST; Mehmet, H; Stassi, G; Medema, JP. The AC133 epitope, but not the CD133 protein, is lost upon cancer stem cell differentiation.. Cancer research. 2010 Jan 15, s. 719–29. PMID 20068153.
- ↑ LIU, C, Kelnar, K; Liu, B; Chen, X; Calhoun-Davis, T; Li, H; Patrawala, L; Yan, H; Jeter, C; Honorio, S; Wiggins, JF; Bader, AG; Fagin, R; Brown, D; Tang, DG. The microRNA miR-34a inhibits prostate cancer stem cells and metastasis by directly repressing CD44.. Nature medicine. 2011 Feb, s. 211–5. PMID 21240262.
- ↑ HO, MM, Ng, AV; Lam, S; Hung, JY. Side population in human lung cancer cell lines and tumors is enriched with stem-like cancer cells.. Cancer research. 2007 May 15, s. 4827–33. PMID 17510412.
- ↑ PATRAWALA, L, Calhoun, T; Schneider-Broussard, R; Li, H; Bhatia, B; Tang, S; Reilly, JG; Chandra, D; Zhou, J; Claypool, K; Coghlan, L; Tang, DG. Highly purified CD44+ prostate cancer cells from xenograft human tumors are enriched in tumorigenic and metastatic progenitor cells.. Oncogene. 2006 Mar 16, s. 1696–708. PMID 16449977.
- ↑ DUBROVSKA, A, Kim, S; Salamone, RJ; Walker, JR; Maira, SM; García-Echeverría, C; Schultz, PG; Reddy, VA. The role of PTEN/Akt/PI3K signaling in the maintenance and viability of prostate cancer stem-like cell populations.. Proceedings of the National Academy of Sciences of the United States of America. 2009 Jan 6, s. 268–73. PMID 19116269.
- ↑ RAJASEKHAR, VK, Studer, L; Gerald, W; Socci, ND; Scher, HI. Tumour-initiating stem-like cells in human prostate cancer exhibit increased NF-κB signalling.. Nature communications. 2011 Jan 18, s. 162. PMID 21245843.
- ↑ LI, T, Su, Y; Mei, Y; Leng, Q; Leng, B; Liu, Z; Stass, SA; Jiang, F. ALDH1A1 is a marker for malignant prostate stem cells and predictor of prostate cancer patients' outcome.. Laboratory investigation; a journal of technical methods and pathology. 2010 Feb, s. 234–44. PMID 20010854.
- ↑ ERAMO, A, Lotti, F; Sette, G; Pilozzi, E; Biffoni, M; Di Virgilio, A; Conticello, C; Ruco, L; Peschle, C; De Maria, R. Identification and expansion of the tumorigenic lung cancer stem cell population.. Cell death and differentiation. 2008 Mar, s. 504–14. PMID 18049477.
- ↑ SULLIVAN, JP, Spinola, M; Dodge, M; Raso, MG; Behrens, C; Gao, B; Schuster, K; Shao, C; Larsen, JE; Sullivan, LA; Honorio, S; Xie, Y; Scaglioni, PP; DiMaio, JM; Gazdar, AF; Shay, JW; Wistuba, II; Minna, JD. Aldehyde dehydrogenase activity selects for lung adenocarcinoma stem cells dependent on notch signaling.. Cancer research. 2010 Dec 1, s. 9937–48. PMID 21118965.
- ↑ DAMELIN, M, Geles, KG; Follettie, MT; Yuan, P; Baxter, M; Golas, J; DiJoseph, JF; Karnoub, M; Huang, S; Diesl, V; Behrens, C; Choe, SE; Rios, C; Gruzas, J; Sridharan, L; Dougher, M; Kunz, A; Hamann, PR; Evans, D; Armellino, D; Khandke, K; Marquette, K; Tchistiakova, L; Boghaert, ER; Abraham, RT; Wistuba, II; Zhou, BB. Delineation of a cellular hierarchy in lung cancer reveals an oncofetal antigen expressed on tumor-initiating cells.. Cancer research. 2011 Jun 15, s. 4236–46. PMID 21540235.
- ↑ THIERY, JP. Epithelial-mesenchymal transitions in tumour progression.. Nature reviews. Cancer. 2002 Jun, s. 442–54. PMID 12189386.
- ↑ ANGERER, LM, Angerer, RC. Regulative development of the sea urchin embryo: signalling cascades and morphogen gradients.. Seminars in cell & developmental biology. 1999 Jun, s. 327–34. PMID 10441547.
- ↑ MANI, SA, Yang, J; Brooks, M; Schwaninger, G; Zhou, A; Miura, N; Kutok, JL; Hartwell, K; Richardson, AL; Weinberg, RA. Mesenchyme Forkhead 1 (FOXC2) plays a key role in metastasis and is associated with aggressive basal-like breast cancers.. Proceedings of the National Academy of Sciences of the United States of America. 2007 Jun 12, s. 10069–74. PMID 17537911.
- ↑ CONACCI-SORRELL, M, Simcha, I; Ben-Yedidia, T; Blechman, J; Savagner, P; Ben-Ze'ev, A. Autoregulation of E-cadherin expression by cadherin-cadherin interactions: the roles of beta-catenin signaling, Slug, and MAPK.. The Journal of cell biology. 2003 Nov 24, s. 847–57. PMID 14623871.
- ↑ KAPLAN, RN, Riba, RD; Zacharoulis, S; Bramley, AH; Vincent, L; Costa, C; MacDonald, DD; Jin, DK; Shido, K; Kerns, SA; Zhu, Z; Hicklin, D; Wu, Y; Port, JL; Altorki, N; Port, ER; Ruggero, D; Shmelkov, SV; Jensen, KK; Rafii, S; Lyden, D. VEGFR1-positive haematopoietic bone marrow progenitors initiate the pre-metastatic niche.. Nature. 2005 Dec 8, s. 820–7. PMID 16341007.
- ↑ HERMANN, PC, Huber, SL; Herrler, T; Aicher, A; Ellwart, JW; Guba, M; Bruns, CJ; Heeschen, C. Distinct populations of cancer stem cells determine tumor growth and metastatic activity in human pancreatic cancer.. Cell stem cell. 2007 Sep 13, s. 313–23. PMID 18371365.
- ↑ YANG, ZF, Ho, DW; Ng, MN; Lau, CK; Yu, WC; Ngai, P; Chu, PW; Lam, CT; Poon, RT; Fan, ST. Significance of CD90+ cancer stem cells in human liver cancer.. Cancer cell. 2008 Feb, s. 153–66. PMID 18242515.
- ↑ SHIPITSIN, M, Campbell, LL; Argani, P; Weremowicz, S; Bloushtain-Qimron, N; Yao, J; Nikolskaya, T; Serebryiskaya, T; Beroukhim, R; Hu, M; Halushka, MK; Sukumar, S; Parker, LM; Anderson, KS; Harris, LN; Garber, JE; Richardson, AL; Schnitt, SJ; Nikolsky, Y; Gelman, RS; Polyak, K. Molecular definition of breast tumor heterogeneity.. Cancer cell. 2007 Mar, s. 259–73. PMID 17349583.
- ↑ SHMELKOV, SV, Butler, JM; Hooper, AT; Hormigo, A; Kushner, J; Milde, T; St Clair, R; Baljevic, M; White, I; Jin, DK; Chadburn, A; Murphy, AJ; Valenzuela, DM; Gale, NW; Thurston, G; Yancopoulos, GD; D'Angelica, M; Kemeny, N; Lyden, D; Rafii, S. CD133 expression is not restricted to stem cells, and both CD133+ and CD133- metastatic colon cancer cells initiate tumors.. The Journal of clinical investigation. 2008 Jun, s. 2111–20. PMID 18497886.
- ↑ BRABLETZ, T, Jung, A; Spaderna, S; Hlubek, F; Kirchner, T. Opinion: migrating cancer stem cells - an integrated concept of malignant tumour progression.. Nature reviews. Cancer. 2005 Sep, s. 744–9. PMID 16148886.
- ↑ DIRKS, P. Cancer stem cells: Invitation to a second round.. Nature. 2010 Jul 1, s. 40-1. DOI 10.1038/466040a. PMID 20596007.
- ↑ GUPTA, PB, Onder, TT; Jiang, G; Tao, K; Kuperwasser, C; Weinberg, RA; Lander, ES. Identification of selective inhibitors of cancer stem cells by high-throughput screening.. Cell. 2009 Aug 21, s. 645-59. DOI 10.1016/j.cell.2009.06.034. PMID 19682730.
Externí odkazy
[editovat | editovat zdroj] Obrázky, zvuky či videa k tématu Nádorová kmenová buňka na Wikimedia Commons
Obrázky, zvuky či videa k tématu Nádorová kmenová buňka na Wikimedia Commons
