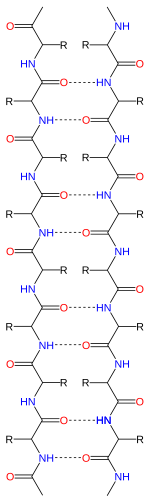
Beta-skládaný list
Beta-skládaný list (někdy jen skládaný list, anglicky beta sheet) je typ prostorového uspořádání bílkovin. Spolu s alfa-helixem představuje asi nejznámější pravidelné uspořádání v tzv. sekundární struktuře bílkovin.[1]
Struktura
[editovat | editovat zdroj]Beta-skládaný list je tzv. plně extendovaný typ struktury, to znamená, že na rozdíl od např. alfa-helixu není příliš kompaktní, ale do všech stran protažený. Skládá se z několika aminokyselinových řetězců (peptidů), které jsou uspořádány vzájemně rovnoběžně a dochází mezi nimi ke vzniku vodíkových vazeb (konkrétně mezi vodíkem amidové skupiny a kyslíkem karbonylové skupiny sousedních řetězců). Tím se tato struktura stává stabilnější.[2]
Sousední řetězce aminokyselin mohou být paralelní (tedy „směřovat“ stejným směrem) nebo antiparalelní (když směřují navzájem opačným směrem). Od tohoto uspořádání se odvíjí přesná struktura skládaného listu, záleží tedy, zda je paralelní nebo antiparalelní.[2]
Z beta skládaných listů se téměř výhradně skládá molekula fibroinu, tedy základní složky hedvábí.[1]