Oxid arsenitý: Porovnání verzí
m Změna způsobu zápisu obrázků v chemickém infoboxu dle ŽOPP z 10.7.2015 |
m Úprava parametrů infoboxu; kosmetické úpravy |
||
| Řádek 1: | Řádek 1: | ||
{{Infobox |
{{Infobox - chemická sloučenina |
||
| |
| název = Oxid arsenitý |
||
| |
| obrázek = Arsenic trioxide.jpg |
||
| |
|velikost obrázku=275px |
||
| |
|popisek=Oxid arsenitý |
||
| |
|obrázek2=Strukt_vzorec_As4O6.PNG |
||
| |
|velikost obrázku2=135px |
||
| |
|popisek2=Strukturní vzorec dimeru |
||
| |
|obrázek3=Arsenic-trioxide-3D-balls.png |
||
| |
|velikost obrázku3=135px |
||
| |
|popisek3=Prostorový vzorec oxidu arsenitého |
||
| |
| systematický název = Oxid arsenitý |
||
| |
| triviální název = Arsenik<br /> Otrušík |
||
| |
| anglický název = Arsenic trioxide |
||
| |
| německý název = Arsen(III)-oxid |
||
| |
| ostatní názvy = Utrejch <br /> Utrých |
||
| |
| číslo CAS = 1327-53-3 |
||
| |
| číslo EINECS = 215-481-4 |
||
| PubChem = 518740 |
| PubChem = 518740 |
||
| |
| sumární vzorec = As<sub>4</sub>O<sub>6</sub> |
||
| |
| vzhled = Bílá pevná látka |
||
| |
| molární hmotnost = 197,841 5 g/mol (''As<sub>2</sub>O<sub>3</sub>'')<br /> 395,682 8 g/mol (''As<sub>4</sub>O<sub>6</sub>'') |
||
| |
| teplota tání = 278 °C (''modifikace α'')<br /> 314 °C (''modifikace β'') |
||
| |
| teplota varu = 457,2 °C (''modifikace α'')<br /> 457,2 °C (''modifikace β'') |
||
| |
| teplota sublimace = 193 °C (''modifikace γ'') |
||
| |
| hustota = 3,865 g/cm<sup>3</sup> (''modifikace α, 25 °C'')<br />4,15 g/cm<sup>3</sup> (''modifikace β, 25 °C'')<br /> 3,738 (''modifikace γ'') |
||
| |
| tvrdost = 1,5 |
||
| pKa = 9,2 |
| pKa = 9,2 |
||
| |
| rozpustnost = 1,21 g/100 ml (''0 °C'')<br /> 2,047 g/100 ml (''25 °C'')<br /> 2,93 g/100 ml (''40 °C'')<br /> 4,4 g/100 ml (''60 °C'')<br /> 5,6 g/100 ml (''75 °C'')<br /> 8,16 g/100 ml (''98,5 °C'') (''modifikace α'') <br /> 3,738 g/100 ml (''20 °C'')<br /> 10,14 g/100 ml (''100 °C'') (''modifikace γ'') |
||
| |
| měrná magnetická susceptibilita = -2,978·10<sup>-6</sup> cm<sup>3</sup>g<sup>-1</sup> |
||
| |
| struktura = zobrazit |
||
| |
| krystalová struktura = [[Krystalografická soustava#Krychlová (kubická)|krychlová]] (''modifikace α'')<br /> [[Krystalografická soustava#KJednoklonná (monoklinická)|jednoklonná]] (''modifikace β'') <br /> [[amorfní látka|amorfní]] (''modifikace γ'') |
||
| |
| hrana mřížky = a= 1 107,44 (''modifikace α'')<br /> a:b:c = 0,409:1:0,349 (''modifikace β'') |
||
| |
| dipólový moment= 0 [[Debye|D]] |
||
| |
| termodynamické vlastnosti = zobrazit |
||
| |
| standardní slučovací entalpie = -1 334,7 kJ/mol (''modifikace α'')<br /> -1 331,6 J/mol (''modifikace β'') |
||
| |
| entalpie tání = 122,6 J/g (''modifikace α'')<br /> 141,8 J/g (''modifikace β'') |
||
| |
| entalpie varu = 114 J/g (''modifikace α'')<br /> 141,8 J/g (''modifikace β'') |
||
| |
| standardní molární entropie = 233,5 JK<sup>-1</sup>mol<sup>-1</sup> (''modifikace α'') <br /> 245 JK<sup>-1</sup>mol<sup>-1</sup> (''modifikace β'') |
||
| |
| standardní slučovací Gibbsova energie = -1 176,4 kJ/mol (''modifikace α'')<br /> -1 178,8 J/mol (''modifikace β'') |
||
| |
| izobarické měrné teplo = 0,516 JK<sup>-1</sup>g<sup>-1</sup> (''25 °C, modifikace α'') <br /> 0,561 JK<sup>-1</sup>g<sup>-1</sup> (''25 °C, modifikace β'') |
||
| |
| bezpečnost = zobrazit |
||
| |
| symboly nebezpečí = {{Vysoce toxický}} {{Nebezpečný pro životní prostředí}} |
||
| R-věty = {{R|45}}, {{R|28}}, {{R|34}}, {{R|50/53}} |
| R-věty = {{R|45}}, {{R|28}}, {{R|34}}, {{R|50/53}} |
||
| S-věty = {{S|53}}, {{S|45}}, {{S|60}}, {{S|61}} |
| S-věty = {{S|53}}, {{S|45}}, {{S|60}}, {{S|61}} |
||
| NFPA 704 = {{NFPA 704 |
| NFPA 704 = {{NFPA 704 |
||
| |
|zdraví=3 |
||
| |
|hořlavost=0 |
||
| |
|reaktivita=2}} |
||
}} |
}} |
||
'''Oxid arsenitý''', známý také pod [[triviální název|triviálním názvem]] '''arsenik''' nebo '''otrušík''', případně pod staršími českými jmény '''utrejch''' nebo '''utrých''', je jeden ze tří{{Doplňte zdroj}} [[Oxidy| |
'''Oxid arsenitý''', známý také pod [[triviální název|triviálním názvem]] '''arsenik''' nebo '''otrušík''', případně pod staršími českými jmény '''utrejch''' nebo '''utrých''', je jeden ze tří{{Doplňte zdroj}} [[Oxidy|oxidů]] [[arsen]]u. Setkáváme se s ním nejčastěji v podobě bílého [[krystal]]ického nebo [[amorfní látka|amorfního]] prášku nebo hrudek. Jedná se o látku bez zápachu, velmi [[toxicita|toxickou]]. Arsen má rovněž [[karcinogen]]ní účinky, tudíž může při dlouhodobé otravě dojít k rozvoji [[Rakovina|nádorů]], např. rakoviny kůže, plic nebo jater. |
||
== Příprava a vlastnosti == |
== Příprava a vlastnosti == |
||
Připravuje se [[redoxní reakce|oxidací]] [[Kovy| |
Připravuje se [[redoxní reakce|oxidací]] [[Kovy|kovového]] práškového arsenu [[vzduch|vzdušným]] [[kyslík]]em při zahřívání na vyšší [[teplota|teplotu]]: |
||
:4 As + 3 O<sub>2</sub> → As<sub>4</sub>O<sub>6</sub>, |
:4 As + 3 O<sub>2</sub> → As<sub>4</sub>O<sub>6</sub>, |
||
| Řádek 108: | Řádek 108: | ||
* pruhy na nehtech a jejich lámavost |
* pruhy na nehtech a jejich lámavost |
||
V místech, kde byly [[podzemní voda|podzemní vody]], užívané jako zdroj [[pitná voda|pitné vody]], bohaté na sloučeniny arsenu, je známo, že organismus místních obyvatel si na nadměrný přísun arsenu do těla zvykl a projevy chronické otravy se buď neprojevily vůbec, nebo byly jen velmi mírné. Dnes je tento jev díky chemické kontrole zdrojů vody velmi vzácný. Může se však objevit tam, kde nebylo správně naloženo s uzavřenými [[Důl| |
V místech, kde byly [[podzemní voda|podzemní vody]], užívané jako zdroj [[pitná voda|pitné vody]], bohaté na sloučeniny arsenu, je známo, že organismus místních obyvatel si na nadměrný přísun arsenu do těla zvykl a projevy chronické otravy se buď neprojevily vůbec, nebo byly jen velmi mírné. Dnes je tento jev díky chemické kontrole zdrojů vody velmi vzácný. Může se však objevit tam, kde nebylo správně naloženo s uzavřenými [[Důl|důlními]] díly; příkladem může být výskyt arsenu ve vodě a [[Půda (pedologie)|půdě]] u [[Kutná Hora|Kutné Hory]] jako důsledek unikající vody z bývalého dolu na [[Kaňk (352 m)|Kaňku]].<ref>[http://www.mu.kutnahora.cz/data/pageadds/1265_OHS.doc Výsledky screeningu možné zátěže arsenem a kadmiem obyvatel Kutné Hory provedené v listopadu 2000 v Malíně]</ref> |
||
=== Léčení === |
=== Léčení === |
||
Verze z 30. 8. 2015, 19:13
| Oxid arsenitý | |
|---|---|
 Oxid arsenitý | |
Strukturní vzorec dimeru | |
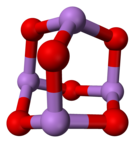 Prostorový vzorec oxidu arsenitého | |
| Obecné | |
| Systematický název | Oxid arsenitý |
| Triviální název | Arsenik Otrušík |
| Ostatní názvy | Utrejch Utrých |
| Anglický název | Arsenic trioxide |
| Německý název | Arsen(III)-oxid |
| Sumární vzorec | As4O6 |
| Vzhled | Bílá pevná látka |
| Identifikace | |
| Registrační číslo CAS | 1327-53-3 |
| EC-no (EINECS/ELINCS/NLP) | 215-481-4 |
| PubChem | 518740 |
| Vlastnosti | |
| Molární hmotnost | 197,841 5 g/mol (As2O3) 395,682 8 g/mol (As4O6) |
| Teplota tání | 278 °C (modifikace α) 314 °C (modifikace β) |
| Teplota varu | 457,2 °C (modifikace α) 457,2 °C (modifikace β) |
| Teplota sublimace | 193 °C (modifikace γ) |
| Hustota | 3,865 g/cm3 (modifikace α, 25 °C) 4,15 g/cm3 (modifikace β, 25 °C) 3,738 (modifikace γ) |
| Tvrdost | 1,5 |
| Disociační konstanta pKa | 9,2 |
| Rozpustnost ve vodě | 1,21 g/100 ml (0 °C) 2,047 g/100 ml (25 °C) 2,93 g/100 ml (40 °C) 4,4 g/100 ml (60 °C) 5,6 g/100 ml (75 °C) 8,16 g/100 ml (98,5 °C) (modifikace α) 3,738 g/100 ml (20 °C) 10,14 g/100 ml (100 °C) (modifikace γ) |
| Měrná magnetická susceptibilita | -2,978·10-6 cm3g-1 |
| Struktura | |
| Krystalová struktura | krychlová (modifikace α) jednoklonná (modifikace β) amorfní (modifikace γ) |
| Hrana krystalové mřížky | a= 1 107,44 (modifikace α) a:b:c = 0,409:1:0,349 (modifikace β) |
| Dipólový moment | 0 D |
| Termodynamické vlastnosti | |
| Standardní slučovací entalpie ΔHf° | -1 334,7 kJ/mol (modifikace α) -1 331,6 J/mol (modifikace β) |
| Entalpie tání ΔHt | 122,6 J/g (modifikace α) 141,8 J/g (modifikace β) |
| Entalpie varu ΔHv | 114 J/g (modifikace α) 141,8 J/g (modifikace β) |
| Standardní molární entropie S° | 233,5 JK-1mol-1 (modifikace α) 245 JK-1mol-1 (modifikace β) |
| Standardní slučovací Gibbsova energie ΔGf° | -1 176,4 kJ/mol (modifikace α) -1 178,8 J/mol (modifikace β) |
| Izobarické měrné teplo cp | 0,516 JK-1g-1 (25 °C, modifikace α) 0,561 JK-1g-1 (25 °C, modifikace β) |
| Bezpečnost | |
| R-věty | R45, R28, R34, R50/53 |
| S-věty | S53, S45, S60, S61 |
| NFPA 704 |  0
3
2
|
Některá data mohou pocházet z datové položky. | |
Oxid arsenitý, známý také pod triviálním názvem arsenik nebo otrušík, případně pod staršími českými jmény utrejch nebo utrých, je jeden ze tří[zdroj?] oxidů arsenu. Setkáváme se s ním nejčastěji v podobě bílého krystalického nebo amorfního prášku nebo hrudek. Jedná se o látku bez zápachu, velmi toxickou. Arsen má rovněž karcinogenní účinky, tudíž může při dlouhodobé otravě dojít k rozvoji nádorů, např. rakoviny kůže, plic nebo jater.
Příprava a vlastnosti
Připravuje se oxidací kovového práškového arsenu vzdušným kyslíkem při zahřívání na vyšší teplotu:
- 4 As + 3 O2 → As4O6,
případně žíháním arsenových rud za přístupu vzduchu, např. arsenopyritu:
- 4 FeAsS + 10 O2 → 2 Fe2O3 + As4O6 + 4 SO2,
přičemž čistý oxid arsenitý sublimuje při teplotě 315 °C (za normálního tlaku).
Oxid arsenitý se vyskytuje ve třech modifikacích: krystalizuje jednak v krychlové, jednak v jednoklonné soustavě, nebo jako amorfní forma. V roztoku a v plynné fázi se vyskytuje v dimerní formě (viz tabulka); teprve při zahřátí par nad 1800 °C se mění v monomerní formu sumárního vzorce As2O3. Je slabě rozpustný ve vodě a dobře rozpustný v kyselině chlorovodíkové za vzniku chloridu arsenitého:
- As4O6 + 12 HCl → 4 AsCl3 + 6 H2O
Oxid arsenitý je amfoterní, tzn. rozpouští se v kyselinách i v silných zásadách, např. hydroxidu draselném za vzniku solí kyseliny arsenité, arsenitanů, v tomto případě arsenitanu tridraselného:
- As4O6 + 12 KOH → 4 K3AsO3 + 6 H2O.
Kyslíkem se dále oxiduje na oxid arseničný:
- As4O6 + 2 O2 → As4O10.
V přírodě se oxid arsenitý nachází ve formě minerálů arsenolitu, tzv. arsenový květ (krychlová modifikace) a claudetitu (jednoklonná modifikace).
Použití
V minulosti nacházel velmi široké uplatnění:
- příprava jiných sloučenin arsenu v anorganické a organické chemii
- výroba skla (čeření skla)
- výroba emailů a barev (tzv. arseniková zeleň)
- konzervace kůže a dřeva
- jako součást jedů na hlodavce (rodenticidy)
- jako součást prostředků pro hubení roztočů (akaricidy)
Oxid arsenitý se v současnosti již k těmto účelům nevyužívá, zejména z důvodu jeho toxicity, karcinogenity a nepříznivého vlivu na přírodní prostředí.
Otrava arsenikem
Otrava arsenikem je nejčastějším případem otravy sloučeninami arsenu. Přibližně 1000 let byl arsenik užíván jako jed na hlodavce, protože je bezbarvý, bez chuti a zápachu. Na přelomu 19. a 20. století byl užíván v medicíně jako Fowlerův roztok (Liquor Kalii arsenicosi) v jednoprocentní směsi s uhličitanem draselným, zejména k léčení kožních onemocnění. Při předávkování tento koktejl způsoboval vleklou (chronickou) otravu.
Smrt nastává po požití 0,3 g arseniku (s ohledem na individuální stav osoby). Při dostatečně velké dávce nastává smrt během několika hodin. Smrtná dávka (LD50) je 20 mg/kg.[zdroj?]
Příznaky otravy
Příznaky akutní otravy jsou bolest břicha, nucení ke zvracení a třes. Při požití menší dávky nebo při vleklé otravě nastupují příznaky apatie, zvracení, průjem, později dehydratace, selhání ledvin. Pokud postižená osoba přežije toto období, dochází k trvalému poškození jater a nervového systému (polyneuropatie).
Jinými běžnými příznaky vleklé otravy jsou:
- kožní změny
- zánět středního ucha
- bolesti břicha
- průjmy
- poruchy periferní cirkulace krve
- úbytek míšní hmoty
- padání vlasů
- pruhy na nehtech a jejich lámavost
V místech, kde byly podzemní vody, užívané jako zdroj pitné vody, bohaté na sloučeniny arsenu, je známo, že organismus místních obyvatel si na nadměrný přísun arsenu do těla zvykl a projevy chronické otravy se buď neprojevily vůbec, nebo byly jen velmi mírné. Dnes je tento jev díky chemické kontrole zdrojů vody velmi vzácný. Může se však objevit tam, kde nebylo správně naloženo s uzavřenými důlními díly; příkladem může být výskyt arsenu ve vodě a půdě u Kutné Hory jako důsledek unikající vody z bývalého dolu na Kaňku.[1]
Léčení
- vypumpování žaludku s dodatkem magnesia
- podání protijedu metallorum Sautera
- léčení následného porušení elektrolytické rovnováhy těla, nízkého krevního tlaku aj.
Regulace
V lednu 2010 byl Evropskou agenturou pro chemické látky zařazen na kandidátský seznam nebezpečných látek vzbuzujících mimořádné obavy pro autorizaci dle směrnice REACH.[2]
Reference
Literatura
- VOHLÍDAL, JIŘÍ; ŠTULÍK, KAREL; JULÁK, ALOIS. Chemické a analytické tabulky. 1. vyd. Praha: Grada Publishing, 1999. ISBN 80-7169-855-5.


