Fluorid zirkoničitý
| Fluorid zirkoničitý | |
|---|---|
 | |
| Obecné | |
| Systematický název | fluorid zirkoničitý |
| Anglický název | Zirconium(IV) fluoride Zirconium tetrafluoride |
| Sumární vzorec | ZrF4 |
| Vzhled | bílý krystalický prášek |
| Identifikace | |
| Registrační číslo CAS | 7783-64-4 (bezvodý) 15298-38-1 (monohydrát) |
| SMILES | F[Zr](F)(F)F |
| InChI | 1S/4FH.Zr/h4*1H;/q;;;;+4/p-4 1/4FH.Zr/h4*1H;/q;;;;+4/p-4 |
| Vlastnosti | |
| Molární hmotnost | 167,210 g/mol |
| Teplota tání | 910 °C (1 183 K) |
| Hustota | 4,430 g/cm3 (20 °C) |
| Rozpustnost ve vodě | 1,32 g/100 ml (20 °C) 1,388 g/100 ml (25 °C) |
| Struktura | |
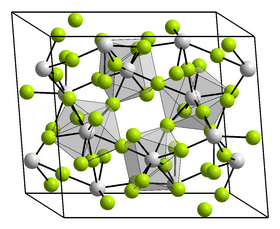
| Krystalová struktura | monoklinická |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
| Teplota vzplanutí | nehořlavý |
Některá data mohou pocházet z datové položky. | |
Fluorid zirkoničitý je anorganická sloučenina se vzorcem ZrF4. Je obtížně rozpustný ve vodě (viz infobox). Jedná se o hlavní složku fluorozirkoničitého skla. Je toxický, orální LD50 pro myši činí 98 mg/kg.
Struktura[editovat | editovat zdroj]
Jsou známy 3 krystalické fáze fluoridu zirkoničitého:
- α (monoklinická, prostorová grupa C12/c1, No 15)
- β (tetragonální, Pearsonův symbol tP40, P42/m, No 84)
- γ (neznámá struktura)
β a γ fáze jsou nestabilní a při teplotě 400 °C nevratně přecházejí do α fáze.[2]
Použití[editovat | editovat zdroj]
Fluorid zirkoničitý se používá jako zdroj zirkonia například ve výrobě kovů.[3]
ZrF4 může být přečištěn destilací nebo sublimací.[4]
Podmínky/látky, kterým je třeba se vyhnout, jsou vlhkost, některé kovy, kyseliny a oxidační činidla.
Odkazy[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Fluorid zirkoničitý na Wikimedia Commons
Obrázky, zvuky či videa k tématu Fluorid zirkoničitý na Wikimedia Commons
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku Zirconium(IV) fluoride na anglické Wikipedii.
- ↑ a b Zirconium(IV) fluoride. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-23]. Dostupné online. (anglicky)
- ↑ Paul L. Brown, Federico J. Mompean, Jane Perrone, Myriam Illemassène. Chemical thermodynamics of zirconium. [s.l.]: Gulf Professional Publishing, 2005. Dostupné online. ISBN 0-444-51803-7. S. 144.
- ↑ Zirconium fluoride [online]. American elements [cit. 2009-07-07]. Dostupné online.
- ↑ Method for preparing ultra-pure zirconium and hafnium tetrafluorides. United States Patent 4578252 [online]. [cit. 2009-07-07]. Dostupné online.


