Tyrosin
| Tyrosin | |
|---|---|
 | |
| Obecné | |
| Systematický název | (2S)-2-amino-3-(4-hydroxyfenyl)-propanová kyselina |
| Triviální název | tyrosin |
| Sumární vzorec | C9H11NO3 |
| Identifikace | |
| Registrační číslo CAS | 60-18-4 |
| Vlastnosti | |
| Molární hmotnost | 181,19 g/mol |
| Disociační konstanta pKa | pKCOOH:2,20 pKNH2: 9,21 pK(fenol)=10,46 |
| Izoelektrický bod | 5,66 |
Některá data mohou pocházet z datové položky. | |
Tyrosin (Tyr, Y) je jednou z 20 základních proteinogenních aminokyselin. Není esenciální aminokyselinou.[1] Řadí se k polárním aminokyselinám, také patří do skupiny aminokyselin s aromatickým postranním řetězcem (spolu s fenylalaninem, tryptofanem a histidinem). Od fenylalaninu se liší pouze hydroxylovou skupinou na čtvrtém uhlíku benzenového jádra.
Tyrosin v určité sekvenci v proteinu může být rozpoznáván některou z tyrosinkináz a fosforylován (Tyr-fosforylace, tj. fosforylace na tyrosinu, která se odehrává na tyrosinkinázových receptorech). Fosforylace tyrosinu může ovlivnit funkce proteinu (aktivace/deaktivace enzymů, změna vazebných schopností, změna substrátové specifity). Tyrosin však může být i sulfonován (pomocí sulfotransferáz).
Biologicky významné deriváty
K biologicky významným derivátům patří:
- fosfotyrosin - fosforylací tyrosinu v proteinu se ovlivňují funkce příslušného proteinu (způsobují tyrosinkinázy)
- katecholaminy
- adrenalin (epinefrin) – hormon dřeni nadledvin a neurotransmiter (hlavně sympatiku)
- noradrenalin (norepinefrin) – hormon dřeni nadledvin, méně účinný analog adrenalinu
- dopamin – neurotransmiter
- hormony štítné žlázy
- trijodthyronin (T3)
- thyroxin (T4)
Tyrosin je prekurzorem také pro:
- melanin - jeden ze základních pigmentů, v kůži
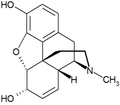
- morfin - alkaloid získávaný z máku setého (Papaver somniferum)
-
adrenalin (epinefrin)
-
noradrenalin (norepinefrin)
-
dopamin
-
triiodtyronin
-
thyroxin
-
morfin
Reference
 Obrázky, zvuky či videa k tématu tyrosin na Wikimedia Commons
Obrázky, zvuky či videa k tématu tyrosin na Wikimedia Commons
- ↑ Tyrosine [online]. University of Maryland Medical Center [cit. 2013-06-08]. Dostupné online. (anglicky)
Externí odkazy
- L-tyrozín. ForGym [online]. [cit. 2017-08-27]. Dostupné online. (slovensky)