Protrombinový čas
Protrombinový čas (anglic. prothrombin time, PT) je také nazýván jako tromboplastinový čas, Quickův test. Jde o laboratorní koagulační test, který monitoruje zevní systém hemokoagulace. Měří se čas, za který se (ve vzorku plazmy a po přídavku reagencie) vytvoří koagulum. Tento čas se dále přepočítává na protrombinový poměr (poměr času vzorku pacienta a času kontroly) a na mezinárodní normalizovaný poměr (INR).
PT umožňuje zjistit změny ve srážlivosti krve např. po podání warfarinu, po poškození jater i po snížení hladiny vitaminu K. Test sleduje správnou funkci koagulačních faktorů: II, V, VII, X a fibrinogenu.
Normální hodnota protrombinového testu je obvykle 12–15 s; normální rozsah INR je 0,8–1,2.
PT se často vyšetřuje společně s testem aPTT (aktivovaný částečný tromboplastinový čas), který monitoruje vnitřní systém hemokoagulace.
Laboratorní měření[editovat | editovat zdroj]
Metoda[editovat | editovat zdroj]
PT se nejčastěji vyšetřuje v krevní plazmě. Žilní krev se odebere do zkumavky obsahující citrát (3,8% citrát sodný, poměr citrátu a krve - 1:9), který zabrání srážení, protože váže vápník z odebrané krve. Nesrážlivá a dekalcifikovaná krev je poté promíchána, centrifugována, aby se oddělila vrstva plazmy, ze které se provede vyšetření. Poměr citrátu a krve by měl být vždy dodržen, aby naměřené výsledky byly přesné.
Vzorek se analyzuje v automatickém analyzátoru, který odebere přesné množství plazmy do plastové kyvety (ohřáté na 37 C) a přidá k ní opět přesné množství tromboplastinové reagencie (ta obsahuje tkáňový faktor a vápenaté ionty v množství, které eliminuje vliv citrátu). Od okamžiku přidání reagencie se měří čas až do vzniku koagula, které analyzátor zjistí např. opticky (podle změny rozptylu světla, které prochází kyvetou) nebo mechanicky (v kyvetě se pohybuje v magnetickém poli kovová kulička a její pohyb se v okamžiku vzniku koagula zastaví).
Vypočte se protrombinový poměr (protrombinový čas pacienta dělený protrombinovym časem normální plazmy).
Mezinárodní normalizovaný poměr (INR)[editovat | editovat zdroj]
Protrombinový čas změřený u zdravého člověka se bude měnit podle toho, jakým analytickým systémem se změří. Je to způsobeno rozdíly mezi šaržemi tkáňového faktoru, které výrobci používají při výrobě tromboplastinové reagencie. Proto bylo zavedeno INR, aby se mohly výsledky standardizovat.
Každý výrobce určí ke svému tkáňovému faktoru hodnotu ISI (Mezinárodní index citlivosti) a tato hodnota informuje o tom, jak je určitá šarže tkáňového faktoru srovnatelná s mezinárodně standardizovaným vzorkem. ISI ma obvykle hodnotu mezi 1,0 a 2,0.
INR se vypočte jako poměr protrombinového času pacienta a času normálního vzorku, který je umocněný na hodnotu ISI podle použitého analytického systému.
Hodnota INR také zohledňuje pacienty léčené kumariny (warfarin, ...). Matematická definice byla odvozena ze studie provedené v nemocnici v Betesdě.
Pro běžné stanovení dostačuje ratio PT, tedy poměr hodnot výsledku pacienta a kontrolního vzorku
Interpretace[editovat | editovat zdroj]
Protrombinový čas, jako čas do koagulace krevní plazmy od okamžiku přidání tkáňového faktoru a je měřítkem kvality zevního systému (a také společné cesty) hemokoagulace.
Rychlost aktivace zevního systému je výrazně ovlivněna hladinou faktoru VII v plazmě. Faktor VII má krátký poločas a k jeho syntéze je potřeba vitamin K. Protrombinový čas může být prodloužen jako výsledek nedostatku vitamínu K, který může vyvolat warfarin, špatné vstřebávání nebo nedostatečná kolonizace střeva mikroorganismy, které tento vitamín syntetizují (např. u novorozenců). Další příčinou může být nedostatečná syntéza faktoru VII (při jaterním onemocnění) nebo jeho zvýšená spotřeba (při diseminované intravaskulární koagulaci).
Vysoká hodnota INR např. 5 naznačuje vysokou pravděpodobnost krvácení.
Normální rozsah INR u zdravých osob je 0,8–1,2 a pro pacienty léčené warfarinem: 2,0–3,0.
Cílová hodnota INR může být v určitých situacích požadována vyšší, např. u pacientů s umělou srdeční chlopní.
Terapeutická hodnota se liší od fyziologické a to směrem nahoru, kdy je účelem upravit krevní srážení. Tyká se to hlavně onemocnění plic, srdce a trombóz dolních končetin. Po operacích se většinou nasazuje heparin, který neovlivňuje test PT.
Faktory ovlivňující přesnost výsledku[editovat | editovat zdroj]
Lupus antikoagulans je cirkulující inhibitor, který dává dispozici k trombóze, a interferuje s vyšetřením PT [1]
Také variace mezi různými tromboplastinovými přípravky vedly v minulosti ke snížené přesnosti výsledků INR, a studie z r.2005 ukázala, že i přes mezinárodní snahu o kalibraci (pomocí INR) existují statisticky významné rozdíly mezi různými diagnostickými soupravami [2] a je tak zpochybněna dlouhodobá udržitelnost PT/INR testu pro sledování antikoagulační terapie. [3]
Počet vyšetření[editovat | editovat zdroj]
Odhaduje se, že celosvětově se provede 800 miliónu PT/INR vyšetření za rok.[3]
Testování přímo u pacientů (anglic. near-patient testing, NPT)[editovat | editovat zdroj]
Kromě laboratorní metody popsané výše, se stále častěji v některých zemích provádí domácí monitoring INR. Ve Velké Británii se NPT testování využívá jak u pacientů doma, tak v některých klinikách zabývajících se antikoagulací (často součásti nemocnice), jako rychlá a spolehlivá alternativa k laboratornímu vyšetření. Po období pochyb o přesnosti NPT výsledků se zdá, že se objevuje nová generace přístrojů a reagencií poskytujících výsledky, které přesností odpovídají výsledkům laboratoře. [4]
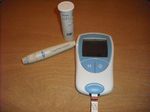
Typicky se pro NPT vyšetření používá malé stolní zřízení; např. CoaguCheck S firmy Roche nebo HemoSense INRatio. Pomocí automatické lancety se provede standardní vpich do prstu a kapka kapilární krve se umístí na testovací proužek, který se vloží do přístroje. Během několika sekund je na displeji zobrazeno výsledné INR. Podobné testovací metody již např. používají diabetici léčení inzulinem ke sledování hladiny glukózy v krvi - postup je jednoduchý a dá se snadno naučit.
Místní předpisy určují, jestli pacient nebo jen koagulační specialista (sestra, praktický lékař, nemocniční lékař) může interpretovat výsledky a stanovit dávku léků. V Německu si pacienti mohou dávku léků upravovat sami, zatímco v USA nebo ve Velké Británii to může provádět jen zdravotník. Např. pacienti, kteří využívají služby jako je Philips INR@Home [1], telefonují své INR výsledky každý týden a tato informace se přenáší k jejich lékaři, který je vždy upozorněn na výsledky mimo meze, které vyžadují okamžitou intervenci nebo úpravu léčby.
Významnou výhodou domácího testování je důkaz, že společně s lékařskou podporou a nastavením dávky léku samotným pacientem (tam, kde je to pro pacienty povoleno) vede toto testování ke zlepšení antikoagulační léčby. Meta analýza, která hodnotila 14 pokusů, ukázala, že domácí testování vedlo ke snížení výskytu komplikací (krvácení a trombóza) i k udržení INR v terapeutickém rozmezí.[5]
Mezi další výhody domácího testování patří jeho rychlost, spolehlivost, je méně bolestivé a umožňuje pacientům měřit si INR, kdykoli to potřebují. Nevýhodou je nutnost nanést kapku krve přesně na určité místo testovacího proužku (to může být problém u některých pacientů) a také je třeba uvážit cenu proužku. Ve Velké Británii jsou testovací proužky k dispozici na předpis - staří lidé a nezaměstnaní za ně nemusí platit a ostatní platí jen standardní poplatek za předpis, který představuje asi 20% ceny proužků.
V USA je domácí testování hrazeno organizací Medicare u pacientů s implantovanou srdeční chlopní, zatímco soukromé pojišťovny jej mohou hradit i v jiných případech. Medicare nyní pokrývá domácí testování u pacientů s chronickou fibrilací srdečních síní. Je vyžadován lékařský předpis.
Existují důkazy, že domácí testování může být méně přesné u určitých pacientů, např. pokud mají onemocnění lupus antikoagulans.
Direktivy[editovat | editovat zdroj]
Mezinárodní direktivy stanovující podmínky pro domácí monitorování antikoagulační léčby vydala v roce 2005 organizace International Self-Monitoring Association for Oral Anticoagulation.[6] Ve studii se uvádí: “bylo dosaženo shody, že domácí monitorování a řízení léčby samotným pacientem jsou efektivní metody pro sledování orální antikoagulační léčby a její výsledky jsou stejné dobré a případně i lepší než výsledky dosažené na klinikách. Pacienti ale musí být vhodně vybíráni a školeni. V současnosti dostupná zařízení pro domácí monitorování a řízení léčby dávají INR výsledky srovnatelné s výsledky získanými v laboratořích.
Historie[editovat | editovat zdroj]
Protrombinový čas objevil Dr.Armand Quick a kol. v roce 1935 [7] a druhou metodu publikoval Dr Paul Owren[8] (také nazývaná "p a p" nebo metoda stanovení "protrombinu a prokonvertinu"). Metoda usnadnila identifikaci antikoagulancií dikumarolu a warfarinu,[9] a byla následně použita jako měřítko aktivity warfarinu při jeho terpeutickém použití.
Vyjadřování výsledků jako INR bylo zavedeno na začátku 80. let, když se ukázalo, že mezi různými testy pro stanovení protrombinového času existují velké rozdíly - způsobeno především problémy s čistotou tromboplastinového (tkáňový faktor) koncentrátu.[10]. INR pak bylo celosvětově uznáno, zvláště poté, co jej schválila Světová zdravotnická organizace.[11]
Dříve se výsledky Quickova testu uváděly v procentech, které vyjadřovaly srážlivost krve jakožto ekvivalent ředění plazmy zdravého jedince. Pokud měl Quickův test hodnotu např. 60%, znamenalo to přibližně, že pacient má 60% koagulačních faktorů vůči zdravému. K převodu času PT na procenta se používala kalibrační tabulka[12], která se připravovala pomocí různě ředěných roztoků plazmy zdravého jedince. Čím nižší je procentní vyjádření Quickova testu, tím větší je odpovídající hodnota INR.
Reference[editovat | editovat zdroj]
V tomto článku byl použit překlad textu z článku Prothrombin time na anglické Wikipedii.
- ↑ Della Valle P, Crippa L, Garlando AM, et al.. Interference of lupus anticoagulants in prothrombin time assays: implications for selection of adequate methods to optimize the management of thrombosis in the antiphospholipid-antibody syndrome. Haematologica. December 1999, roč. 84, čís. 12, s. 1065–74. Dostupné v archivu pořízeném dne 2011-10-02. PMID 10586206. Archivováno 2. 10. 2011 na Wayback Machine.
- ↑ Horsti J, Uppa H, Vilpo JA. Poor agreement among prothrombin time international normalized ratio methods: comparison of seven commercial reagents. Clin. Chem.. March 2005, roč. 51, čís. 3, s. 553–60. Dostupné v archivu pořízeném dne 2009-10-01. DOI 10.1373/clinchem.2004.043836. PMID 15665046.
- ↑ a b Jackson CM, Esnouf MP. Has the time arrived to replace the quick prothrombin time test for monitoring oral anticoagulant therapy?. Clin. Chem.. March 2005, roč. 51, čís. 3, s. 483–5. Dostupné v archivu pořízeném dne 2009-05-03. DOI 10.1373/clinchem.2004.045393. PMID 15738512.
- ↑ Poller L, Keown M, Chauhan N, et al.. European Concerted Action on Anticoagulation. Correction of displayed international normalized ratio on two point-of-care test whole-blood prothrombin time monitors (CoaguChek Mini and TAS PT-NC) by independent international sensitivity index calibration. Br. J. Haematol.. September 2003, roč. 122, čís. 6, s. 944–9. DOI 10.1046/j.1365-2141.2003.04521.x. PMID 12956765.
- ↑ Heneghan C, Alonso-Coello P, Garcia-Alamino JM, Perera R, Meats E, Glasziou P. Self-monitoring of oral anticoagulation: a systematic review and meta-analysis. Lancet. February 2006, roč. 367, čís. 9508, s. 404–11. DOI 10.1016/S0140-6736(06)68139-7. PMID 16458764.
- ↑ Guidelines for implementation of patient self-testing and patient self-management of oral anticoagulation. International consensus guidelines prepared by International Self-Monitoring Association for Oral Anticoagulation. International Journal of Cardiology. 10 March 2005. Dostupné v archivu pořízeném dne 2009-02-07.
- ↑ Quick AJ, Stanley-Brown M, Bancroft FW. A study of the coagulation defect in hemophilia and in jaundice. Am J Med Sci. 1935, roč. 190, s. 501. DOI 10.1097/00000441-193510000-00009.
- ↑ Owren PA, Aas K. The control of dicumarol therapy and the quantitative determination of prothrombin and proconvertin. Scand. J. Clin. Lab. Invest.. 1951, roč. 3, čís. 3, s. 201–8. DOI 10.3109/00365515109060600. PMID 14900966.
- ↑ Campbell HA, Smith WK, Roberts WL, Link KP. Studies on the hemorrhagic sweet clover disease. II. The bioassay of hemorrhagic concentrates by following the prothrombin level in the plasma of rabbit blood. J Biol Chem. 1941, roč. 138, s. 1–20.
- ↑ Hirsh J, Bates SM. Clinical trials that have influenced the treatment of venous thromboembolism: a historical perspective. Ann. Intern. Med.. March 2001, roč. 134, čís. 5, s. 409–17. Dostupné online. PMID 11242501.
- ↑ Anonymous. World Health Organ Tech Rep Ser. [s.l.]: [s.n.], 1983. Kapitola 33: Expert Committee on Biological Standardization. Requirements for thromboplastins and plasma used to control oral anticoagulant therapy, s. 81–105.
- ↑ Roche diagnostics: CoaguChek - Otázky a odpovědi Archivováno 27. 9. 2013 na Wayback Machine. česky
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Protrombinový čas na Wikimedia Commons
Obrázky, zvuky či videa k tématu Protrombinový čas na Wikimedia Commons

