Imunoglobulin A
Imunoglobulin A(Ig A) je jedna z 5 hlavních tříd lidských protilátek (imunoglobulinů) vyskytujících se u člověka. S IgA se můžeme setkat, jako s bílkovinou plazmy (glykoprotein), produkovanou plazmatickými buňkami a B lymfocyty v lymfoidních tkáních. Je ve velké míře uvolňován na povrch sliznic a významně se podílí na ochraně proti mikroorganismům. Jako ostatní imunoglobuliny může specificky interagovat s antigenními determinanty - malými molekulami bílkovin či polysacharidů volně, či na povrchu makromolekul nebo buněk (nádorové buňky, bakterie, např. povrch bakterie, může obsahovat mnoho různých antigenů), které se navážou na jeho vazebné místo (receptor), [1]

1 H-chain
2 L-chain
3 J-chain
4 secretory component
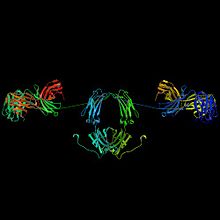
IgA B-lymfocyt[editovat | editovat zdroj]
které je tvořeno neuvěřitelně variabilními sekvencemi vzniklými také díky procesu genových přestaveb. IgA se vyskytuje ve dvou formách - slizniční a sérové. [2]
Význam[editovat | editovat zdroj]
Hlavní funkce IgA spolu s IgM je neutralizace antigenů na slizničním povrchu (proces imunitní exkluze), ve spolupráci s obrannými mechanismy sliznic (hlen, řasinky, peristaltika) jsou komplexy IgA (i IgG,IgM) s bakteriálními jedy, mikroorganismy a dalšími potenciálními škodlivými antigeny transportovány ven z organismu. Důležité je, že IgA nespouští komplement, který by mohl poškozovat sliznici. Komplexy s IgA však mohou fungovat jako opsonin = vázat na fcα receptor na různých efektorových buňkách (fagocytech, např. makrofázích, neutrofilech) a být posléze odstraňovány fagocytózou. Sekreční IgA je odolný proti působení některých enzymů, takže zabraňuje množení mikroorganismů v tělních sekretech a pomáhá tak chránit organismus proti pronikání cizorodých molekul. [2]
Výskyt[editovat | editovat zdroj]
Hlavní imunoglobulin slz, slin, v mateřském mléce, nachází se v nosním, bronchiálním, střevním, prostatickém, vaginálním sekretu.[1]
IgA může být dvojího izotopu IgA1, IgA2. V zažívacím traktu převládá IgA2 a v dýchacím traktu IgA1.[2]
Struktura[editovat | editovat zdroj]
Monomer imunoglobulinu se skládá ze 2 identických lehkých řetězců proteinů a ze 2 identických těžkých řetězců, které jsou k sobě drženy nekovalentními vazbami a disulfidovými můstky. Tato základní struktura je u slizničního IgA propojena proteinem J s další podjednotkou IgA do dimeru, navíc obsahuje jednotku sekreční komponenty. Sérový IgA je buď monomer, dimer nebo trimer, spojení mezi jednotlivými monomery také uskutečňuje protein J.[2]
Vznik slizničního IgA[editovat | editovat zdroj]
Na vnitřní straně epiteliální buňky se IgA váže na transportní Fc receptor (tzv. poly-Ig receptor). Komplex tohoto receptoru s IgA je pak endocytován a transportním váčkem přenesen na druhou stranu buňky (luminální stranu). Tam fúzuje s membránou a část receptorové molekuly spolu s navázaným IgA se proteolyticky odštěpí. Část sekreční molekuly, která zůstává spojena s IgA, se nazývá sekreční komponenta a zajišťuje IgA rezistenci vůči střevním proteázám. Tímto způsobem se také IgA dostává do mateřského mléka a z něj do zažívacího traktu novorozence. Tam má důležitou ochranou funkci v době, kdy jeho imunitní systém ještě IgA neprodukuje. [2]
Patologie[editovat | editovat zdroj]
Při deficitu IgA mohou jeho funkci vykonávat do určité míry IgM, v dolních cestách dýchacích IgG. Postižení jedinci nemusí mít klinické příznaky, častěji jsou ale náchylnější k respiračním infekcím, alergiím, autoimunitním a nádorovým chorobám.[2]
Reference[editovat | editovat zdroj]
Externí odkazy[editovat | editovat zdroj]
 Obrázky, zvuky či videa k tématu Imunoglobulin A na Wikimedia Commons
Obrázky, zvuky či videa k tématu Imunoglobulin A na Wikimedia Commons
